Содержание
- 2. Оксиды азота. Азот образует шесть кислородных соединений. степени окисления +1 N2O +2 NO +3 N2O3 +4
- 3. Получение: NH4NO = N2O +2H2O Химические свойства: 1. разложение при нагревании 2N2+1O = 2N20+O2 2. с
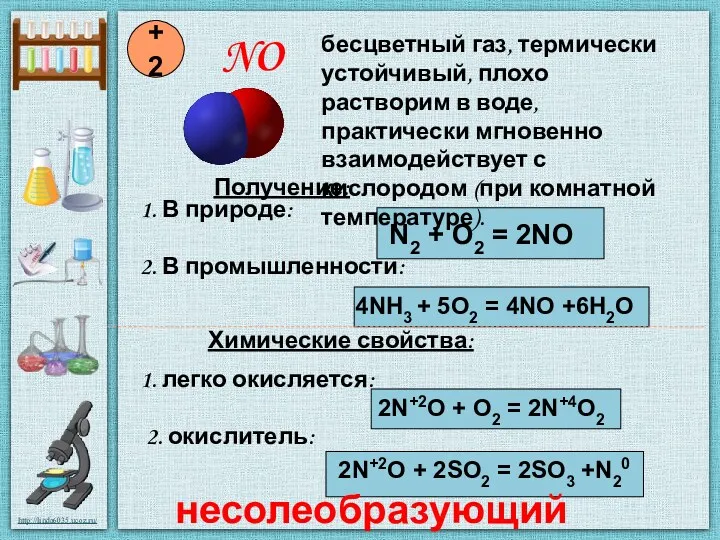
- 4. NO +2 Получение: 1. В природе: N2 + O2 = 2NO 2. В промышленности: 4NH3 +
- 5. N2O3 +3 Химические свойства: NO2 + NO N2O3 Получение: ВСЕ свойства кислотных оксидов. кислотный оксид жидкость
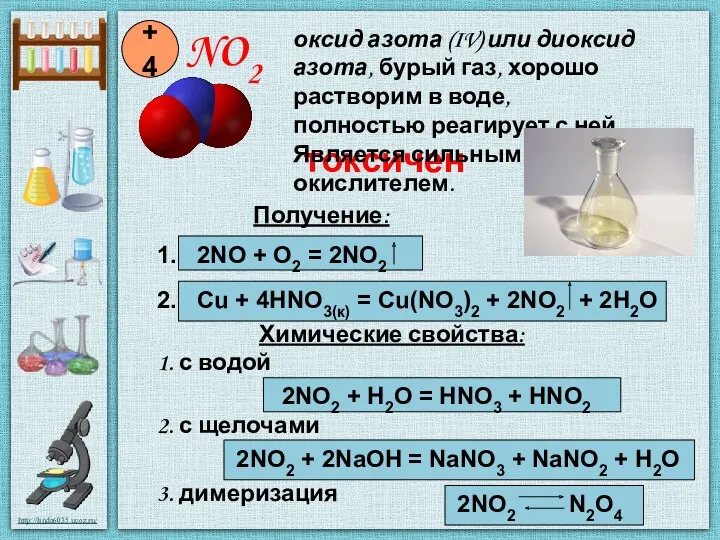
- 6. NO2 +4 Получение: 1. 2NO + O2 = 2NO2 2. Cu + 4HNO3(к) = Cu(NO3)2 +
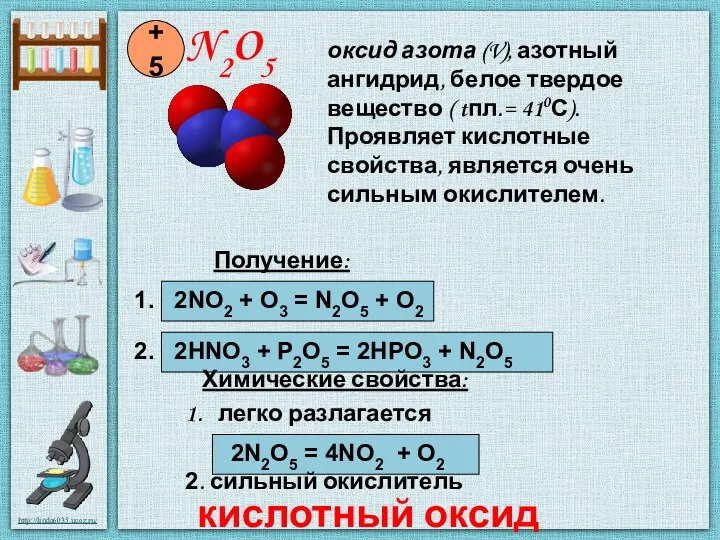
- 7. N2O5 +5 Получение: 1. 2NO2 + O3 = N2O5 + O2 2. 2HNO3 + P2O5 =
- 8. HNO3 Состав. Строение. Свойства. H O N O O — — степень окисления азота валентность азота
- 9. Азотная кислота (HNO3) Классификация по: наличию кислорода: основности: растворимости в воде: летучести: степени электролитической диссоциации: кислородсодержащая
- 10. Получение азотной кислоты в промышленности NH3 NO NO2 HNO3 4NH3+ 5O2 = 4NO + 6H2O 2NO+O2
- 11. В лаборатории азотную кислоту получают действием концентрированной серной кислоты на нитраты при слабом нагревании. NaNO3 +
- 12. Химические свойства азотной кислоты Азотная кислота проявляет все типичные свойства кислот. 1. Свойства HNO3 как электролита:
- 13. 2. Окислительные свойства: особенности взаимодействия с металлами: (азотная кислота никогда не выделяет водород!) Me + HNO3
- 14. С металлами, стоящими в ряду напряжений левее водорода: С металлами, стоящими в ряду напряжений правее водорода:
- 15. 2. Окислительные свойства 2) Особенности взаимодействия с неметаллами (S, P, C): 3) Взаимодействует с органическими веществами
- 16. Применение азотной кислоты 1 5 4 6 2 3 Производство азотных и комплексных удобрений. Производство взрывчатых
- 17. Нитраты – соли азотной кислоты, получают при действии кислоты на металлы, их оксиды и гидроксиды. Селитры
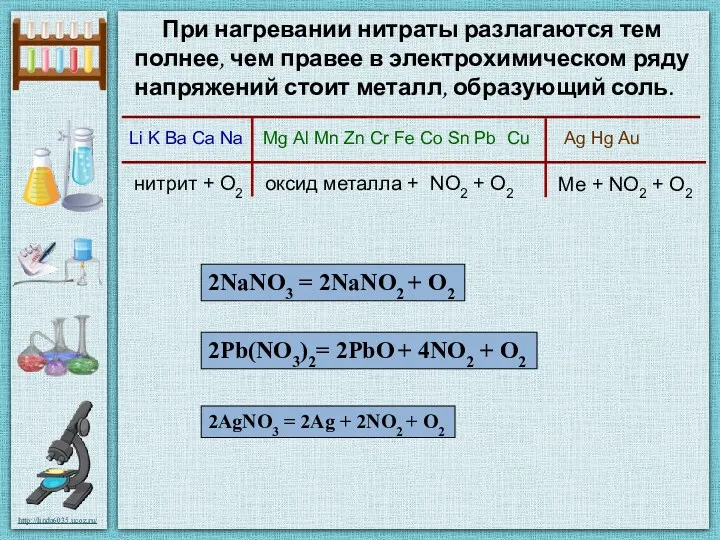
- 18. При нагревании нитраты разлагаются тем полнее, чем правее в электрохимическом ряду напряжений стоит металл, образующий соль.
- 19. Селитры используются как удобрения. KNO3 применяется для приготовления черного пороха.
- 21. Скачать презентацию














 Смог и его виды
Смог и его виды Химический эквивалент. Формульные единицы
Химический эквивалент. Формульные единицы Кристаллические решетки. Кристаллические вещества
Кристаллические решетки. Кристаллические вещества Уравнения химических реакций. Алгоритм расстановки коэффициентов
Уравнения химических реакций. Алгоритм расстановки коэффициентов Свинец
Свинец Строительное материаловедение. (Лекции 1-2)
Строительное материаловедение. (Лекции 1-2) Летучие органические соединения (ЛОС)
Летучие органические соединения (ЛОС) Общая схема радиолиза алифатических углеводородов. Радиолиз органических кислот. Радиолиз кетонов эфиров
Общая схема радиолиза алифатических углеводородов. Радиолиз органических кислот. Радиолиз кетонов эфиров Механизм реакции в органической химии
Механизм реакции в органической химии Агрегатные состояния вещества
Агрегатные состояния вещества Чистые вещества и смеси
Чистые вещества и смеси Атомы, молекулы и ионы
Атомы, молекулы и ионы №2 Практикалық жұмыс. Химиялық реакция жылдамдығына әртүрлі факторлардың әсерін зерттеу
№2 Практикалық жұмыс. Химиялық реакция жылдамдығына әртүрлі факторлардың әсерін зерттеу Обмен простых белков. Дезаминирование и трансаминирование аминокислот
Обмен простых белков. Дезаминирование и трансаминирование аминокислот Ионная химическая связь
Ионная химическая связь Виды химических реакций
Виды химических реакций Кислоты. Определение рН кислоты, щелочи, воды
Кислоты. Определение рН кислоты, щелочи, воды Кристалічні ґратки. Залежність фізичних властивостей речовини від типів кристалічних ґраток
Кристалічні ґратки. Залежність фізичних властивостей речовини від типів кристалічних ґраток Кристалы и их свойства
Кристалы и их свойства Фармацевтический анализ лекарственных средств группы алкилуреидов сульфокислот
Фармацевтический анализ лекарственных средств группы алкилуреидов сульфокислот Атомы, молекулы и ионы. Вещества молекулярного и немолекулярного строения
Атомы, молекулы и ионы. Вещества молекулярного и немолекулярного строения Поняття про багатоатомні спирти на прикладі гліцеролу, його хімічні властивості
Поняття про багатоатомні спирти на прикладі гліцеролу, його хімічні властивості Оксигеновмісні сполуки. Одноатомні та багатоатомні спирти. Феноли. Лекція №6
Оксигеновмісні сполуки. Одноатомні та багатоатомні спирти. Феноли. Лекція №6 Факторы, влияющие на скорость химической реакции
Факторы, влияющие на скорость химической реакции Водород H2
Водород H2 Окислительно-восстановительные реакции. Урок в 11 классе
Окислительно-восстановительные реакции. Урок в 11 классе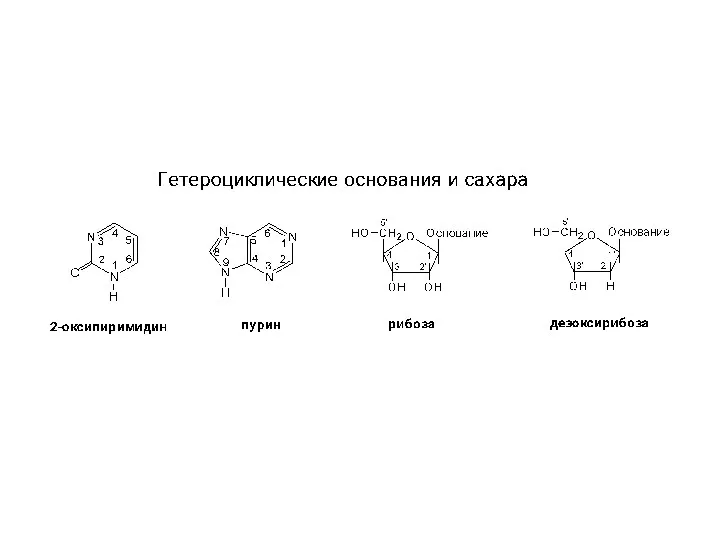 Структура гетероциклов, нуклеозидов и нуклеотидов
Структура гетероциклов, нуклеозидов и нуклеотидов Окислительно-восстановительные реакции
Окислительно-восстановительные реакции