Содержание
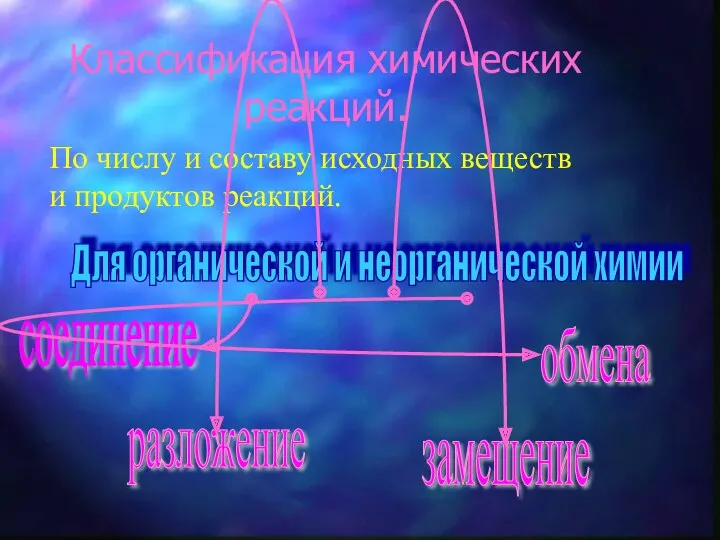
- 2. Классификация химических реакций. По числу и составу исходных веществ и продуктов реакций.
- 3. Реакции соединения
- 4. Реакции разложения Это реакции, в которых из одного сложного вещества получается несколько простых или сложных веществ:
- 5. Реакция замещения Это реакция между простым и cложным веществом, приводящая к образованию другого простого и сложного
- 6. Реакция обмена Это реакция между двумя сложными веществами, приводящая к образованию других сложных веществ. Реакция обмена
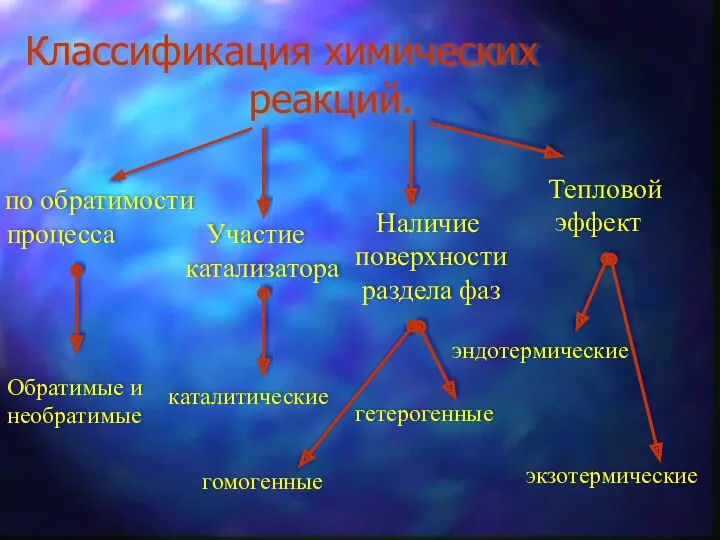
- 7. Классификация химических реакций. по обратимости процесса Обратимые и необратимые Участие катализатора каталитические Наличие поверхности раздела фаз
- 8. Обратимые и необратимые реакции. Обратимые реакции -протекают во взаимно противоположных направлениях: N2 + 3H2 ↔ 2NH3
- 9. Каталитические реакции. Каталитические реакции- протекают в присутствии катализатора: C2H4+H2O C2H5OH H2SO4
- 10. Гомогенные и гетерогенные реакции. Гомогенные- протекают между веществами находящимися в одном агрегатном состоянии: NaOH+HCl NaCl+H2Oж Гетерогенные-
- 11. Экзотермические и эндотермические реакции. Эндотермические- протекают с выделением тепла: N2+3H2 2NH3+Q Эндотермические- протекают с поглощением тепла:
- 12. Окислительно-восстановительные реакции.
- 14. Скачать презентацию









 Органолептические и визуальные методы идентификация полимера
Органолептические и визуальные методы идентификация полимера Көміртекті материалдар
Көміртекті материалдар Количественный учет влияния заместителя на реакционную способность и его использование для интерпретации механизмов реакций
Количественный учет влияния заместителя на реакционную способность и его использование для интерпретации механизмов реакций Валентность и степень окисления химического элемента
Валентность и степень окисления химического элемента Vitaminele
Vitaminele Амины. Классификация аминов. Характеристика метиламина и анилина
Амины. Классификация аминов. Характеристика метиламина и анилина Окисно-відновні реакції. Хімія. 9 клас
Окисно-відновні реакції. Хімія. 9 клас Явления, происходящие с веществами
Явления, происходящие с веществами Муравьиная кислота
Муравьиная кислота Свойства и классификация нефти
Свойства и классификация нефти Химические и физические свойства воды
Химические и физические свойства воды Полистирол өндірісі
Полистирол өндірісі Химический элемент и вещество
Химический элемент и вещество Природный газ
Природный газ Количество вещества. 8 класс
Количество вещества. 8 класс Электролитическая диссоциация
Электролитическая диссоциация Неметаллы: общая характеристика. 9 класс
Неметаллы: общая характеристика. 9 класс Нитраты в овощах и фруктах
Нитраты в овощах и фруктах Кремний. Применение кремния
Кремний. Применение кремния Химические свойства металлов
Химические свойства металлов Методы анализа. Классификация методов анализа
Методы анализа. Классификация методов анализа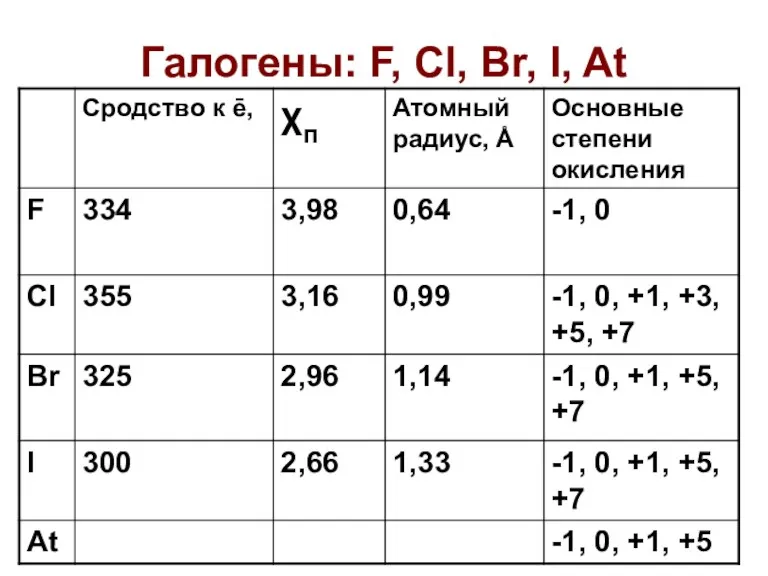 Галогены: F, Cl, Br, I, At
Галогены: F, Cl, Br, I, At Химическая посуда и лабораторное оборудование
Химическая посуда и лабораторное оборудование Скорость химических реакций. Факторы, влияющие на скорость химической реакции (лекция № 5)
Скорость химических реакций. Факторы, влияющие на скорость химической реакции (лекция № 5) Интегрированный урок по химии и немецкому языку “Anwendung Hydrolyse von Wasser”
Интегрированный урок по химии и немецкому языку “Anwendung Hydrolyse von Wasser” Гидролиз. Классификация солей
Гидролиз. Классификация солей Бумажная и тонкослойная хроматография
Бумажная и тонкослойная хроматография Химическая посуда и лабораторное оборудование
Химическая посуда и лабораторное оборудование