Содержание
- 2. Можно считать молекулы поштучно? неудобно…
- 3. 8 класс Количество вещества
- 4. Количество вещества Обозначение: ν (ню), или n Единица измерения: моль А что такое МОЛЬ?
- 5. Определение Моль – это количество вещества (порция) содержащее 6,02 10 23 частиц (атомов, молекул, ионов) .
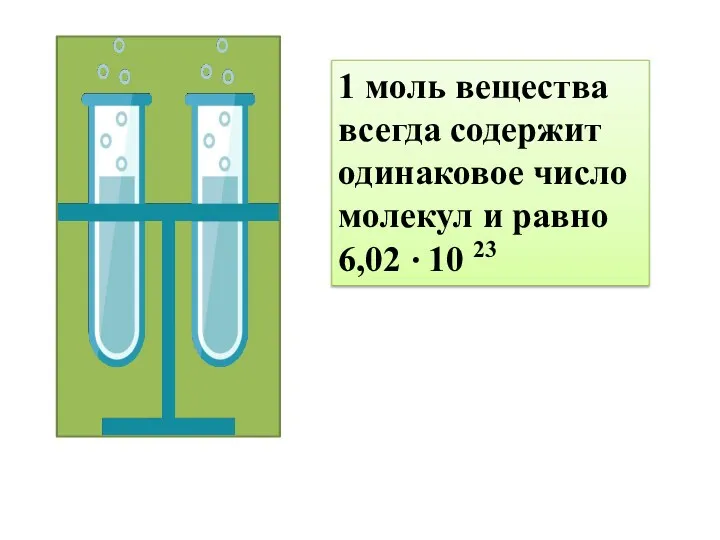
- 6. 1 моль вещества всегда содержит одинаковое число молекул и равно 6,02 10 23 .
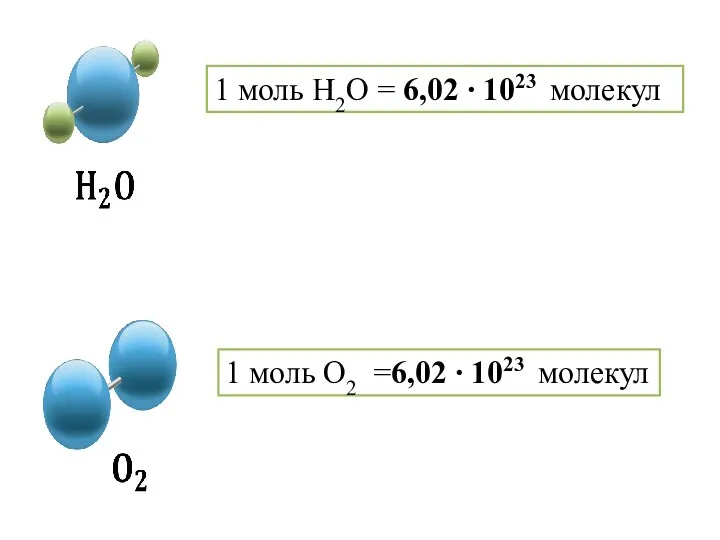
- 7. 1 моль H2O = 6,02 ∙ 1023 молекул 1 моль O2 =6,02 ∙ 1023 молекул
- 8. число Авогадро NА = 6,02 ∙ 1023 моль-1
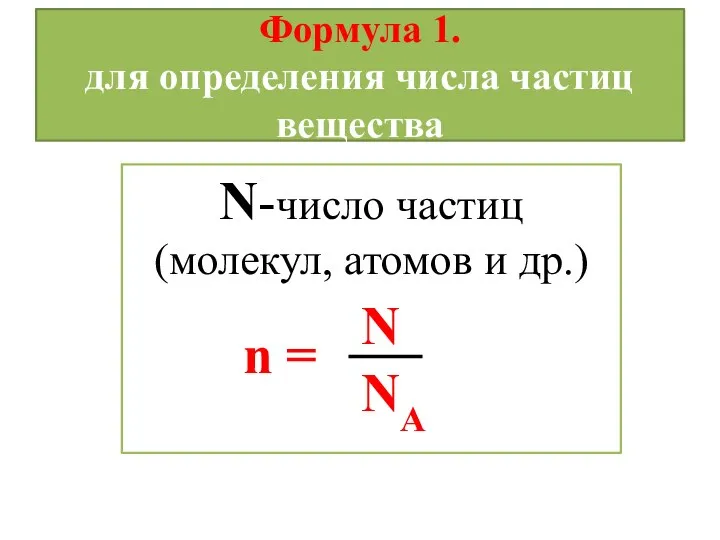
- 9. Формула 1. для определения числа частиц вещества N-число частиц (молекул, атомов и др.) NА
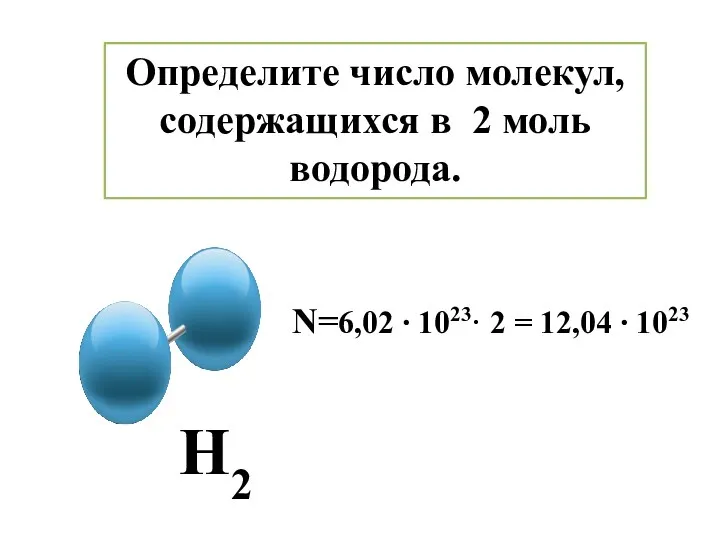
- 10. Определите число молекул, содержащихся в 2 моль водорода. Н2 N=6,02 ∙ 1023· 2 = 12,04 ∙
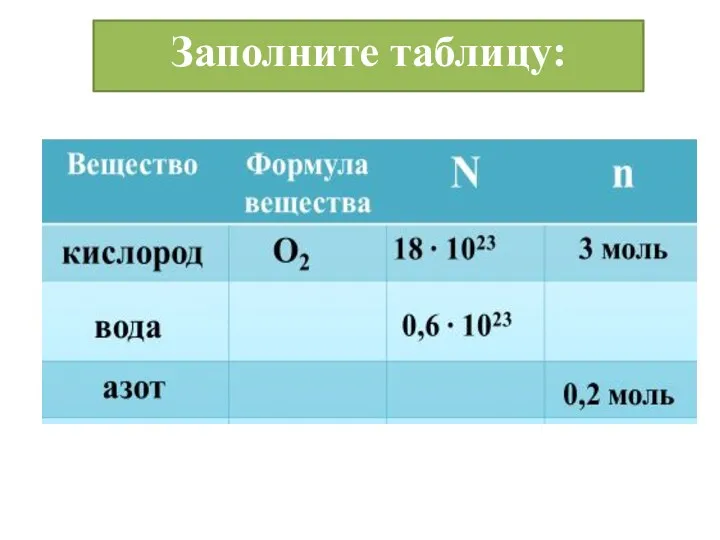
- 11. Заполните таблицу:
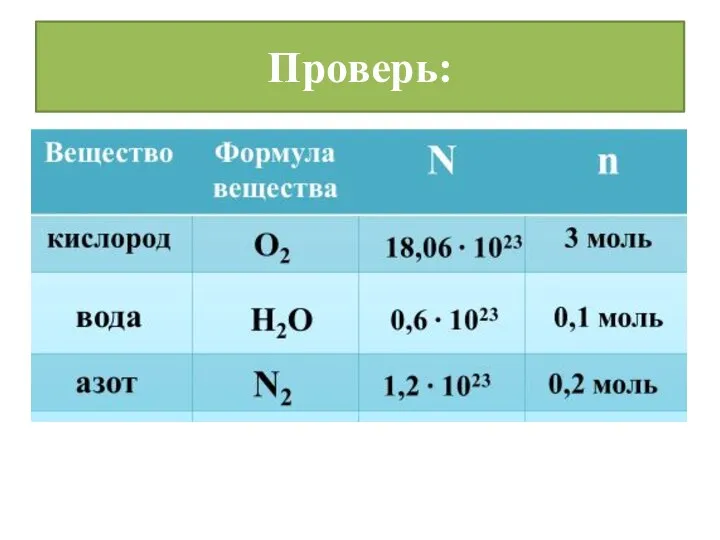
- 12. Проверь:
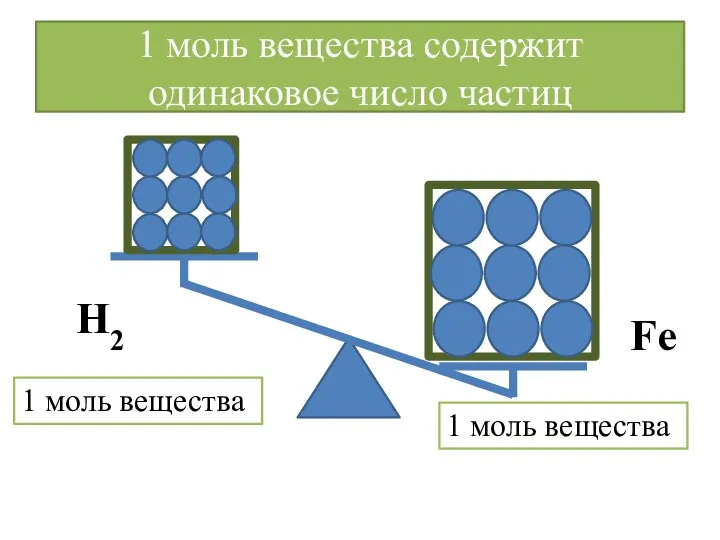
- 13. 1 моль вещества содержит одинаковое число частиц 1 моль вещества 1 моль вещества Н2 Fe
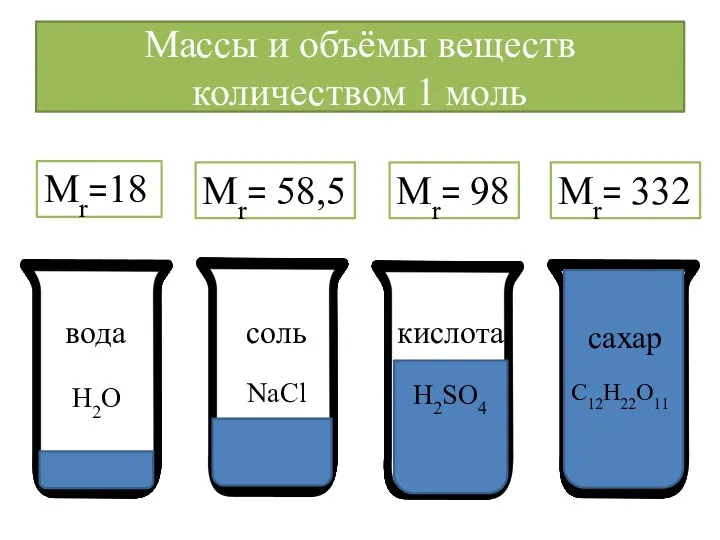
- 14. Массы и объёмы веществ количеством 1 моль вода соль кислота сахар Mr=18 Mr= 58,5 Mr= 98
- 15. Как отмерить 1 моль вещества? 1 г
- 16. Молярная масса вещества Это масса 1 моль вещества. Обозначается - М ед.измерения А сколько весит 1
- 17. Молярная масса вещества численно совпадает с его относительной молекулярной массой. M(Fe2O3) - ? Молярная масса Mr
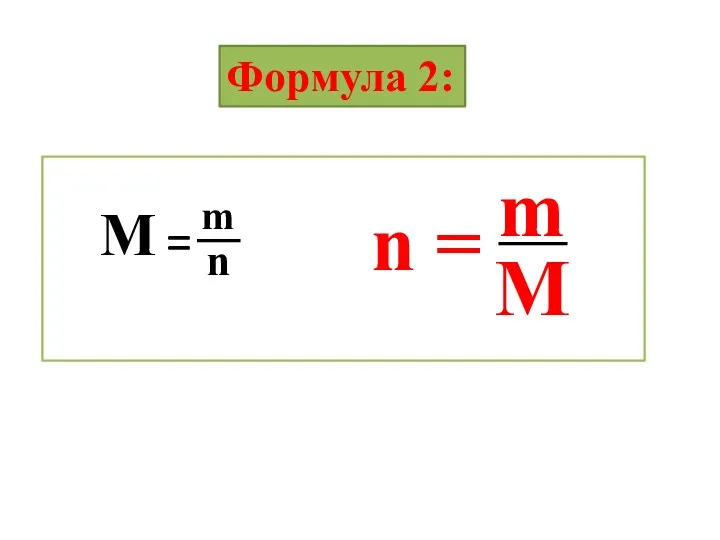
- 18. Формула 2:
- 19. Какую массу имеют 5 моль углекислого газа? Дано: n(CO2) = 5 моль m(CO2) - ? Решение:
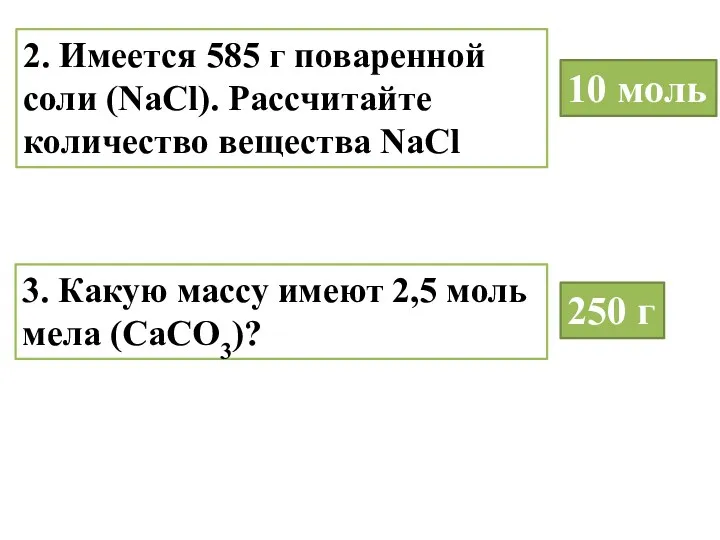
- 20. 2. Имеется 585 г поваренной соли (NaCl). Расcчитайте количество вещества NaCl 10 моль 3. Какую массу
- 21. А как же газы? С ними так же?
- 22. Масса 1 моль вещества называется молярной, а как по-вашему называется объем 1 моль газообразного вещества? Объем
- 23. Нормальные условия (н.у.) Т = 0 0С Р = 760 мм. рт. ст. или 1 атм
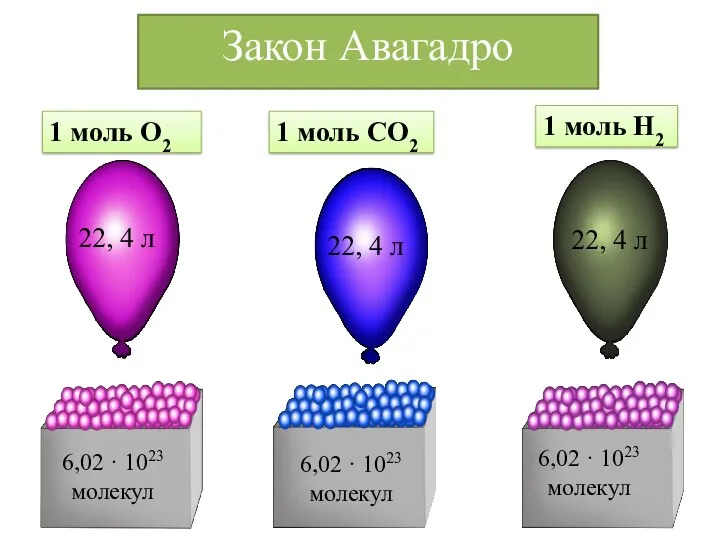
- 24. 1 моль О2 1 моль СО2 1 моль Н2 22, 4 л 6,02 · 1023 молекул
- 25. Объем, который занимает один моль любого газа называется Молярным объемом Молярный объём любого газа при н.у.
- 26. Задача №4 Какой объем занимает 0,2 моль N2 при н.у.? Дано: н.у. Vm = 22, 4
- 27. Относительная плотность Отношение масс одинаковых объёмов различных газов при одинаковых условиях равно отношению их молярных масс
- 28. Относительная плотность (D) Она показывает, во сколько раз один газ тяжелее или легче другого
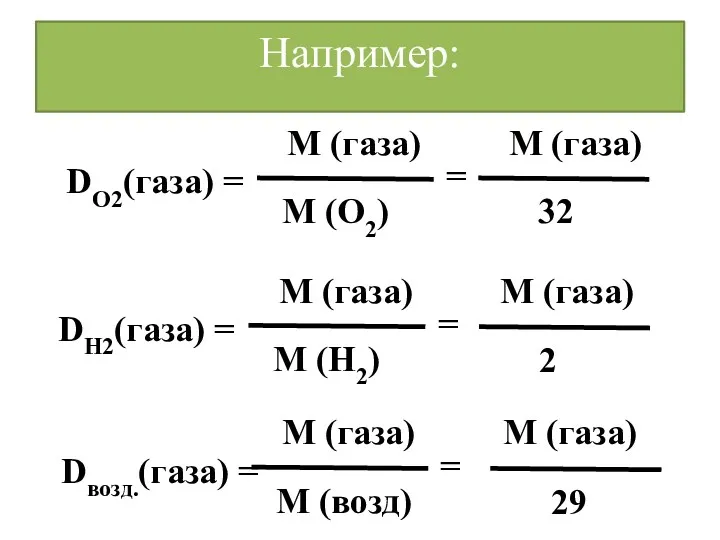
- 29. Например:
- 30. Задача 5 Найдите массу 1 л аммиака NH3 при н.у. Ответ: V(NH3) = 1л m(NH3) -?
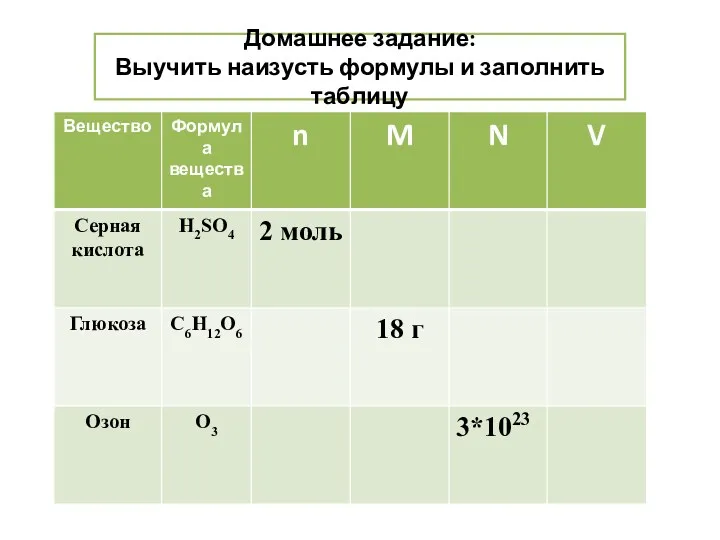
- 31. Домашнее задание: Выучить наизусть формулы и заполнить таблицу
- 32. Домашнее задание: §18, 19 читать, таблица в тетради
- 34. Скачать презентацию

















 Бензин. Производство бензина
Бензин. Производство бензина Types of chemical reactions
Types of chemical reactions соединения VI группы продвинутая версия
соединения VI группы продвинутая версия Азотсодержащие органические соединения
Азотсодержащие органические соединения Органическая химия. Лекция 13
Органическая химия. Лекция 13 Химическое равновесие. Смещение химического равновесия
Химическое равновесие. Смещение химического равновесия Современные положения теории А.М. Бутлерова
Современные положения теории А.М. Бутлерова Химические формулы. Относительная молекулярная масса
Химические формулы. Относительная молекулярная масса Изотопный обмен
Изотопный обмен Растворы. Вычисление массовой доли растворенного вещества в растворе. Урок для 8-го класса
Растворы. Вычисление массовой доли растворенного вещества в растворе. Урок для 8-го класса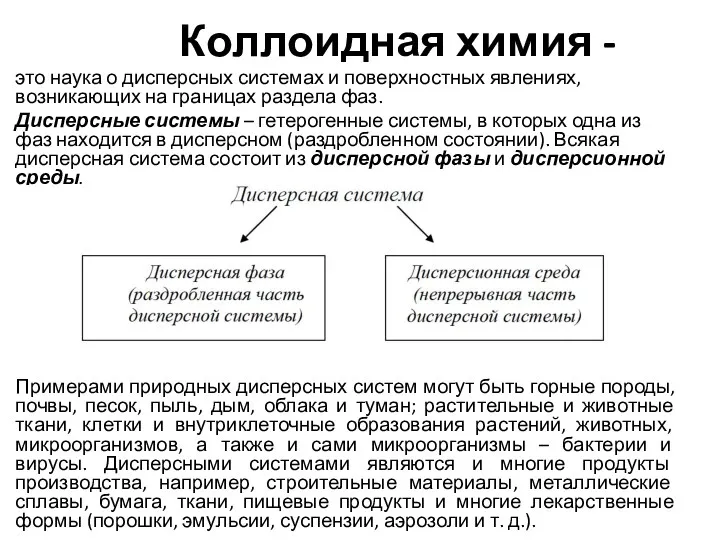 Коллоидная химия
Коллоидная химия Алкены. Этиленовые углеводороды, олефины
Алкены. Этиленовые углеводороды, олефины Nucleic acids
Nucleic acids Общая и медицинская химия
Общая и медицинская химия Создание косметических средств
Создание косметических средств Лекарственные средства из группы карбоновых кислот и их производных калия ацетат, кальция лактат, натрия цитрат
Лекарственные средства из группы карбоновых кислот и их производных калия ацетат, кальция лактат, натрия цитрат Алюминий и бор
Алюминий и бор Получение галогенов. Биологическое значение и применение галогенов и их соединений
Получение галогенов. Биологическое значение и применение галогенов и их соединений Титриметрический анализ. (Лекция 22)
Титриметрический анализ. (Лекция 22) проект по биологииНаучно-исследовательская работа
проект по биологииНаучно-исследовательская работа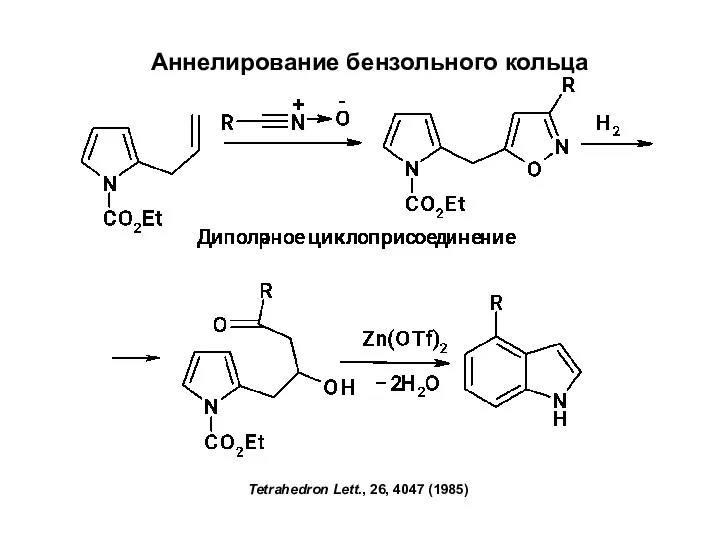 Аннелирование бензольного кольца
Аннелирование бензольного кольца Строение атома. Теории строения атома
Строение атома. Теории строения атома Анализ начальных участков изотерм адсорбции
Анализ начальных участков изотерм адсорбции Многоатомные спирты
Многоатомные спирты Щелочноземельные металлы. Химические свойства
Щелочноземельные металлы. Химические свойства Азот и его свойства
Азот и его свойства Нефть. Способы её переработки. Фракции нефти
Нефть. Способы её переработки. Фракции нефти Процесс электролиза
Процесс электролиза