Содержание
- 2. История открытия азота: В 1772 г. Англичанин Д. Резерфорд установил, что воздух, оставшийся под колоколом, где
- 3. Нахождение в природе: В воздухе - 78,09% (по объему) В земной коре – 0,01% ( по
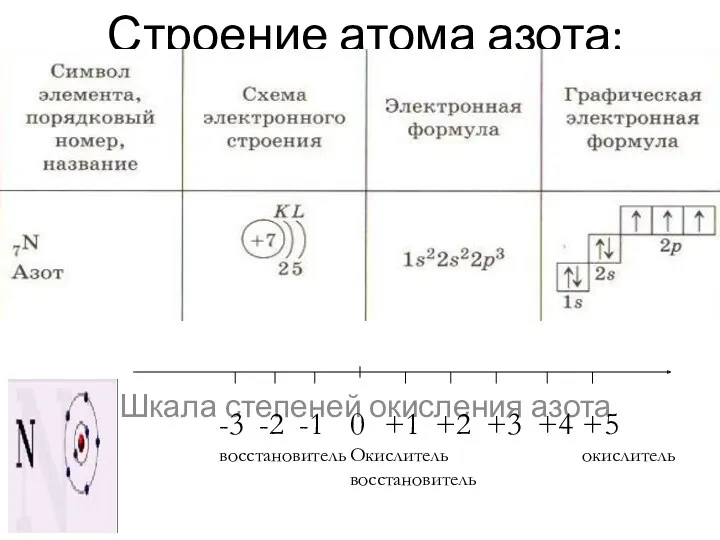
- 4. Строение атома азота: Шкала степеней окисления азота -1 0 Окислитель восстановитель +1 -2 -3 восстановитель +2
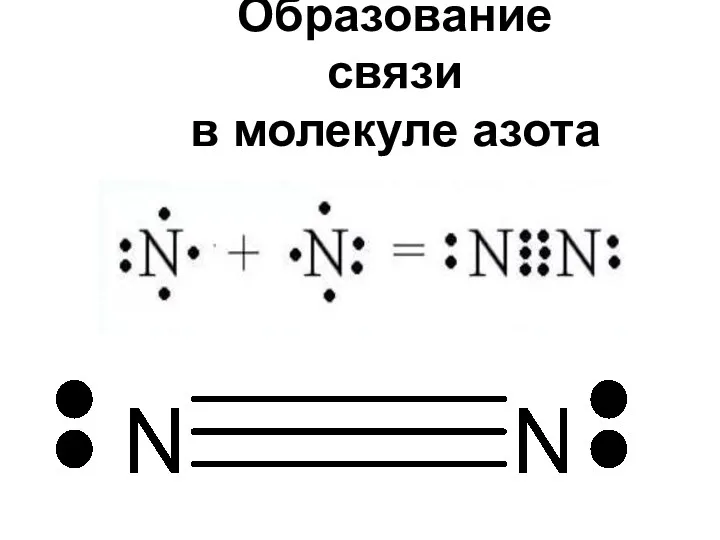
- 5. Образование связи в молекуле азота
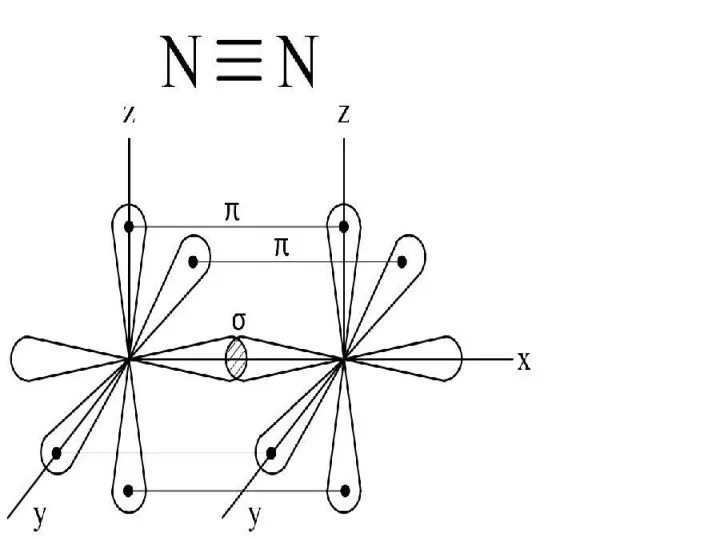
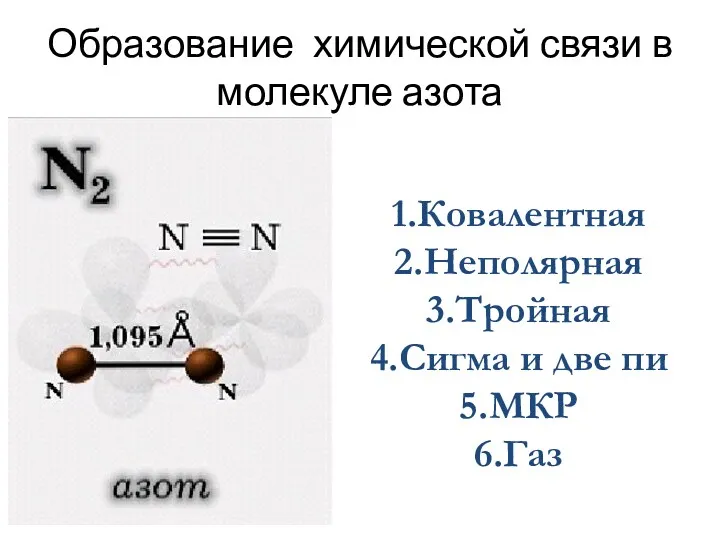
- 7. Образование химической связи в молекуле азота 1.Ковалентная 2.Неполярная 3.Тройная 4.Сигма и две пи 5.МКР 6.Газ
- 8. Каким образом можно объяснить химическую инертность молекулы азота? 2 атома азота соединены в молекулу тройной ковалентной
- 9. Физические свойства Т кип (N2)= - 196 °C ГАЗ БЕЗ ЦВЕТА БЕЗ ЗАПАХА малорастворим в воде
- 10. Химические свойства Окислитель N2+Na= N2+Ca= N2+H2= СОЭ АЗОТА с металлами и водородом -3 Восстановитель N2+O2= NO!!!
- 11. Получение азота:
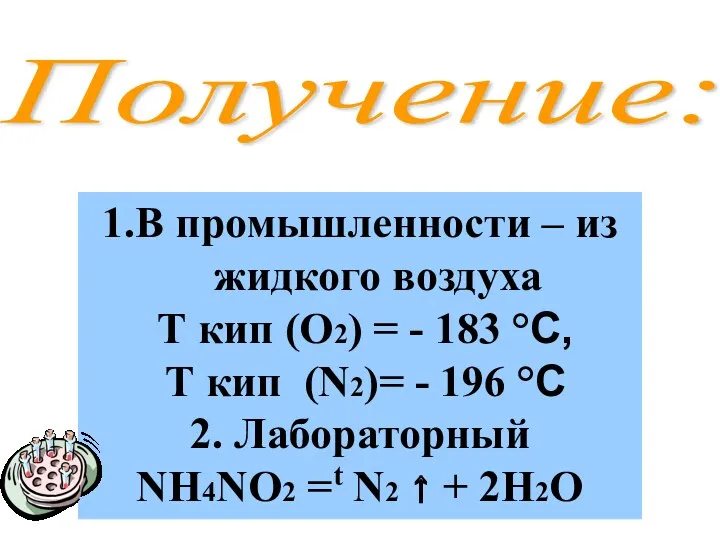
- 12. Получение: 1.В промышленности – из жидкого воздуха Т кип (О2) = - 183 °C, Т кип
- 14. Скачать презентацию






 Александр Евгеньевич Ферсман
Александр Евгеньевич Ферсман Кислород и озон
Кислород и озон Алкандар. Метан және оның құрылысы
Алкандар. Метан және оның құрылысы Соли аммония
Соли аммония Химические свойства алканов
Химические свойства алканов Свободное окисление и токсические формы кислорода
Свободное окисление и токсические формы кислорода Формирование ключевых и предметных компетенций учащихся при изучении темы “Металлы”
Формирование ключевых и предметных компетенций учащихся при изучении темы “Металлы” Углерод. Оксиды углерода
Углерод. Оксиды углерода Применение соляной кислоты и её солей
Применение соляной кислоты и её солей Антибиотики как ЛС
Антибиотики как ЛС Соли. CaSO4 - Сульфат кальция
Соли. CaSO4 - Сульфат кальция Class micro and macro elements
Class micro and macro elements Строение атома. Периодический закон Менделеева
Строение атома. Периодический закон Менделеева Простые вещества – неметаллы
Простые вещества – неметаллы Вычисление массовой доли растворенного вещества. 8 класс
Вычисление массовой доли растворенного вещества. 8 класс Цинк в функциональных пищевых и кормовых продуктах
Цинк в функциональных пищевых и кормовых продуктах Ювелирное дело. Империя самоцветов
Ювелирное дело. Империя самоцветов Ферменты в биотехнологии
Ферменты в биотехнологии Строение вещества и агрегатные состояния вещества
Строение вещества и агрегатные состояния вещества Мило та миловаріння
Мило та миловаріння Почему мыло пенится
Почему мыло пенится Основные классы неорганических соединений
Основные классы неорганических соединений Тренувальні вправи. Задачі
Тренувальні вправи. Задачі Період як особлива синтаксична конструкція
Період як особлива синтаксична конструкція Кислородсодержащие органические соединения. Лабораторная работа
Кислородсодержащие органические соединения. Лабораторная работа Химия элементов. Общая характеристика элементов
Химия элементов. Общая характеристика элементов Вклад М.В. Ломоносова в развитие химии
Вклад М.В. Ломоносова в развитие химии Узагальнення знань з теми Вуглеводні
Узагальнення знань з теми Вуглеводні