Содержание
- 2. ПЛАН Сущность и задачи титриметрии. Классификация методов титриметрического анализа. 3. Первичные, вторичные стандарты. Способы приготовления растворов,
- 3. 1. Сущность и задачи титриметрии. Титриметрический анализ основан на измерении количества реагента, израсходованного на реакцию с
- 4. Если определяемый компонент Х взаимодействует с реагентом R в стехиометрических отношениях, то независимо от типа протекающей
- 5. Стандартный раствор постепенно прибавляют к раствору определяемого вещества до тех пор, пока не наступит точка эквивалентности
- 6. 2. Классификация методов титриметрического анализа. Методы титриметрического анализа можно классифицировать по характеру химической реакции, лежащей в
- 7. 1). Методы нейтрализации, или кислотно-основного титрования основаны на реакциях нейтрализации, т. е. на взаимодействии кислот и
- 8. 2). Методы окисления – восстановления (редоксметрия или оксидиметрия) основаны на применении ОВ реакций, в качестве титрантов
- 9. 3). Методы комплексообразования, или комплексометрия (меркуриметрия, фторометрия и др.), основаны на применении реакций, при которых образуются
- 10. 4). Методы осаждения основаны на титровании веществ, образующих в определенной среде нерастворимые соединения, например соли бария,
- 11. Реакции, лежащие в основе титриметрических методов, должны удовлетворять ряду требований: 1. Взаимодействие титранта с определяемым веществом
- 12. 3. Первичные, вторичные стандарты. В титриметрии используют стандартные (приготовленные) и стандартизированные (установленные) растворы титрантов. Приготовленные растворы
- 13. Первичные стандарты. Химические соединения высокой степени чистоты, которые используются в качестве эталона, называются первичными стандартами. Правильность
- 14. В некоторых случаях вместо первичных стандартов приходится использовать менее чистые вещества – вторичные стандарты. Степень чистоты
- 15. Раствор титранта (раствор реагента, который используют для титрования раствора определяемого вещества) готовят используя следующие методы: -
- 16. Метод фиксаналов. Для приготовления раствора титранта используют фиксаналы. Метод отдельных навесок. На аналитических весах берут 2-3
- 17. Лишь немногие из применяемых в титриметрии реагентов полностью удовлетворяют выше приведенным требованиям. Поэтому, часто используют стандартизированные
- 18. 4. Способы (приемы) проведения титриметрического анализа. прямое титрование; обратное титрование (или титрование по остатку); титрование по
- 19. 1. Взаимодействие титруемого вещества с реагентом в условиях проведения анализа должно быть специфическим, т.е. с применяемым
- 20. Расчеты результатов прямого титрования. Если известна молярная концентрация щелочи c и объем раствора V израсходованный на
- 21. Масса кислоты в анализируемом растворе m(HCl) рассчитывается по соотношению: c(NaOH) ∙ V(NaOH) m(HCl) = n(HCl) ∙M(HCl)
- 22. Широко распространен способ расчета результатов с помощью условного титра рабочего раствора или титра по определяемому веществу.
- 23. Обратное титрование Обратное титрование применяют, когда мала скорость прямой реакции, отсутствует подходящий индикатор или при прямом
- 24. Расчеты результатов в методе обратного титрования. Рассмотрим расчет результата на примере обратного титрования хлорида. В этом
- 25. Количество вещества эквивалента хлорида в анализируемом растворе находим из уравнения (3) n(AgCl) = n(AgNO3) - n(AgSCN)
- 27. Скачать презентацию
























 Химический элемент: йод
Химический элемент: йод Электролитическая диссоциация
Электролитическая диссоциация Галогены. Хлор
Галогены. Хлор Спирты и фенолы
Спирты и фенолы Азот
Азот Растворы. Часть 2
Растворы. Часть 2 Поливинилхлорид (ПВХ, PVC)
Поливинилхлорид (ПВХ, PVC) Металлы и сплавы с высокой удельной прочностью
Металлы и сплавы с высокой удельной прочностью Главная подгруппа IV группы. Общая характеристика элементов
Главная подгруппа IV группы. Общая характеристика элементов Арены. Бензол
Арены. Бензол Карбон қышқылдары, жіктелуі, сипаттамалары, таралуы
Карбон қышқылдары, жіктелуі, сипаттамалары, таралуы Совйства спиртов. 10 класс
Совйства спиртов. 10 класс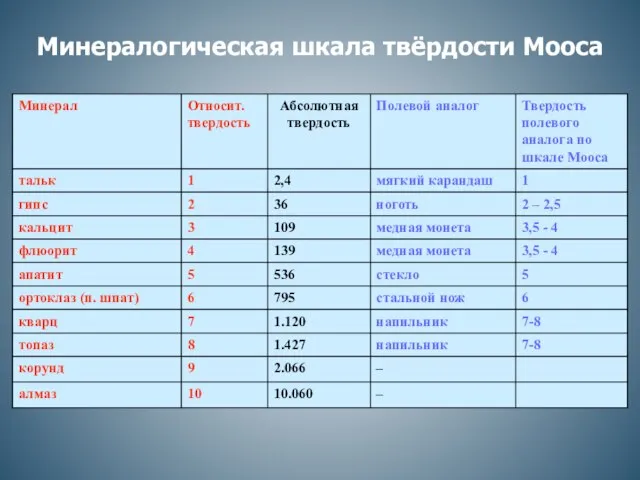 Минералогическая шкала твёрдости Мооса
Минералогическая шкала твёрдости Мооса Получение галогенов. Биологическое значение и применение галогенов и их соединений
Получение галогенов. Биологическое значение и применение галогенов и их соединений Азот, фосфор и их соединения
Азот, фосфор и их соединения Тепловой эффект химической реакции
Тепловой эффект химической реакции Окислительно-восстановительные реакции
Окислительно-восстановительные реакции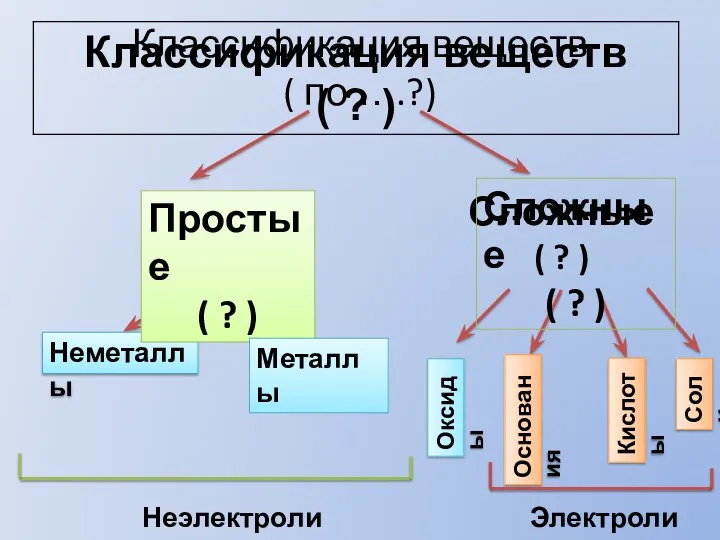 Классификация веществ
Классификация веществ Тефлон. Что такое тефлон?
Тефлон. Что такое тефлон? Нефтепродукты в косметическом производстве. Биологически активные вещества
Нефтепродукты в косметическом производстве. Биологически активные вещества Строение и физические свойства металлов
Строение и физические свойства металлов Неон. Физические свойства
Неон. Физические свойства Анализ проб воды
Анализ проб воды Наглядное пособие Динамические модели. Химическое равновесие в растворах
Наглядное пособие Динамические модели. Химическое равновесие в растворах Silicon. Silicate minerals. Weathering
Silicon. Silicate minerals. Weathering Химическая кинетика. Часть II. Скорость химической реакции - развитие реакции во времени
Химическая кинетика. Часть II. Скорость химической реакции - развитие реакции во времени Углерод
Углерод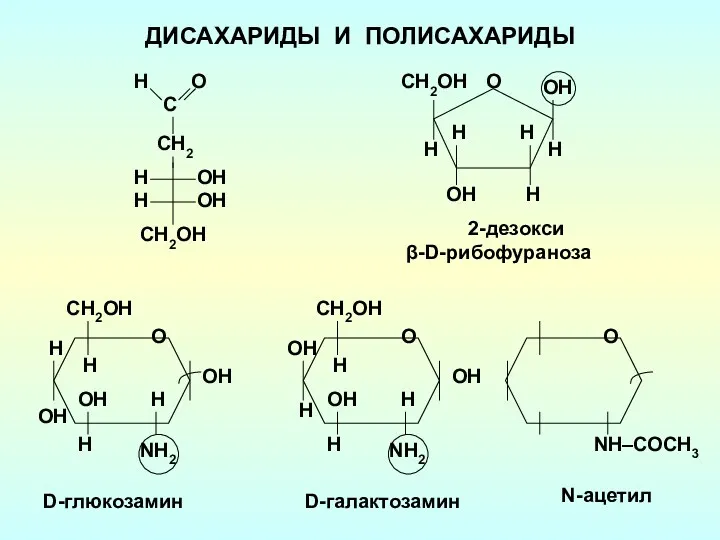 Дисахариды и полисахариды
Дисахариды и полисахариды