Содержание
- 2. Строение и свойства 1. Кислотные свойства (значительный δ+ на Н) 2. АN не характерно (δ+ на
- 3. Названия НСООН муравьиная СН3СООН уксусная С2Н5СООН пропионовая С3Н7СООН масляная С5Н11СООН валериановая С6Н13СООН капроновая С15Н31СООН пальмитиновая С17Н35СООН
- 4. Кислотные свойства HCOOH > CH3COOH > (CH3)2CH-COOH > (CH3)3C-COOH 1,8⋅10-4 1,8⋅10-5 1,4⋅10-5 Как зависят от радикала?
- 5. Проявление кислотных свойств + активные металлы 2RCOOH + Mg → (RCOO)2Mg + H2 + основные оксиды
- 6. Образование функциональных производных (SN) Галогенангидриды (алканоилгалогениды) RCOOH + PCl5 = RCOCl + POCl3 + HCl (PCl3,
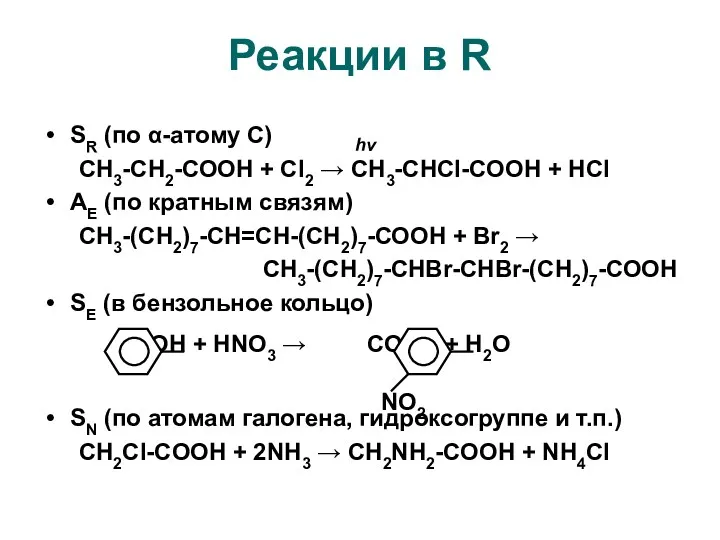
- 7. Реакции в R SR (по α-атому С) СН3-СН2-СООН + Cl2 → CH3-CHCl-COOH + HCl AE (по
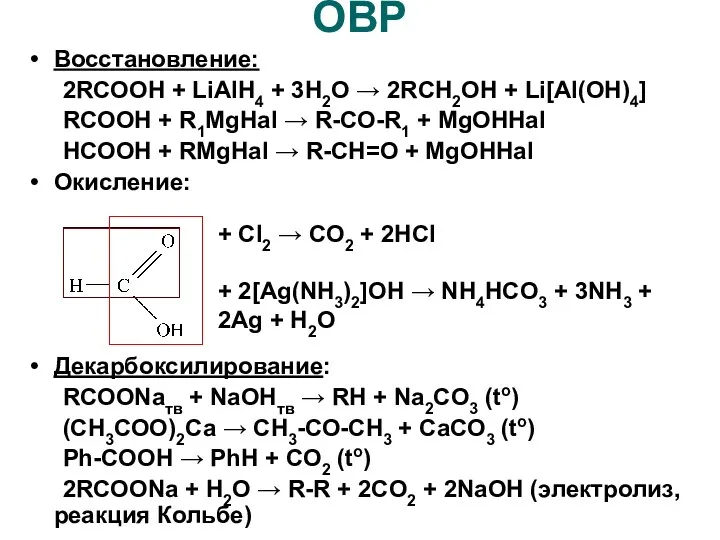
- 8. ОВР Восстановление: 2RCOOH + LiAlH4 + 3H2O → 2RCH2OH + Li[Al(OH)4] RCOOH + R1MgHal → R-CO-R1
- 9. Получение Окисление альдегидов и спиртов R-CHO + 2[Ag(NH3)2]OH → R-COONH4 + 2Ag↓ + 3NH3 + H2O
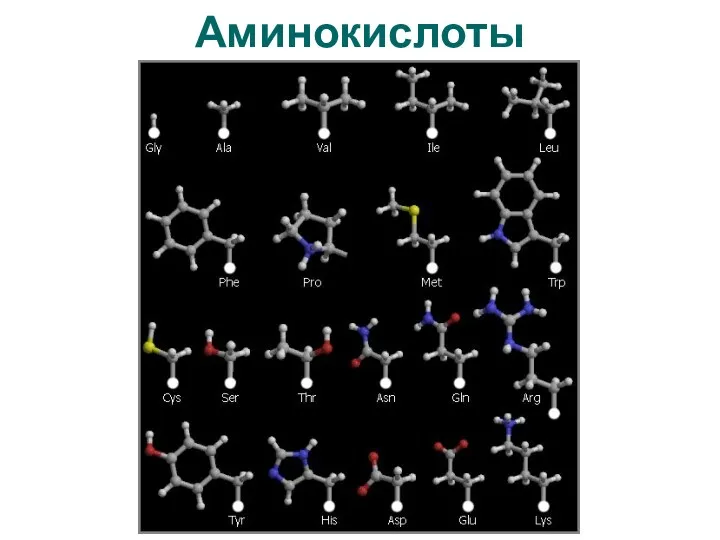
- 10. Аминокислоты
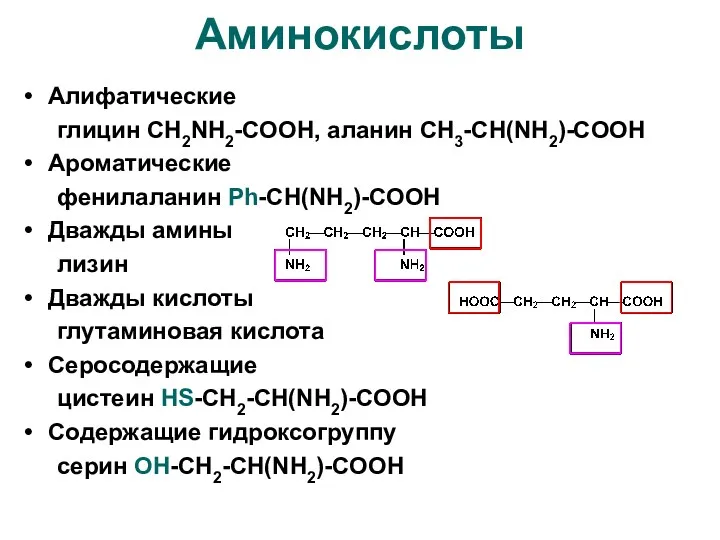
- 11. Аминокислоты Алифатические глицин CH2NH2-COOH, аланин CH3-CH(NH2)-COOH Ароматические фенилаланин Ph-CH(NH2)-COOH Дважды амины лизин Дважды кислоты глутаминовая кислота
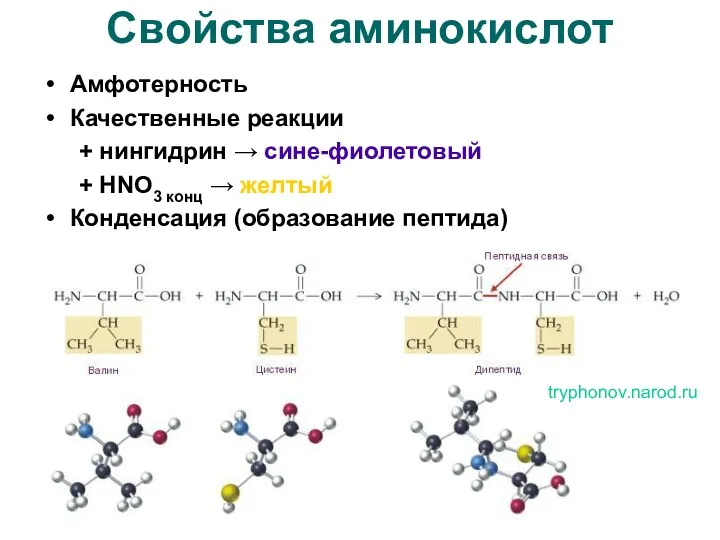
- 12. Свойства аминокислот Амфотерность Качественные реакции + нингидрин → сине-фиолетовый + HNO3 конц → желтый Конденсация (образование
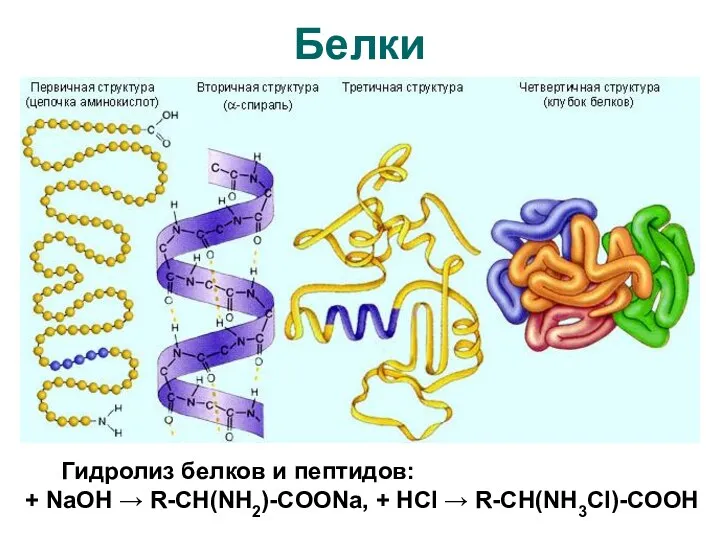
- 13. Белки Гидролиз белков и пептидов: + NaOH → R-CH(NH2)-COONa, + HCl → R-CH(NH3Cl)-COOH
- 14. Галогенангидриды Гидролиз RCOCl + H2O = RCOOH + HCl Аммонолиз RCOCl + 2NH3 = RCONH2 +
- 15. Сложные эфиры Гидролиз RCOOR + H2O ⇔ RCOOH + ROH (в прис. Н+) RCOOR + NaOH
- 16. Ангидриды Гидролиз (RCO)2О + H2O = 2RCOOH Аммонолиз (RCO)2О + 2NH3 = RCONH2 + RCOONH4 Алкоголиз
- 17. Амиды RCONH2 первичный амид СН3-СОNH2 этанамид RCONHR вторичный амид СН3-СОNHСН3 N-метилэтанамид RCONR2 третичный амид СН3-СОN(СН3)2 N,N-диметилэтанамид
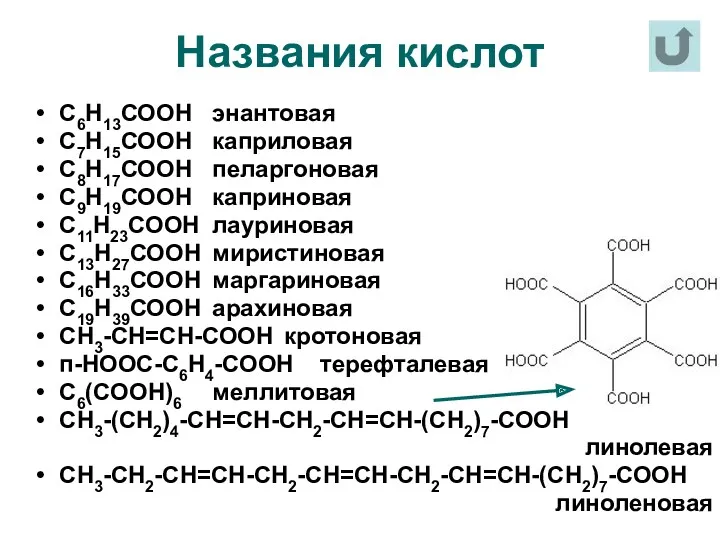
- 18. Названия кислот С6Н13СООН энантовая С7Н15СООН каприловая С8Н17СООН пеларгоновая С9Н19СООН каприновая С11Н23СООН лауриновая С13Н27СООН миристиновая С16Н33СООН маргариновая
- 20. Скачать презентацию





![Получение Окисление альдегидов и спиртов R-CHO + 2[Ag(NH3)2]OH → R-COONH4](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/399768/slide-8.jpg)




 Углерод. Элемент IV группы
Углерод. Элемент IV группы Электронный помощник по химии 8 класс
Электронный помощник по химии 8 класс Химия переходных элементов IV – V группы
Химия переходных элементов IV – V группы Общая характеристика неметаллов
Общая характеристика неметаллов Ископаемые углеводороды
Ископаемые углеводороды Закон сохранения массы веществ. Химические уравнения
Закон сохранения массы веществ. Химические уравнения Гидролиз солей
Гидролиз солей Неорганическая химия
Неорганическая химия Химический анализ веществ
Химический анализ веществ Альдегиды и кетоны
Альдегиды и кетоны Углеводы. 10 класс
Углеводы. 10 класс Углеводороды. Применение природных источников углеводородов и продуктов их переработки
Углеводороды. Применение природных источников углеводородов и продуктов их переработки Состав, строение и свойства натурального каучука
Состав, строение и свойства натурального каучука Титан және титан қорытпалары. Деформацияланған және кұйма титан қорытпалары
Титан және титан қорытпалары. Деформацияланған және кұйма титан қорытпалары Химическая технология природных энергоносителей и углеродных материалов
Химическая технология природных энергоносителей и углеродных материалов Кислые породы умеренно-щелочного ряда
Кислые породы умеренно-щелочного ряда Классификация химических реакций
Классификация химических реакций Характеристика химического элемента по кислотно-основным свойствам образуемых им соединений. Амфотерные оксиды и гидроксиды
Характеристика химического элемента по кислотно-основным свойствам образуемых им соединений. Амфотерные оксиды и гидроксиды Первые шаги в минералогию: от новичка до знатока
Первые шаги в минералогию: от новичка до знатока Инертные газы
Инертные газы Металлогеническая периодизация истории Земли. Геолого-металлогенические ранги
Металлогеническая периодизация истории Земли. Геолого-металлогенические ранги Диссоциация кислот, оснований, солей
Диссоциация кислот, оснований, солей 20231110_zakon_avogadro
20231110_zakon_avogadro Спирттер мен фенолдар
Спирттер мен фенолдар Аминокислоты и белки
Аминокислоты и белки Карбон
Карбон Класифікація дисперсних систем харчових продуктів. Характеристика колоїдних систем
Класифікація дисперсних систем харчових продуктів. Характеристика колоїдних систем Азотная кислота
Азотная кислота