Содержание
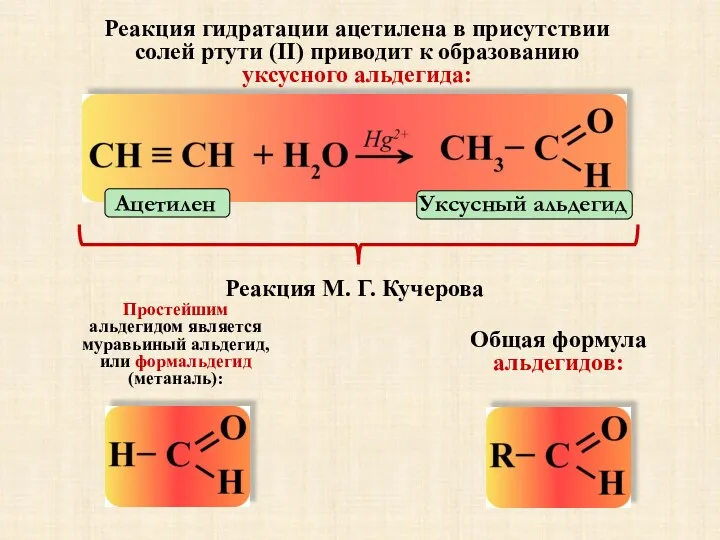
- 2. Уксусный альдегид Ацетилен Реакция М. Г. Кучерова Реакция гидратации ацетилена в присутствии солей ртути (II) приводит
- 3. Альдегиды - это карбонильные производные углеводородов, в молекулах которых присутствует альдегидная группа: Альдегиды – это органические
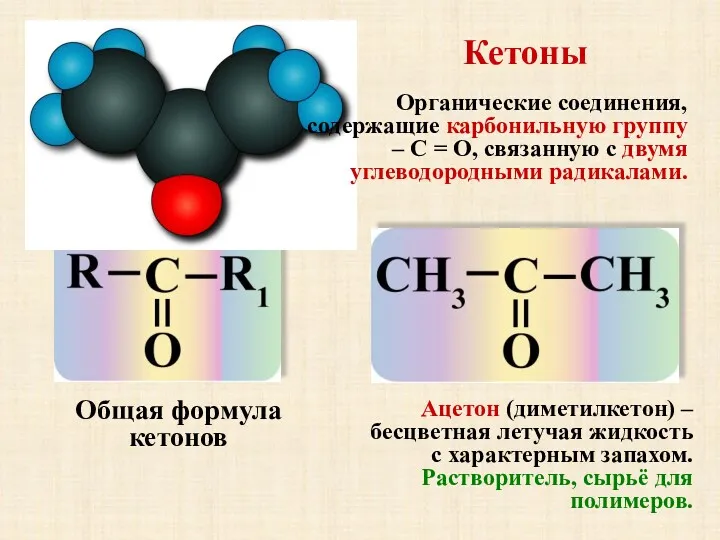
- 4. Кетоны Общая формула кетонов Ацетон (диметилкетон) – бесцветная летучая жидкость с характерным запахом. Растворитель, сырьё для
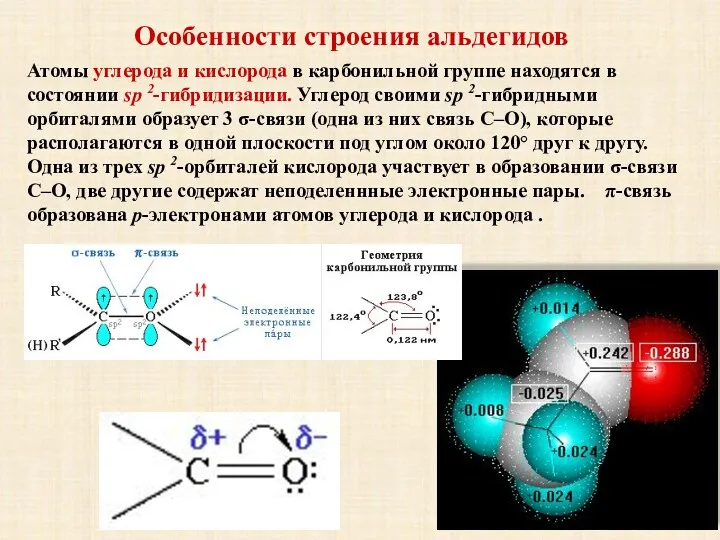
- 5. Особенности строения альдегидов Атомы углерода и кислорода в карбонильной группе находятся в состоянии sp 2-гибридизации. Углерод
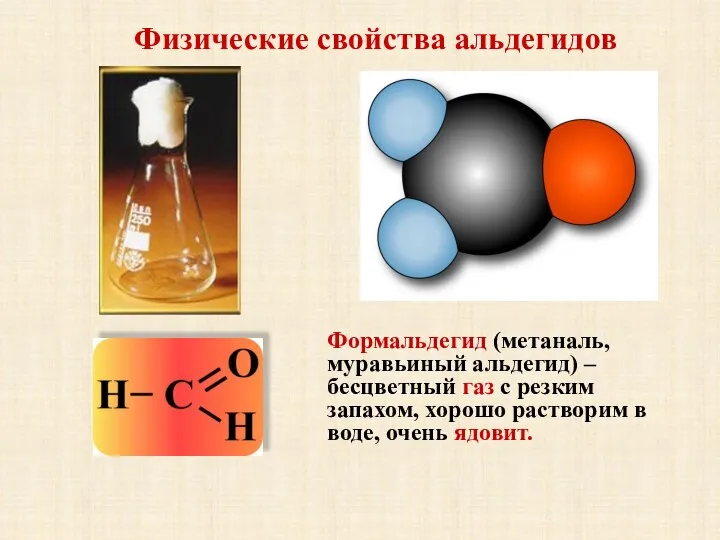
- 6. Физические свойства альдегидов Формальдегид (метаналь, муравьиный альдегид) – бесцветный газ с резким запахом, хорошо растворим в
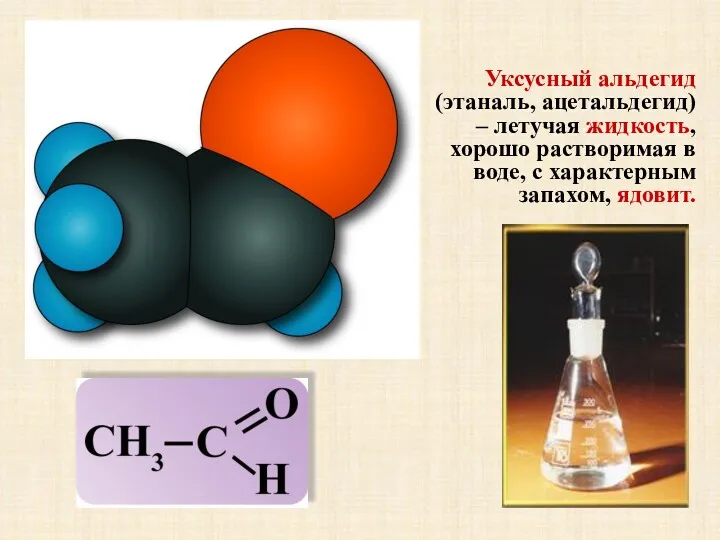
- 7. Уксусный альдегид (этаналь, ацетальдегид) – летучая жидкость, хорошо растворимая в воде, с характерным запахом, ядовит.
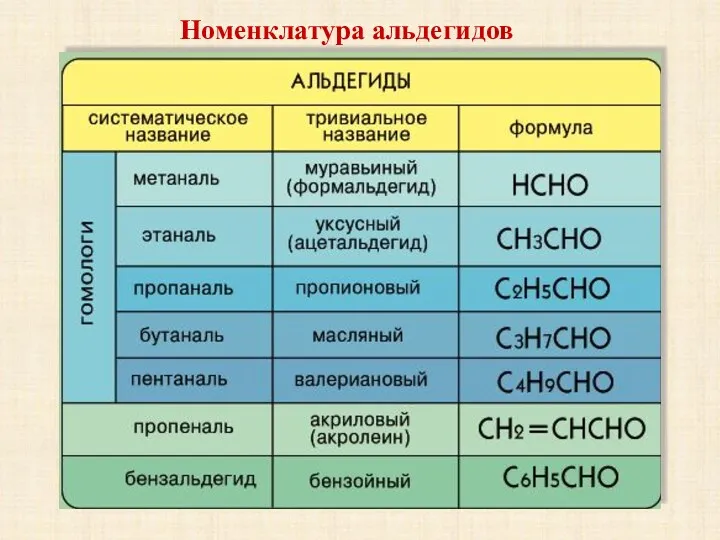
- 8. Номенклатура альдегидов
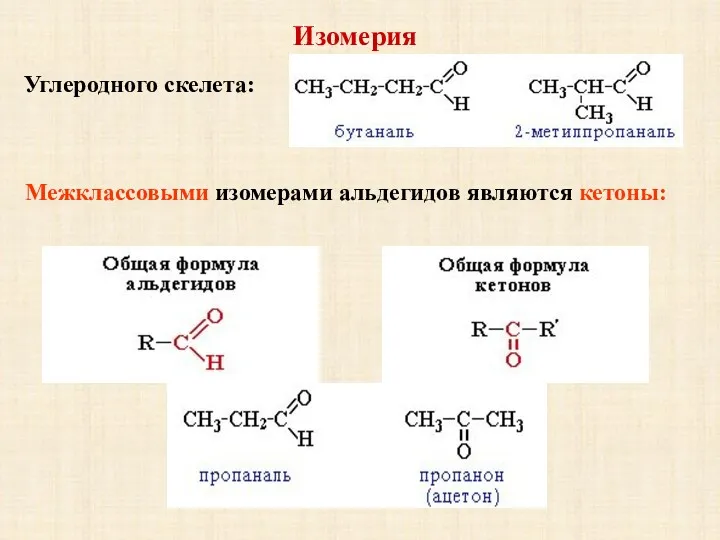
- 9. Изомерия Межклассовыми изомерами альдегидов являются кетоны: Углеродного скелета:
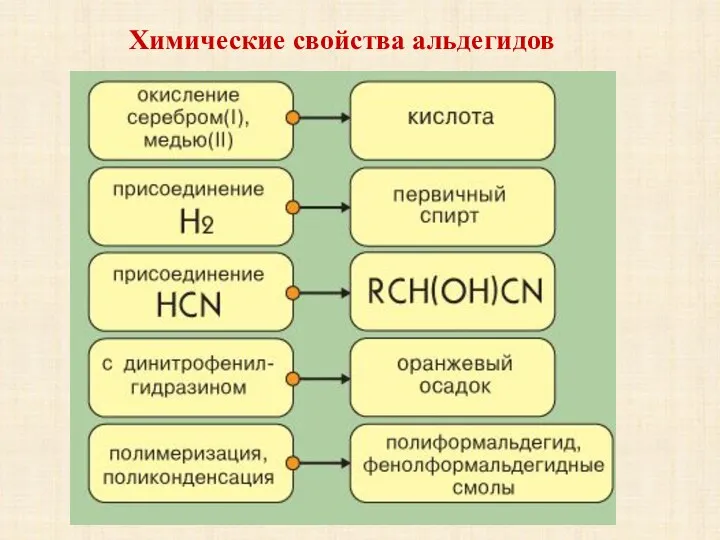
- 10. Химические свойства альдегидов
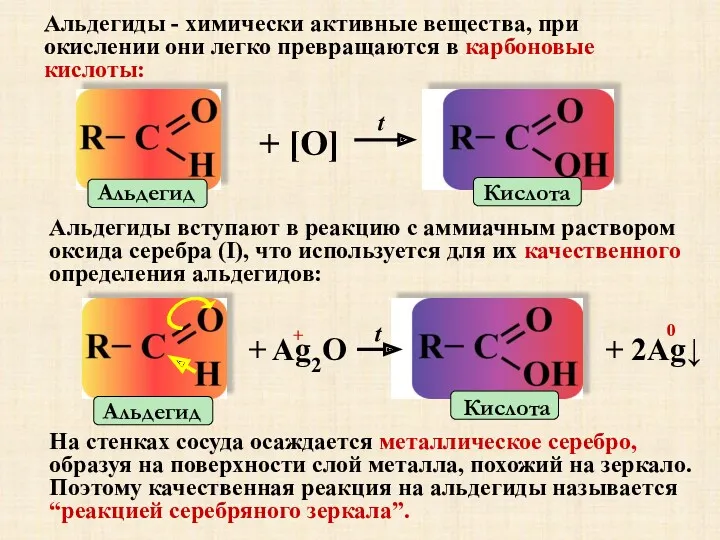
- 11. Альдегиды - химически активные вещества, при окислении они легко превращаются в карбоновые кислоты: Альдегиды вступают в
- 12. Реакция «серебряного зеркала»
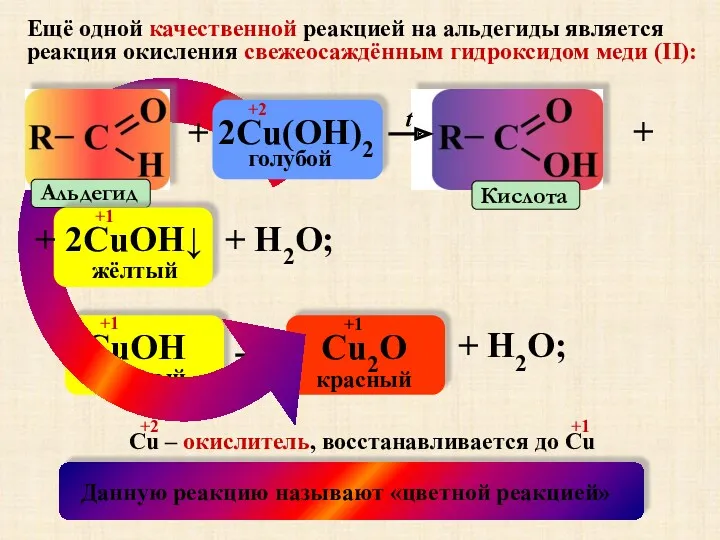
- 13. Ещё одной качественной реакцией на альдегиды является реакция окисления свежеосаждённым гидроксидом меди (II): Кислота t +
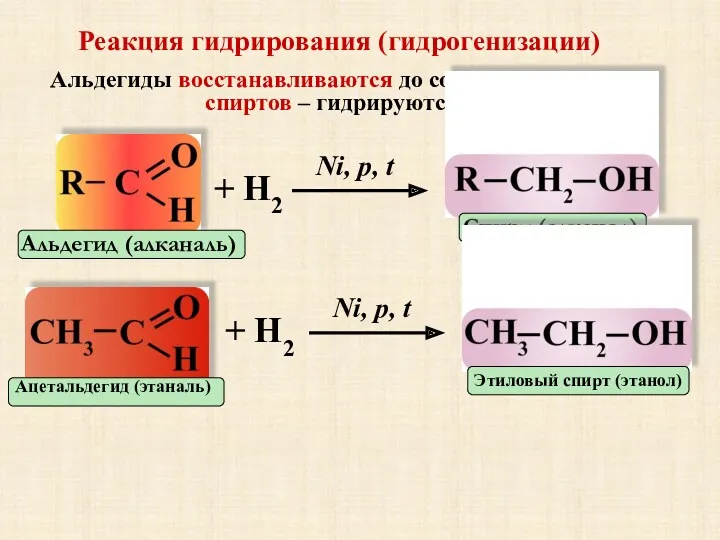
- 14. Реакция гидрирования (гидрогенизации) Альдегиды восстанавливаются до соответствующих спиртов – гидрируются: Альдегид (алканаль) + Н2 Ni, p,
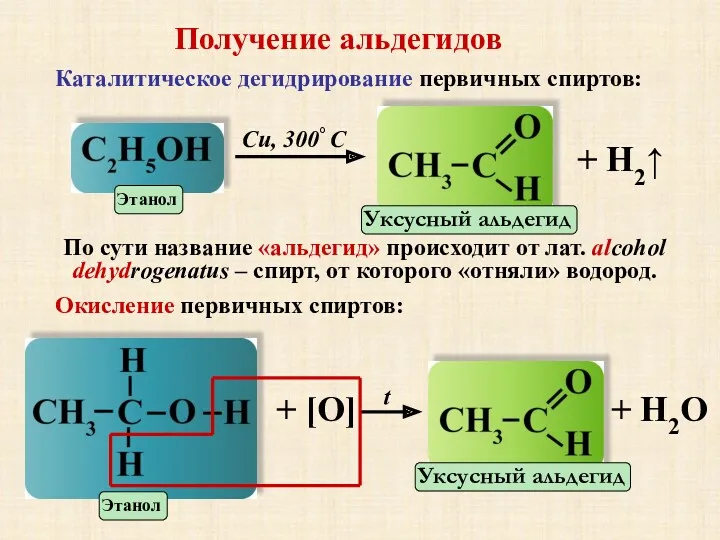
- 15. Получение альдегидов Каталитическое дегидрирование первичных спиртов: Cu, 300° C + H2↑ По сути название «альдегид» происходит
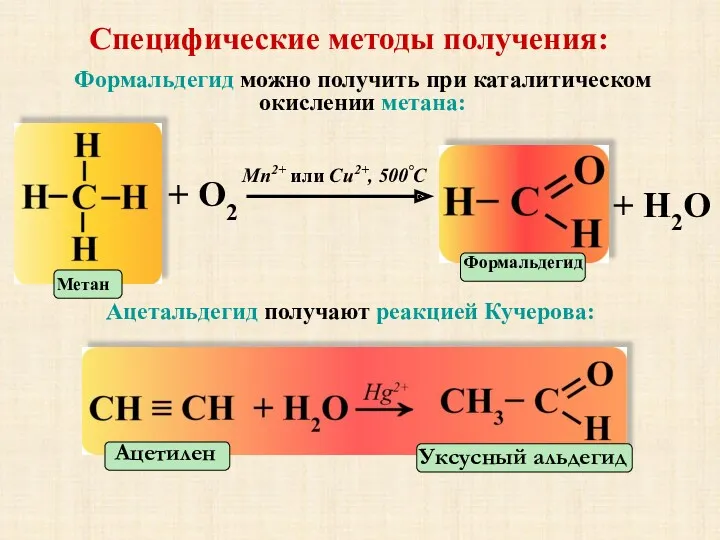
- 16. Специфические методы получения: Формальдегид можно получить при каталитическом окислении метана: + О2 + Н2О Mn2+ или
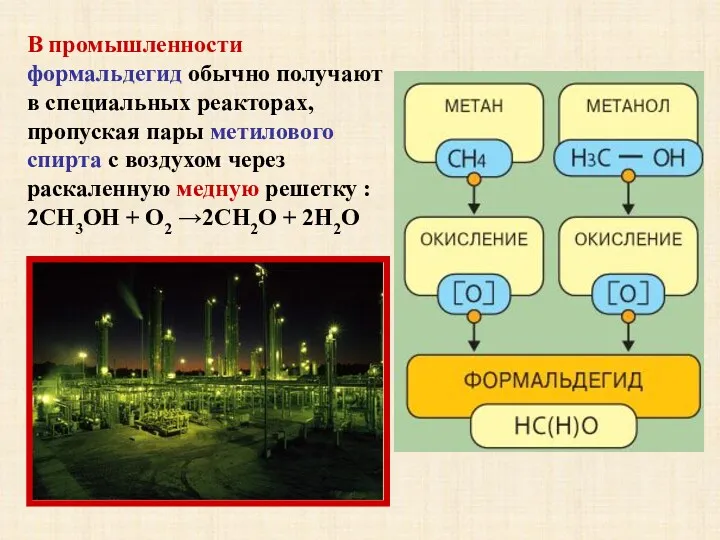
- 17. В промышленности формальдегид обычно получают в специальных реакторах, пропуская пары метилового спирта с воздухом через раскаленную
- 19. Скачать презентацию


 Гидролиз. Необратимый гидролиз
Гидролиз. Необратимый гидролиз Растворимость. Равновесие системы осадок-раствор
Растворимость. Равновесие системы осадок-раствор Побочная подгруппа. 8 группы
Побочная подгруппа. 8 группы Галогены. Строение атома
Галогены. Строение атома Химическое кафе Кислоты
Химическое кафе Кислоты Гетерофазный катализ. (Лекция 20)
Гетерофазный катализ. (Лекция 20) Классификация кристаллов по типу химической связи
Классификация кристаллов по типу химической связи Обмен липидов
Обмен липидов Определите положение в ПСХЭ элементов
Определите положение в ПСХЭ элементов La notion de catabolisme et d’anabolisme. La bioenergetique. La chaine mitochondriale de transfert d’electrons
La notion de catabolisme et d’anabolisme. La bioenergetique. La chaine mitochondriale de transfert d’electrons Подготовка к ВПР по химии. 8 класс
Подготовка к ВПР по химии. 8 класс Свойства кислорода. Получение кислорода методом вытеснения воздуха
Свойства кислорода. Получение кислорода методом вытеснения воздуха Типы химических реакций
Типы химических реакций Понятия про синтетические лекарственные средства
Понятия про синтетические лекарственные средства Побочная подгруппа VIII группы периодической системы
Побочная подгруппа VIII группы периодической системы Введение. Предмет и содержание фармацевтической химии, её связи с другими науками
Введение. Предмет и содержание фармацевтической химии, её связи с другими науками Физические и химические свойства воды
Физические и химические свойства воды Physiology lab
Physiology lab Фосфорлы тыңайытқыштар
Фосфорлы тыңайытқыштар становление органической химии
становление органической химии Обмен нуклеопротеинов
Обмен нуклеопротеинов Химические свойства алканов
Химические свойства алканов ВОДОРОД
ВОДОРОД Хінони
Хінони Физические свойства минералов
Физические свойства минералов Основные понятия и законы химии
Основные понятия и законы химии Кислоты, основания, соли в свете ТЭД
Кислоты, основания, соли в свете ТЭД Роль хімії у суспільстві
Роль хімії у суспільстві