Содержание
- 2. Лекция 11 Липогенез
- 3. Актуальность темы Липогенез – совокупность метаболических путей обмена липидов, связанных с синтезом высших жирных кислот (ВЖК)
- 4. План лекции Синтез ТАГ в тканях Транспорт эндогенных ТАГ из печени в ткани Нарушения транспорта эндогенных
- 5. Цель лекции Знать: химико-биологическую сущность процессов липогенеза, протекающих в организме человека Использовать знания о липогенезе для
- 6. План основной характеристики метаболических процессов Когда преимущественно идет процесс в норме (абсорбтивный, постабсорбтивный период, голодание, физическая
- 7. План характеристики гормонов-регуляторов метаболических процессов Химическая природа гормона (белково-пептидный, стероидный, производное аминокислоты) Место синтеза (органы, ткани)
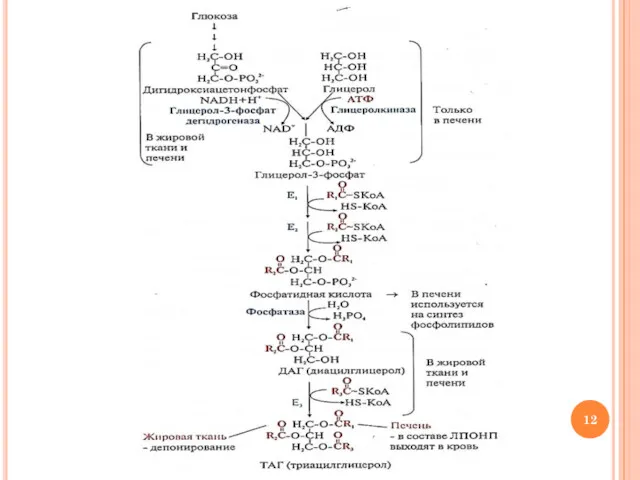
- 8. СИНТЕЗ ТАГ В ТКАНЯХ Происходит в абсорбтивный период (после приема пищи, содержащей углеводы и липиды) Основное
- 9. Синтез ТАГ: этап 1 Образование активных форм субстратов Образование активной формы ВЖК RCOOH + HS-КoA +
- 10. Синтез ТАГ: этап 1 Образование активных форм субстратов Образование активной формы глицерола глицерол + АТФ →
- 11. Синтез ТАГ: этап 2 Перенос ацильных остатков 1) глицерол-3-Р + 2 ацил-КоА → 1,2-ДАГ-3-Р (фосфатидная кислота)
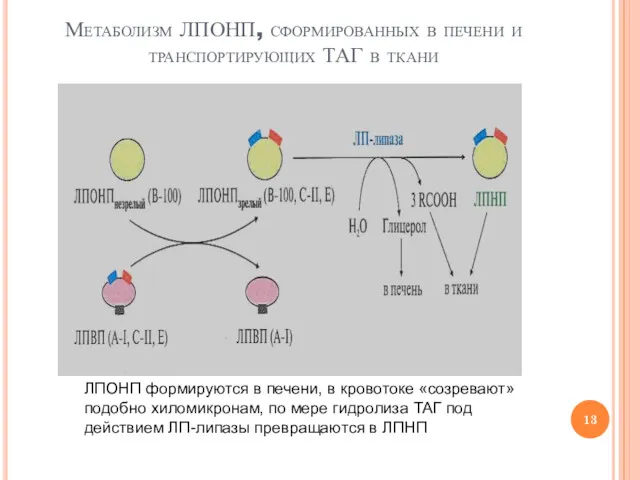
- 13. Метаболизм ЛПОНП, сформированных в печени и транспортирующих ТАГ в ткани ЛПОНП формируются в печени, в кровотоке
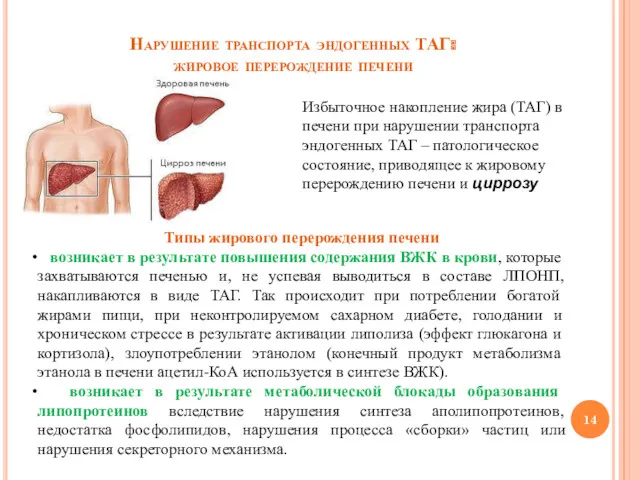
- 14. Нарушение транспорта эндогенных ТАГ: жировое перерождение печени Избыточное накопление жира (ТАГ) в печени при нарушении транспорта
- 15. СИНТЕЗ ВЖК В ТКАНЯХ Происходит в абсорбтивный период Значение: трансформация избытка углеводов и аккумулирование их энергии
- 16. Синтез ВЖК в тканях (ПРОДОЛЖЕНИЕ) Источники NADPН: ПФП окисления глюкозы (глюкозо-6-фосфат дегидрогеназа, 6-фосфоглюконатдегидрогеназа) Окислительное декарбоксилирование малата
- 17. Синтез ВЖК в тканях Основные этапы: перенос ацетильных групп ацетил-КоА из митохондрий в цитоплазму в составе
- 18. Синтез ВЖК: этап 1. Перенос ацетильных групп из митохондрий в цитоплазму Митохондрии ацетил-КоА + ЩУК +
- 19. Использование ЩУК в цитоплазме ЩУК + NADН+Н+ → малат + NAD+ фермент: NAD-малатдегидрогеназа Малат + NADP+
- 20. Синтез ЖК: этап 2 Образование малонил-КоА Ключевая реакция синтеза ВЖК ацетил-КоА + СО2 + АТФ →
- 21. Синтез ВЖК: этап 3 Удлинение углеродной цепи Ацетил-КоА – источник С15 и С16 атомов пальмитиновой кислоты
- 22. Удлинение углеродной цепи Мультиферментный комплекс - пальмитоилсинтаза Структура комплекса: димер, состоящий из 2-х идентичных полипептидных мономеров
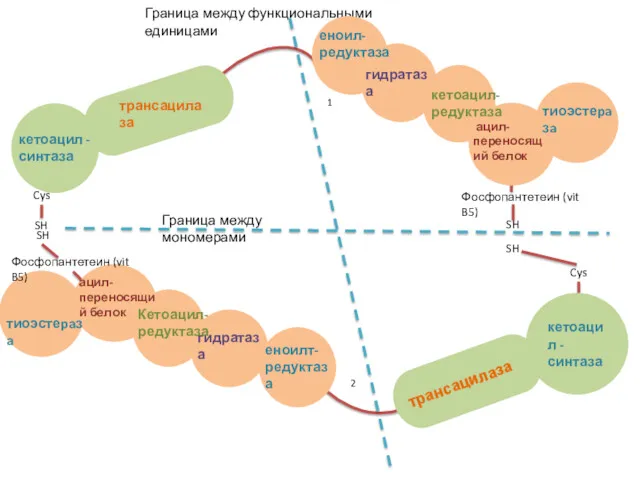
- 23. Структура мономеров пальмитоилсинтазного комплекса 7 доменов ацилпереносящий белок (АПБ), содержащий витамин В5 - пантотеновую кислоту в
- 24. кетоацил - синтаза трансацилаза Граница между функциональными единицами Граница между мономерами Еноилт- редуктаза гидратаза кетоацил-редуктаза ацил-переносящий
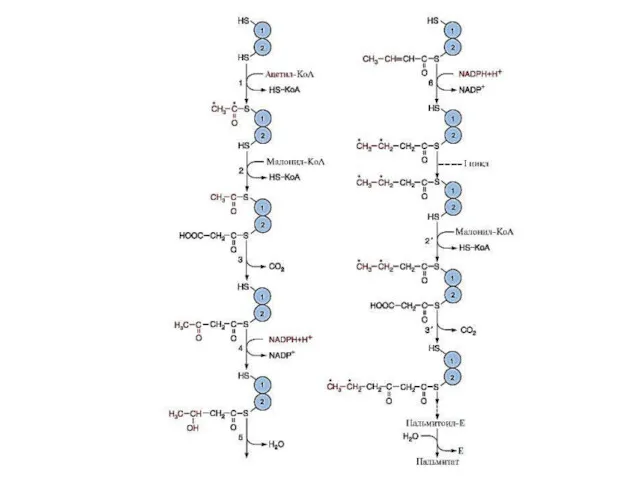
- 25. Этапы синтеза пальмитиновой кислоты Перенос ацетильного и малонильного остатков на активные центры пальмитоилсинтазы (реакции 1,2) (трансацилаза)
- 27. Суммарное уравнение синтеза пальмитиновой кислоты на пальмитоилсинтазном комплексе ацетил-КоА + 7 малонил-КоА + 14 NADPН +
- 28. Синтез ненасыщенных жирных кислот – реакции десатурации (образование двойных связей) Синтез пальмитоолеиновой кислоты С16:1, 9, ώ7
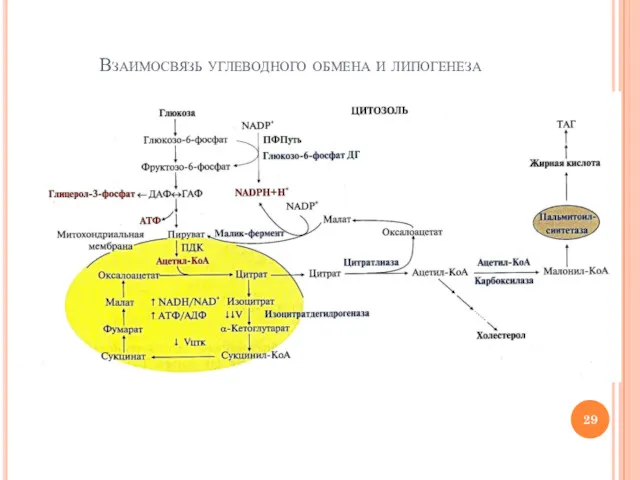
- 29. Взаимосвязь углеводного обмена и липогенеза
- 30. «Точки соприкосновения» липогенеза и обмена глюкозы Гликолиз – источник АТФ для реакций синтеза ВЖК и ТАГ
- 31. Регуляция липогенеза Синтез ВЖК «запускается» инсулином Вспомните механизм передачи сигнала инсулина в клетки-мишени! Механизмы регуляции стимулирование
- 32. Механизмы регуляции липогенеза инсулином (продолжение) индукция синтеза ферментов в печени и жировой ткани липидного обмена: ЛП-липазы,
- 33. Аллостерическая регуляция липогенеза При избыточном потреблении легкоусвояемых углеводов и активации гликолиза, реакций ОПК энергетический статус гепатоцитов
- 34. Регуляция активности ацетил-КоА карбоксилазы – ключевого фермента синтеза ВЖК Способы регуляции индукция синтеза (инсулин) ассоциация /диссоциация
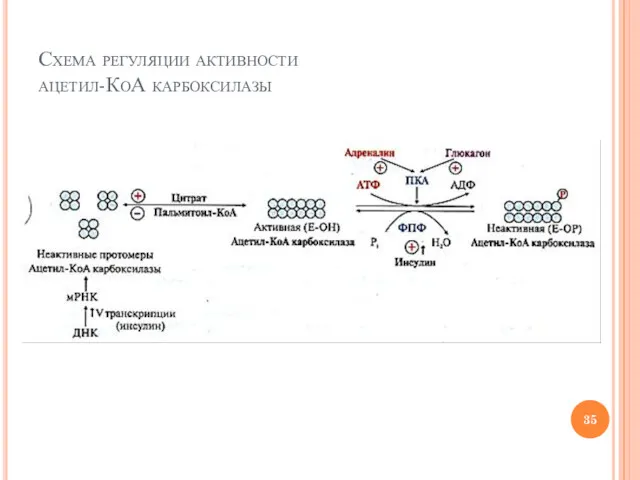
- 35. Схема регуляции активности ацетил-КоА карбоксилазы
- 36. абсорбтивный период После приема пищи, содержащей липиды и углеводы в крови повышается Уровень хиломикронов (ТАГ) Концентрация
- 37. Ожирение В норме у человека с массой тела 70 кг количество жира в депо - 10-11
- 38. Первичное ожирение: причины Алиментарный дисбаланс – избыточная калорийность питания по сравнению с расходами энергии Генетические факторы
- 39. Первичное ожирение: причины (продолжение) Генетические факторы ожирения Например: мутация гена белка адипоцитов – лептина лептин действует
- 40. Вторичное ожирение: причины Вторичное ожирение развивается в результате какого-либо заболевания (чаще эндокринного, например, гипотиреоза) Чем опасно
- 41. Заключение Процессы липогенеза (синтез ВЖК и ТАГ) являются источником образования в организме резервного «топлива» с большой
- 43. Скачать презентацию

































 Основания. 8 класс
Основания. 8 класс Контрольная работа по дисциплине Физическая химия. Раздел: Электрохимия
Контрольная работа по дисциплине Физическая химия. Раздел: Электрохимия Поняття про побутові хімікати
Поняття про побутові хімікати Цинковое покрытие
Цинковое покрытие Кремний и его соединения. Аллотропные модификации
Кремний и его соединения. Аллотропные модификации Р-элементы VI A группы. Свойства их соединений
Р-элементы VI A группы. Свойства их соединений Группы сходных химических элементов
Группы сходных химических элементов Кислород
Кислород Кислород. Строение молекулы кислорода. Получение кислорода. Взаимодействие с кислородом простых и сложных веществ
Кислород. Строение молекулы кислорода. Получение кислорода. Взаимодействие с кислородом простых и сложных веществ Свойства фосфора
Свойства фосфора Бытовая химическая грамотность
Бытовая химическая грамотность Электролитическая диссоциация. Реакции ионного обмена
Электролитическая диссоциация. Реакции ионного обмена Алмазы. Бриллианты
Алмазы. Бриллианты Пластмаси. Класифікація пластмас
Пластмаси. Класифікація пластмас Арены. Бензол
Арены. Бензол Камни и Скорпион
Камни и Скорпион Наноматериалы. Свойства наноматериалов. Особенности свойств
Наноматериалы. Свойства наноматериалов. Особенности свойств Силикаты. Гранат. Берилл
Силикаты. Гранат. Берилл Reactors for catalytic alkylation
Reactors for catalytic alkylation Электрохимия. Электропроводность растворов. Электродные потенциалы. Гальванические элементы
Электрохимия. Электропроводность растворов. Электродные потенциалы. Гальванические элементы Домашнее задание по теме Химические свойства альдегидов, их получение
Домашнее задание по теме Химические свойства альдегидов, их получение Кинетика процессов твердофазного взаимодействия
Кинетика процессов твердофазного взаимодействия Тяжёлая вода
Тяжёлая вода Fiber-Sludge-Sulfur-Beton (FiSHSB)
Fiber-Sludge-Sulfur-Beton (FiSHSB) Двовимірний ямр. Приклади
Двовимірний ямр. Приклади Чистые вещества и смеси
Чистые вещества и смеси Понятие о спиртах. 9 класс
Понятие о спиртах. 9 класс Методы титрования. Перманганатометрия. (Лекция 24)
Методы титрования. Перманганатометрия. (Лекция 24)