Содержание
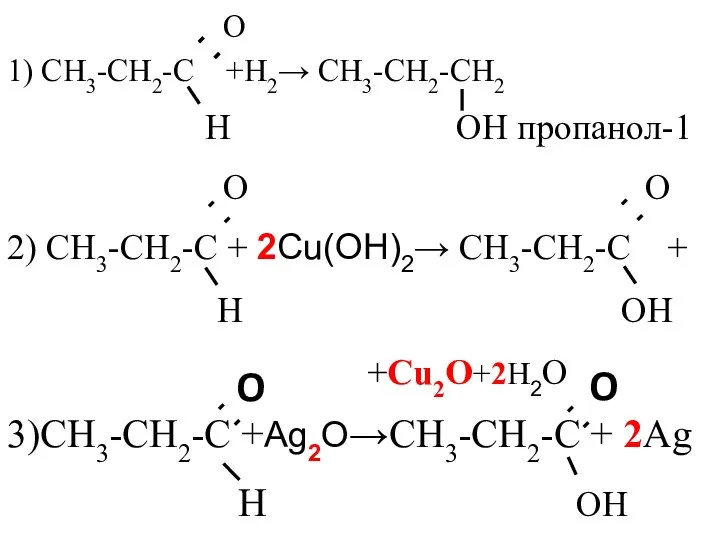
- 2. пропаналь + водород → пропаналь + Сu(OH)2 → пропаналь + Ag2O → пропанол-1 + СuO →
- 3. О 1) СН3-СН2-С +Н2→ СН3-СН2-СН2 Н ОН пропанол-1 О О 2) СН3-СН2-С + 2Сu(OH)2→ СН3-СН2-С +
- 4. О 4) СН3-СН2-СН2 + СuO→СН3-СН2-С + Cu +Н2O ОН Н 5)* СН3-СН-СН3 + СuO→СН3-С-СН3 + Cu
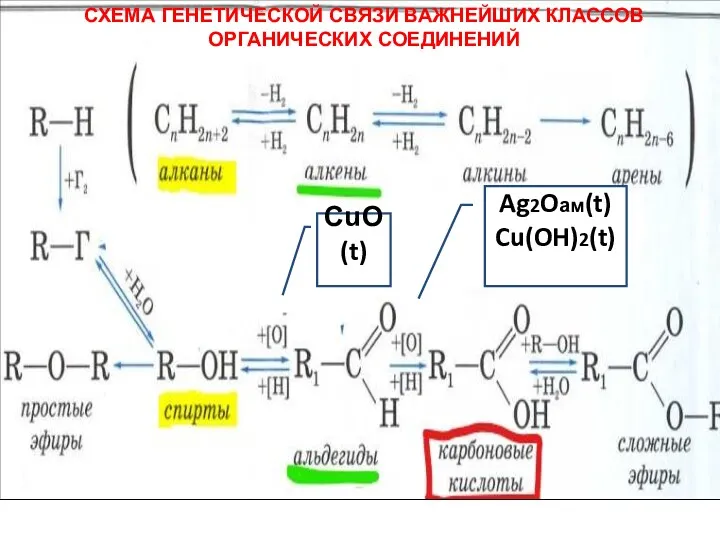
- 6. СХЕМА ГЕНЕТИЧЕСКОЙ СВЯЗИ ВАЖНЕЙШИХ КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Ag2Oам(t) Cu(OH)2(t) CuO(t)
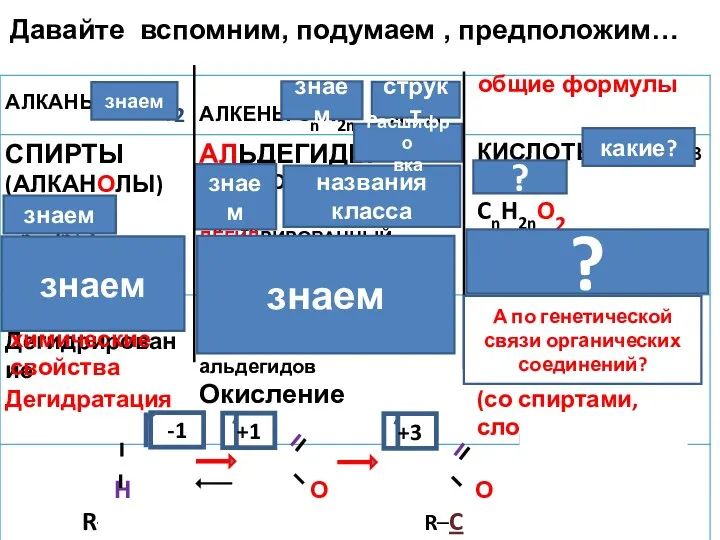
- 7. знаем знаем знаем знаем ? названия класса соли знаем знаем ? структ химические свойства Расшифро вка
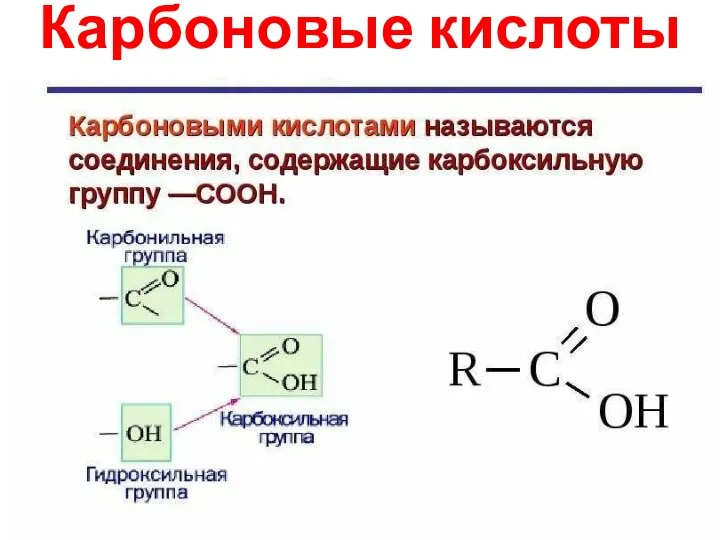
- 8. Карбоновые кислоты
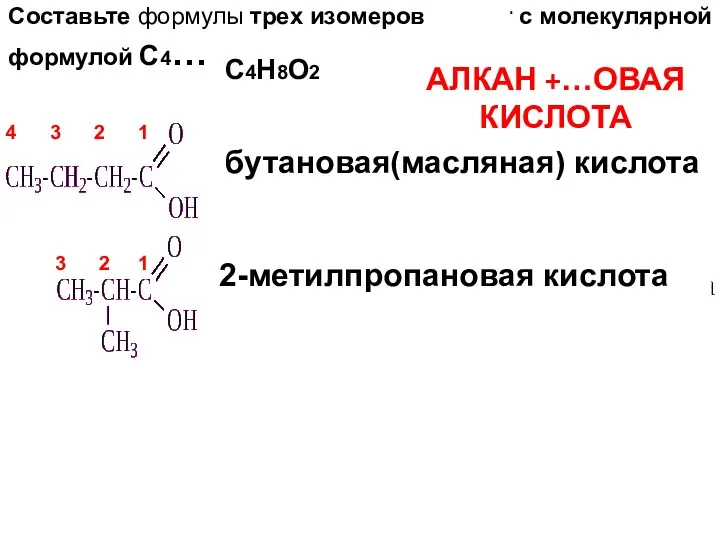
- 9. Составьте формулы трех изомеров кислот с молекулярной формулой С4… СсСС С4Н8О2 4 3 2 1 бутановая(масляная)
- 10. Составьте формулы трех изомеров с молекулярной формулой СсСС С4Н8О2 4 3 2 1 бутановая(масляная) кислота 2-метилпропановая
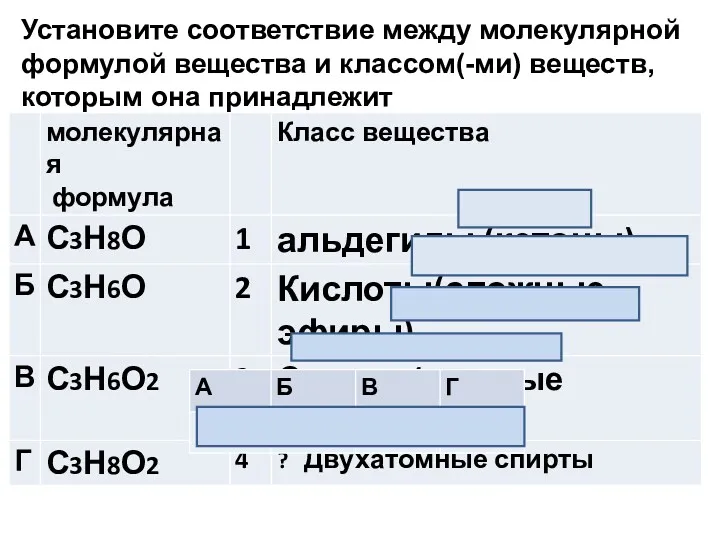
- 11. Установите соответствие между молекулярной формулой вещества и классом(-ми) веществ, которым она принадлежит
- 12. Сравнение t кипения(высокая/низкая) и растворимости алканов, спиртов, эфиров, альдегидов и кислот t кип Знаем!Объясняла! Растворимость Знаем!
- 13. Классификация карбоновых кислот R-C 1 По характеру радикала(R-) 1Предельные- СН3- СН2-СООН 2 Непредельные СН2= СН-СООН 3
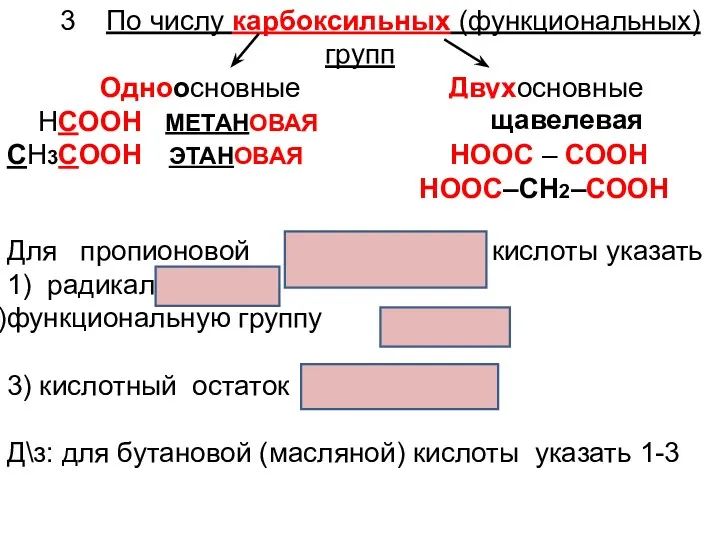
- 14. 3 По числу карбоксильных (функциональных) групп Одноосновные Двухосновные НСООН МЕТАНОВАЯ СН3СООН ЭТАНОВАЯ НООС – СООН СН3СН2СООН
- 15. Химические свойства кислот Основные оксиды Кислоты Основания Сои ли НО H2O 3 2 4, ПОЛУЧЕНИЕ Металлы
- 16. 1) Слабые электролиты (диссоциация!!!) НСООН ↔ НСОО + Н+ СН3СООН ↔ СН3СОО + Н+ формиат-ион, соли
- 17. 4) соль + кислота = новая соль + новая кислота NaHCO3 + СН3СООН = СН3СООNa +
- 18. состав строение свойства Вещества
- 19. Причина общих свойств неорганических и органических кислот – присутствие ионов водорода в их растворах. Органические кислоты
- 20. что добавлено? Растворение синего осадка, образование голубого раствора образование ярко-синего раствора Можно ли с помощью гидроксида
- 21. Домашнее задание - в презентации и пар.23 упр 1, (для сдающих ЕГЭ -ниже)
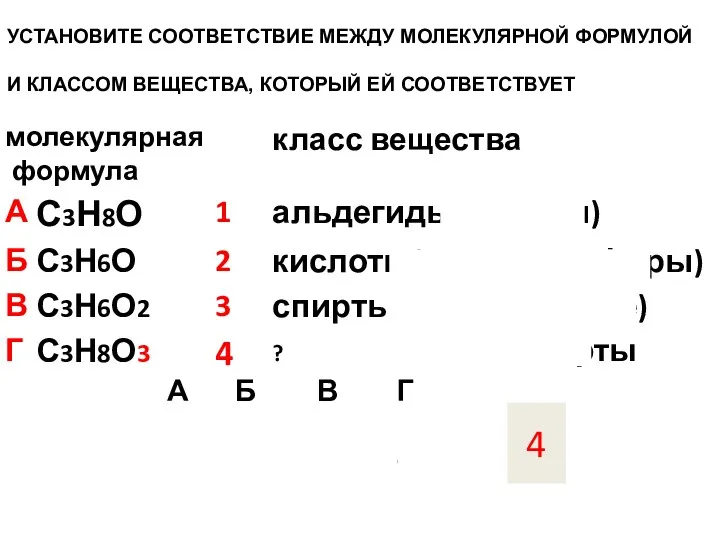
- 22. УСТАНОВИТЕ СООТВЕТСТВИЕ МЕЖДУ МОЛЕКУЛЯРНОЙ ФОРМУЛОЙ И КЛАССОМ ВЕЩЕСТВА, КОТОРЫЙ ЕЙ СООТВЕТСТВУЕТ 4
- 24. Скачать презентацию













 Гидролиз солей
Гидролиз солей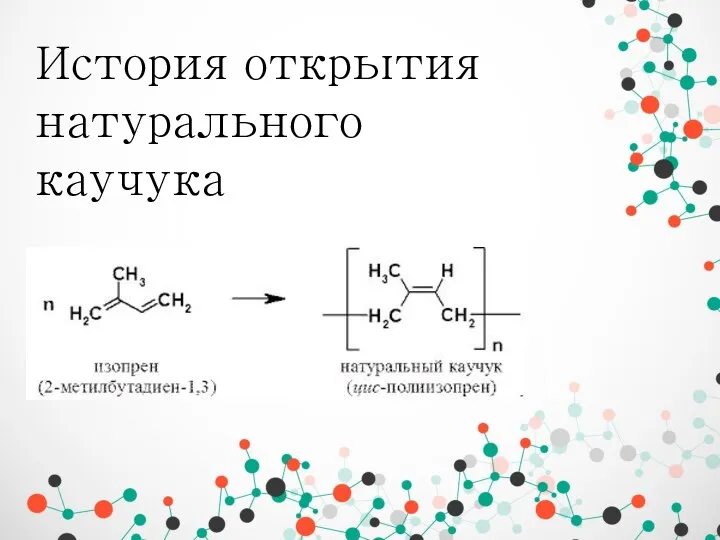 История открытия натурального каучука
История открытия натурального каучука Химическая промышленность России входит в авангардную тройку
Химическая промышленность России входит в авангардную тройку Коррозия металлов
Коррозия металлов Минералы. Химическая классификация
Минералы. Химическая классификация Свойства моторных топлив
Свойства моторных топлив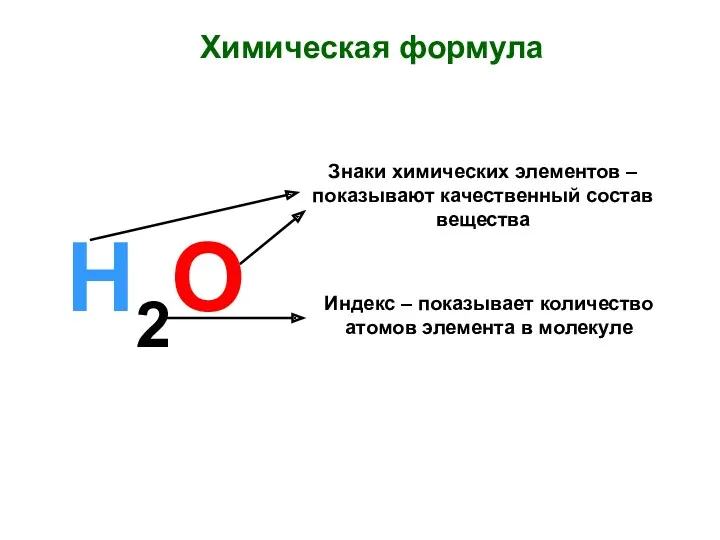 Химическая формула. Знаки химических элементов
Химическая формула. Знаки химических элементов Классификация строительных материалов. Коррозия бетона и железобетона
Классификация строительных материалов. Коррозия бетона и железобетона Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Ветеринариялық гигиена және санитария
Ветеринариялық гигиена және санитария Классификация моторных масел
Классификация моторных масел Алюминий на кухне - опасный враг или верный помощник?
Алюминий на кухне - опасный враг или верный помощник? Уравнения химических реакций
Уравнения химических реакций Природний газ
Природний газ Physical and chemical properties of oil
Physical and chemical properties of oil Подготовка учащихся к выполнению заданий различного уровня сложности ЕГЭ по химии
Подготовка учащихся к выполнению заданий различного уровня сложности ЕГЭ по химии Таза зат және қоспа. Қоспаларды бөлу әдістері. Қосылыс Рure substances and mixtures . Мethods for separating mixtures. Compound
Таза зат және қоспа. Қоспаларды бөлу әдістері. Қосылыс Рure substances and mixtures . Мethods for separating mixtures. Compound Тепловой эффект химической реакции, термохимические уравнения, экзо- и эндотермические реакции
Тепловой эффект химической реакции, термохимические уравнения, экзо- и эндотермические реакции Химическая посуда и ее назначения (6)
Химическая посуда и ее назначения (6) Бейорганикалық заттар технологиясындағы жүйелерді термодинамикалық талдау
Бейорганикалық заттар технологиясындағы жүйелерді термодинамикалық талдау Электрохимические методы. Кондуктометрия в анализе объектов окружающей среды
Электрохимические методы. Кондуктометрия в анализе объектов окружающей среды Хімічні властивості оксидів
Хімічні властивості оксидів Основания. Состав, классификация, свойства, получение
Основания. Состав, классификация, свойства, получение Виды соли и ее значение в питании
Виды соли и ее значение в питании Производство извести в домашних условиях. 7 класс
Производство извести в домашних условиях. 7 класс Альдегиды и кетоны. 10 класс
Альдегиды и кетоны. 10 класс Координационные комплексные соединения
Координационные комплексные соединения Реакции солей в растворе. Гидролиз солей. Водородный показатель рН
Реакции солей в растворе. Гидролиз солей. Водородный показатель рН