Содержание
- 2. ПЛАН ВЕБИНАРА: 1. Общие рекомендации по планированию подготовки учащихся к ЕГЭ по химии. 2. Рекомендации по
- 3. Важная информация о ЕГЭ Записи вебинаров https://www.youtube.com/watch?v=AX1iOh9UCp0 https://www.youtube.com/watch?v=tQynD4W-FkY Вебинар МГУ 29 августа 2018 г: Вебинар издательства
- 4. Важная информация о ЕГЭ www.fipi.ru
- 5. Важная информация о ЕГЭ Видеоконсультации - в разделе «Для выпускников» www.fipi.ru
- 6. Важная информация о ЕГЭ www.fipi.ru Информация о правилах оценивания и требованиях к оформлению заданий 2-ой части
- 7. Каких заданий не бывает на ЕГЭ по химии и почему 1. В на стоящее время содержание
- 8. Каких заданий не бывает на ЕГЭ по химии и почему 3. Для проверки усвоения определенных элементов
- 9. Рекомендации по подготовке к ЕГЭ Н.Е. Кузьменко, В.В. Еремин, В.А. Попков Начала химии. Современный курс для
- 10. Рекомендации по подготовке к ЕГЭ Дополнительная литература: Пособие содержит весь необходимый теоретический и фактологический материал, изучение
- 11. Рекомендации по подготовке к ЕГЭ Завершающий этап подготовки – тренировка в выполнении заданий и типовых вариантов
- 12. Ю.Н. Медведев. Химия. ЕГЭ 2019. Типовые тестовые задания. 14 вариантов ЕГЭ 2019. Химия. 30 вариантов. Типовые
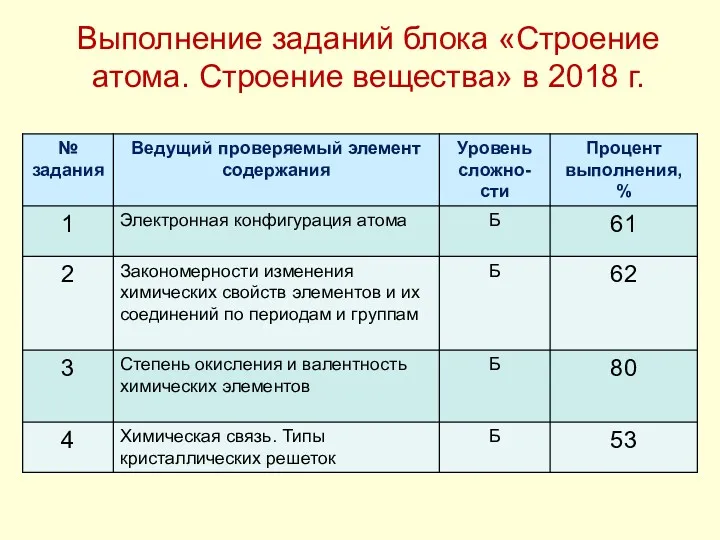
- 13. Выполнение заданий блока «Строение атома. Строение вещества» в 2018 г.
- 14. О заданиях 1 Пример 1-1 Вариант формулировки: определите , атомы каких из указанных в ряду элементов
- 15. Систематизация теоретического материала 1. Как определить число протонов и нейтронов в ядре атома? Что такое изотопы?
- 16. 8. Как записать электронные конфигурации ионов? Приведите пример двух катионов и двух анионов, имеющих электронную конфигурацию
- 17. Пример 1-2 О заданиях 1 Пример 1-3
- 18. О заданиях 1 Пример 1-4 Пример 1-5
- 19. Пример 1-6 О заданиях 1
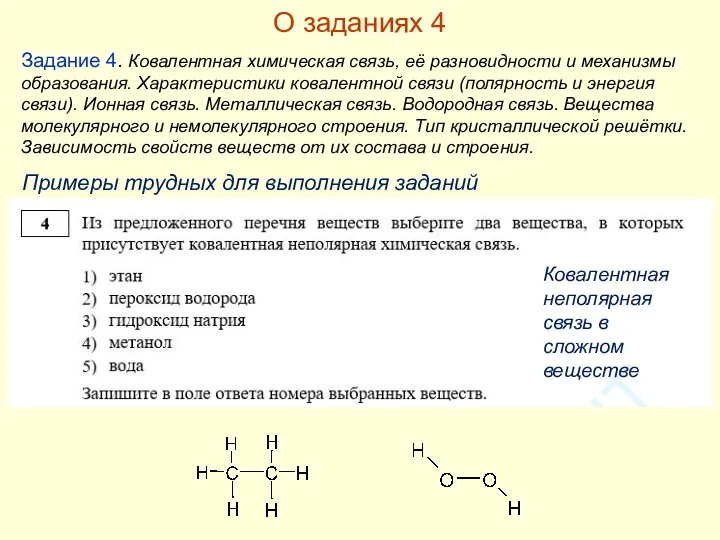
- 20. О заданиях 4 Задание 4. Ковалентная химическая связь, её разновидности и механизмы образования. Характеристики ковалентной связи
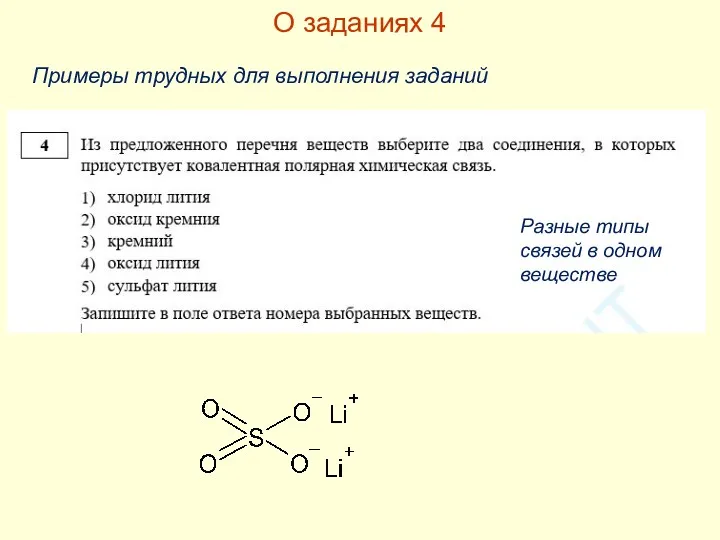
- 21. О заданиях 4 Примеры трудных для выполнения заданий Разные типы связей в одном веществе
- 22. О заданиях 4 Примеры трудных для выполнения заданий Водородная связь Возникает между молекулами NH3, H2O, HF,
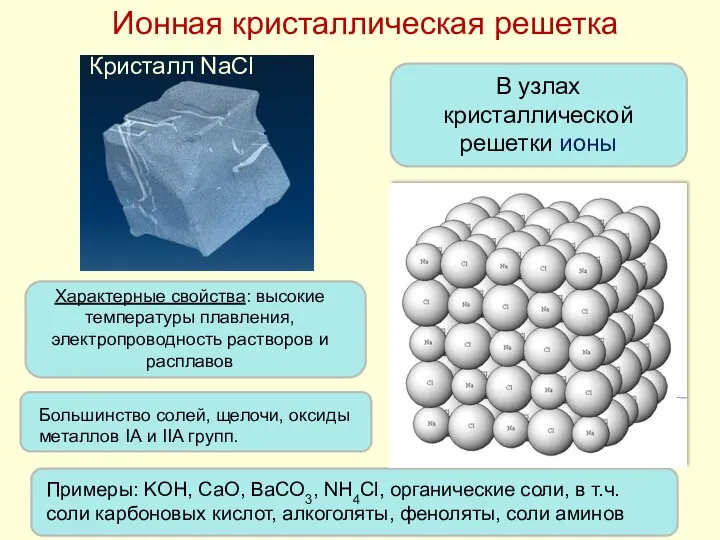
- 23. Ионная кристаллическая решетка Кристалл NaCl В узлах кристаллической решетки ионы Характерные свойства: высокие температуры плавления, электропроводность
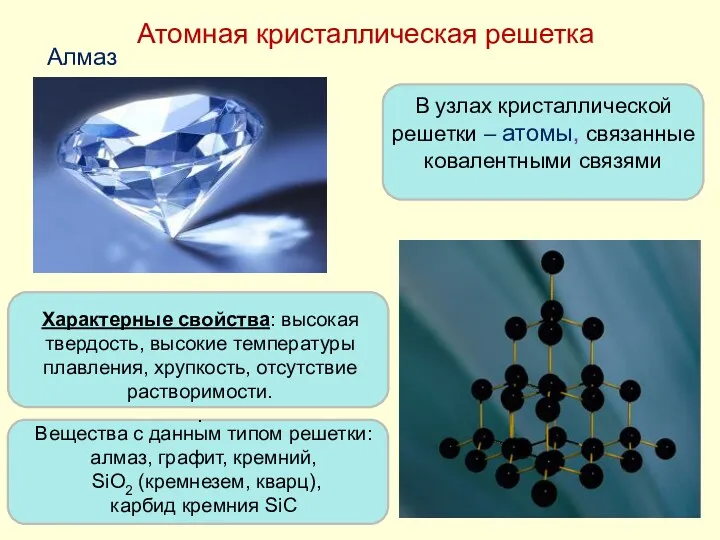
- 24. Атомная кристаллическая решетка В узлах кристаллической решетки – атомы, связанные ковалентными связями Алмаз Характерные свойства: высокая
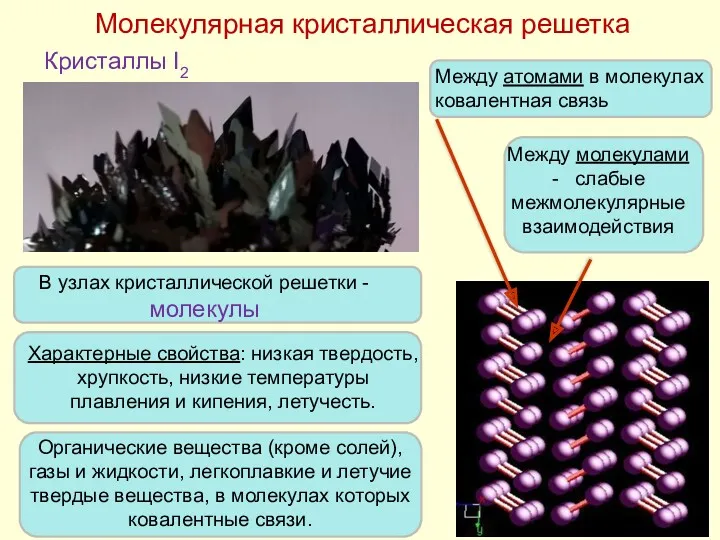
- 25. Молекулярная кристаллическая решетка Характерные свойства: низкая твердость, хрупкость, низкие температуры плавления и кипения, летучесть. Между атомами
- 26. Металлическая кристаллическая решетка Na В узлах кристаллической решетки атомы и катионы металла. Валентные электроны обобществлены, образуют
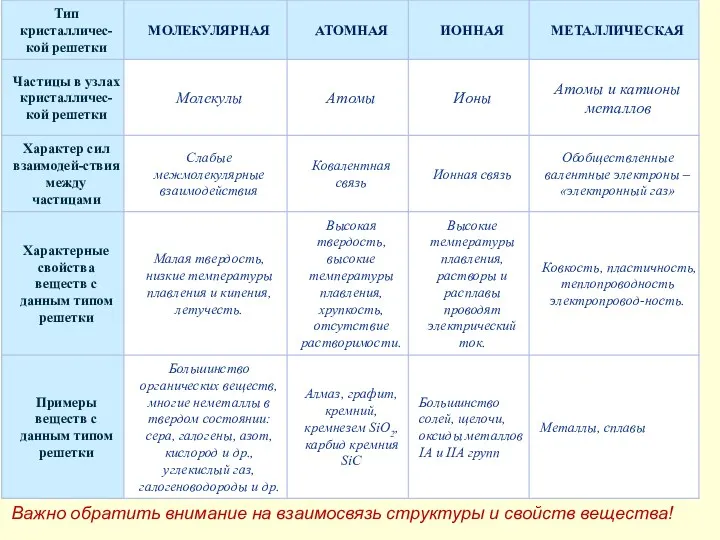
- 27. Важно обратить внимание на взаимосвязь структуры и свойств вещества!
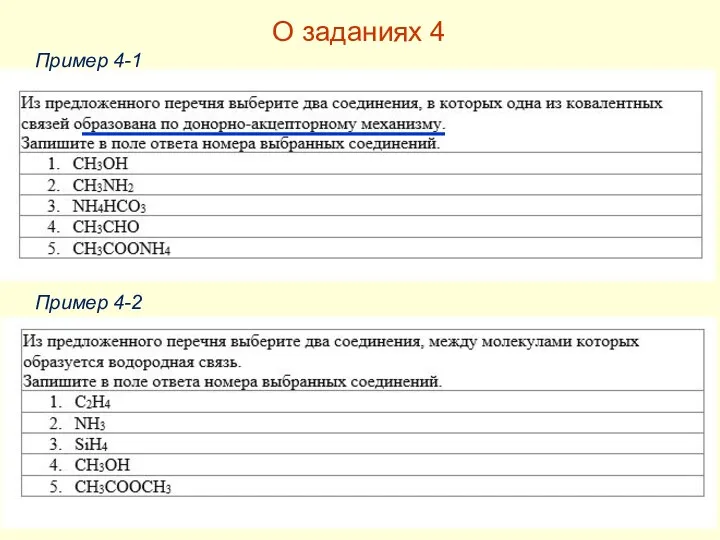
- 28. О заданиях 4 Пример 4-1 Пример 4-2
- 29. О заданиях 4 Пример 4-3 Пример 4-4
- 30. О заданиях 4 Пример 4-5 Пример 4-6
- 31. О заданиях 7 Задание 7. Характерные химические свойства оснований и амфотерных гидроксидов. Характерные химические свойства кислот.
- 32. Такого задания не будет! Вопрос по заданию 7
- 33. Задание 8. Характерные химические свойства неорганических веществ: – простых веществ–металлов: щелочных, щелочноземельных, магния, алюминия, переходных металлов
- 34. Систематизация теоретического материала 1. Вещества, имеющие кислотный характер, реагируют с веществами основного характера. Давайте вспомним! 3.
- 35. Систематизация теоретического материала 5. Оксиды, как правило, не реагируют с солями. Иногда встречаются реакции типа Na2CO3
- 36. 2334 О заданиях 8 Пример 8-1 4153 Пример 8-2
- 37. 1542 О заданиях 8 4513 Пример 8-3 Пример 8-4
- 38. О заданиях 8 1523 5214 Пример 8-5 Пример 8-6
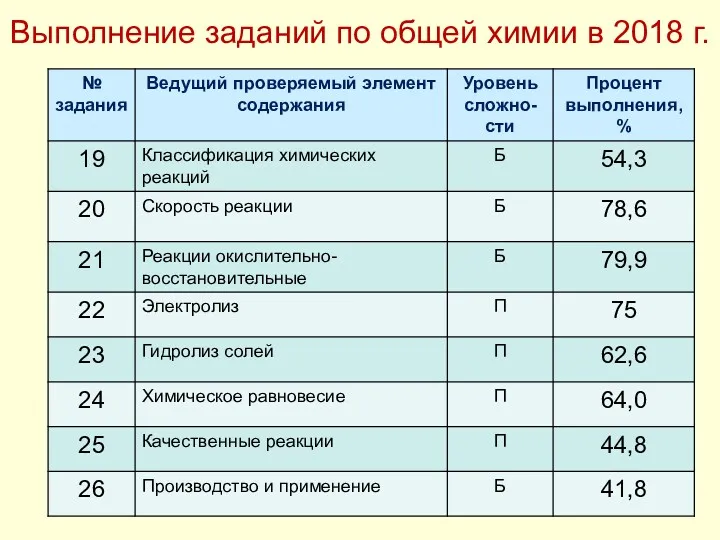
- 39. Выполнение заданий по общей химии в 2018 г.
- 40. О заданиях 23 Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная Пример 23-1 Пример 23-2
- 41. О заданиях 23
- 42. О заданиях 23 В заданиях 23 могут встретиться: соли рубидия и цезия, аммония и метиламмония; ацетаты,
- 43. Гидролиз бинарных соединений (задания 9, 32, 34) Гидролиз карбидов кальция и алюминия: CaC2 + 2H2O =
- 44. Совместный гидролиз (задания 9, 32, 34) Совместный гидролиз с участием двухзарядных катионов не используется в заданиях
- 45. Важнейшие окислители: Cl2, Br2, HNO3, H2SO4(конц.), KMnO4, MnO2, K2Cr2O7, K2CrO4, KClO, KClO3, H2O2, (O2, соединения Fe(III))
- 46. Задание 30 Эксперту необходимо в первую очередь сосредоточить внимание на тех ведущих умениях, которые по своей
- 47. Вопрос по оцениванию задания 30
- 48. K2Cr2O7 + KBr + H2SO4 → Cr2(SO4)3 + Br2 + … 2Cr+6 + 6ē → 2Cr+3
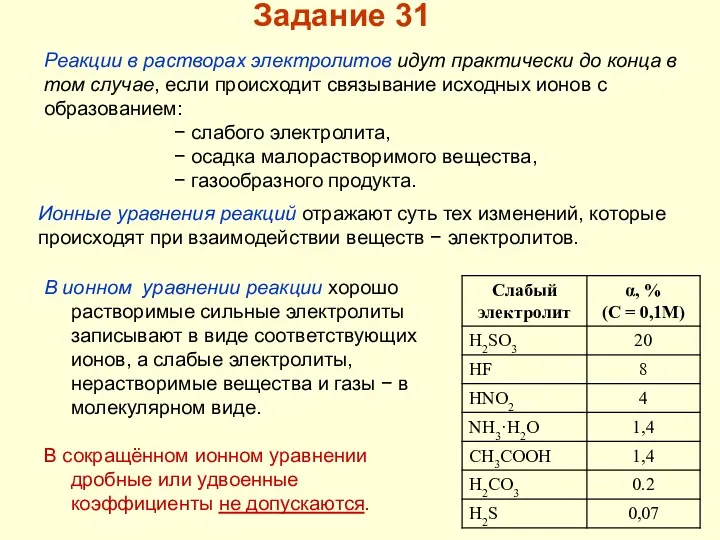
- 49. Ионные уравнения реакций отражают суть тех изменений, которые происходят при взаимодействии веществ − электролитов. . Реакции
- 50. Если в качестве одного из исходных веществ выбрана соль,то она должна быть растворима в воде (исключение
- 51. Реакции образования гидроксокомплексов при взаимодействии растворов щелочей и растворимых солей цинка и алюминия также можно отнести
- 52. Нитрит калия KNO2 и ацетат натрия CH3COONa представляют собой соли слабых кислот. Сильная азотная кислота способна
- 53. О задачах 2. Растворимость сероводорода в воде при н.у. составляет 2,5 л на 1 л воды.
- 55. Скачать презентацию










































 Каменный уголь
Каменный уголь p-элементы 17 группы периодической системы: галогены
p-элементы 17 группы периодической системы: галогены Снежинки. Рождение снежинки
Снежинки. Рождение снежинки Соли, их классификация и свойства
Соли, их классификация и свойства Коррозионная стойкость и повышение долговечности полимерных строительных материалов
Коррозионная стойкость и повышение долговечности полимерных строительных материалов Одноатомные спирты. Простые эфиры
Одноатомные спирты. Простые эфиры Общая характеристика углеводов: глюкоза
Общая характеристика углеводов: глюкоза Химические методы выявления потожировых следов
Химические методы выявления потожировых следов Углеводы (монозы, биозы)
Углеводы (монозы, биозы) Соли, их классификация и свойства
Соли, их классификация и свойства Лекарства
Лекарства Чистые вещества и смеси
Чистые вещества и смеси Обратимые реакции. Химическое равновесие. Смещение равновесия
Обратимые реакции. Химическое равновесие. Смещение равновесия Защита металлов от коррозии
Защита металлов от коррозии Закон сохранения массы веществ
Закон сохранения массы веществ Розрахунки за хімічними рівняннями
Розрахунки за хімічними рівняннями Многоатомные спирты
Многоатомные спирты Пниктогены элеметны VA группы
Пниктогены элеметны VA группы СВОЙСТВА ЧЕРНЫХ И ЦВЕТНЫХ МЕТАЛЛОВ.
СВОЙСТВА ЧЕРНЫХ И ЦВЕТНЫХ МЕТАЛЛОВ. Каталітичний крекінг. Основні етапи становлення технології каталітичного крекінгу. Каталізатор крекінгу
Каталітичний крекінг. Основні етапи становлення технології каталітичного крекінгу. Каталізатор крекінгу Периодический закон и система элементов Д.И. Менделеева
Периодический закон и система элементов Д.И. Менделеева Ізомери у природі
Ізомери у природі Ионная связь и степень окисления. 8 класс
Ионная связь и степень окисления. 8 класс Геохимические показатели техногенеза
Геохимические показатели техногенеза Алены. Строение, изомерия, номенклатура
Алены. Строение, изомерия, номенклатура Энергетика химических процессов. Энтропия и энергия Гиббса
Энергетика химических процессов. Энтропия и энергия Гиббса Гидролиз солей
Гидролиз солей Кластер Химические реакции
Кластер Химические реакции