Содержание
- 2. Li …2s1 Be…2s2 B…2s22p1 …. F…2s22p5 Ne…2s22p6 Na …3s1 Mg …3s2 Al …3s23p1 ….. Cl…3s2 3p5
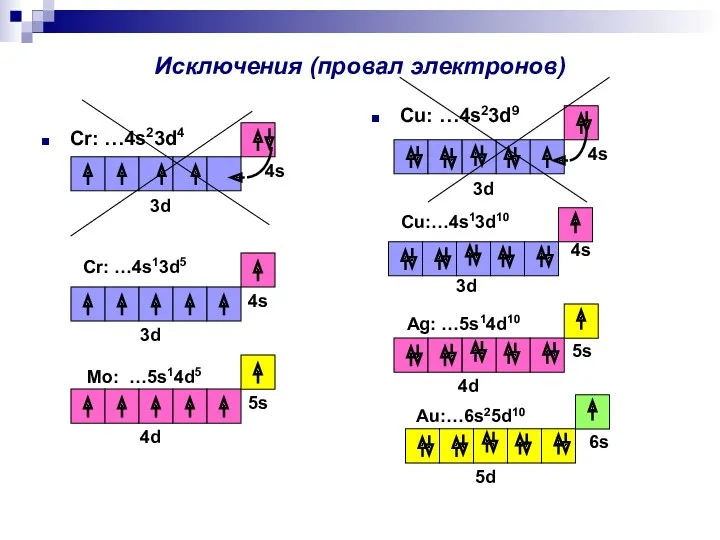
- 3. Исключения (провал электронов) Cr: …4s23d4 Cu: …4s23d9 Cr: …4s13d5 3d 4s 3d 4s Cu:…4s13d10 3d 4s
- 4. La …6s25d1 Ce …6s25d14f1 Pr …6s25d14f2 Nd…6s25d14f3 ……………… Lu…6s25d14f14 Hf…6s25d2(4f14) В 6-ом и 7-ом периодах после
- 5. Периодический закон (Д.И.Менделеев, 1869) Химические свойства простых веществ, а также свойства и формы соединений элементов находятся
- 6. Триады Деберейнера (1811-1829) F2 – Cl2 – I2 Ca – Sr – Ba S – Se
- 7. Д.И.Менделеев (1834-1907) Открыл периодический закон Предсказал открытие и свойства ряда элементов, открытых позд-нее (галлий, скандий, германий
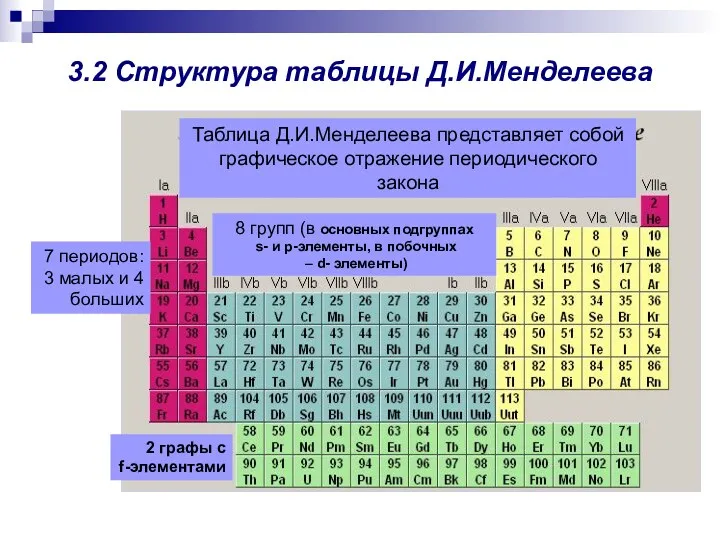
- 8. 3.2 Структура таблицы Д.И.Менделеева Таблица Д.И.Менделеева представляет собой графическое отражение периодического закона 7 периодов: 3 малых
- 9. 3.2. Химические свойства элементов и их положение в таблице Д.И.Менделеева Наиболее устойчивой является конфигурация инертного га-за,
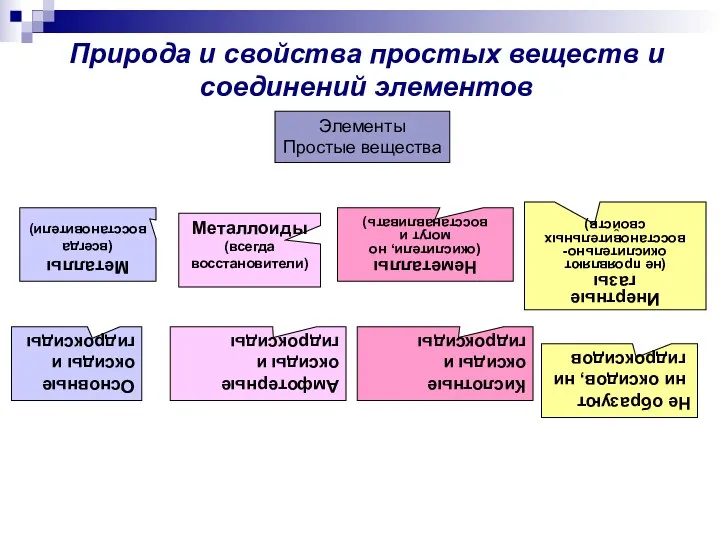
- 10. Природа и свойства простых веществ и соединений элементов Элементы Простые вещества Металлы (всегда восстановители) Неметаллы (окислители,
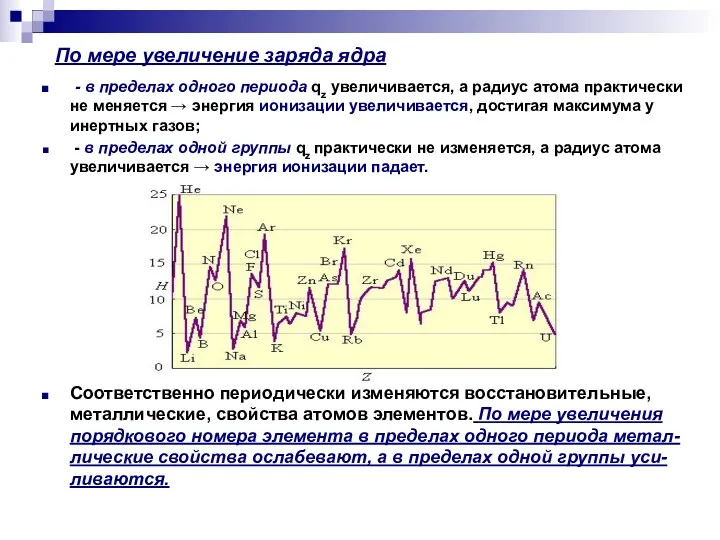
- 11. Восстановительные свойства атомов элементов, характерные для металлов, определяются энергией (потенциалом) ионизации. Энергией (потенциалом) ионизации атома называется
- 12. По мере увеличение заряда ядра - в пределах одного периода qz увеличивается, а радиус атома практически
- 14. Скачать презентацию







 Производство азотной кислоты
Производство азотной кислоты 20230419_izomery
20230419_izomery Обратимые реакции. Химическое равновесие. Смещение равновесия
Обратимые реакции. Химическое равновесие. Смещение равновесия Строение атома
Строение атома Физические и химические явления. Признаки и условия протекания химических реакций
Физические и химические явления. Признаки и условия протекания химических реакций Полиамидные волокна
Полиамидные волокна Непредельные углеводороды
Непредельные углеводороды General, specific properties are common to all matters
General, specific properties are common to all matters III А – топтың элементтері
III А – топтың элементтері Степень диссоциации. 9 класс
Степень диссоциации. 9 класс Химическая связь и ее типы. Основные классы неорганических соединений
Химическая связь и ее типы. Основные классы неорганических соединений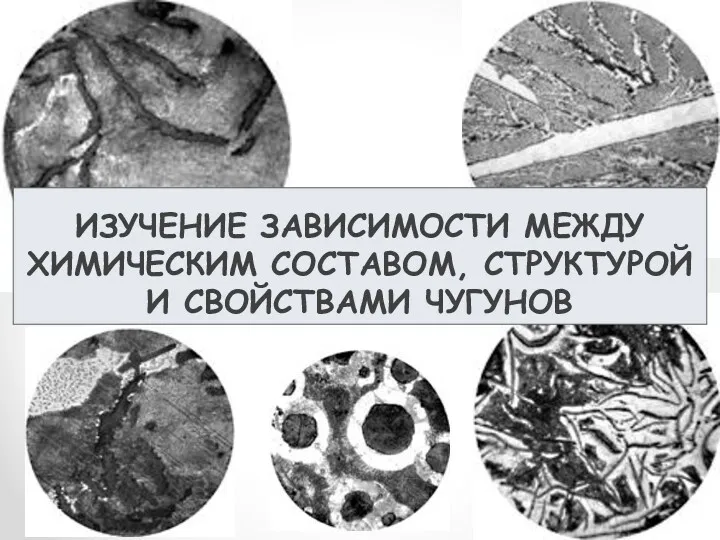 Изучение зависимости между химическим составом, структурой и свойствами чугунов
Изучение зависимости между химическим составом, структурой и свойствами чугунов Волшебные кристалы
Волшебные кристалы Тамақ өнімдерінің құрылымын және физико-химиялық қасиеттерін өзгертетін тағамдық қоспалар
Тамақ өнімдерінің құрылымын және физико-химиялық қасиеттерін өзгертетін тағамдық қоспалар Водород. Распространенность в природе
Водород. Распространенность в природе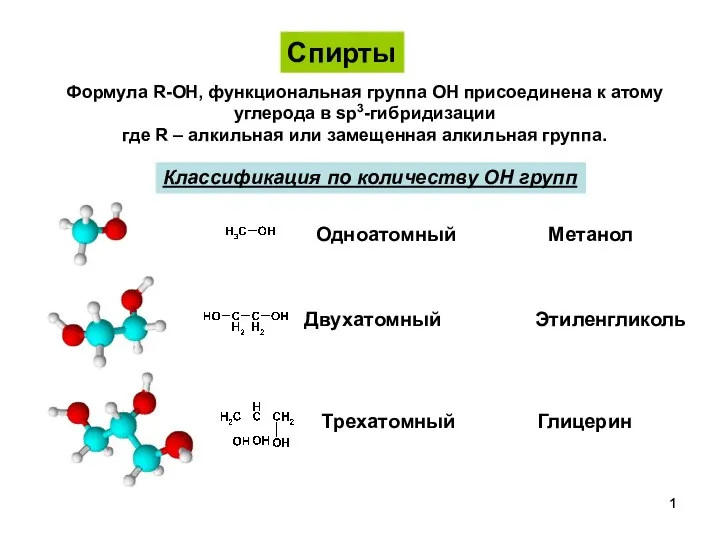 СпиртыПростыеЭфиры-1
СпиртыПростыеЭфиры-1 Растворы. Вычисление массовой доли растворенного вещества в растворе. Урок для 8-го класса
Растворы. Вычисление массовой доли растворенного вещества в растворе. Урок для 8-го класса Стоматологические материалы на основе полимеров
Стоматологические материалы на основе полимеров Кінетика хімічних реакцій і хімічна рівновага
Кінетика хімічних реакцій і хімічна рівновага Метанол, етанол та їхнє застосування
Метанол, етанол та їхнє застосування Особенности лантаноидов и актиноидов
Особенности лантаноидов и актиноидов Химия в строительстве
Химия в строительстве Углерод
Углерод Второе начало термодинамики и его применимость к биосистемам. Химическое равновесие. (Лекция 05)
Второе начало термодинамики и его применимость к биосистемам. Химическое равновесие. (Лекция 05) Основы органической химии
Основы органической химии Аминокислоты 2
Аминокислоты 2 Правила роботи на уроці
Правила роботи на уроці Коррозия металлов
Коррозия металлов