Слайд 2
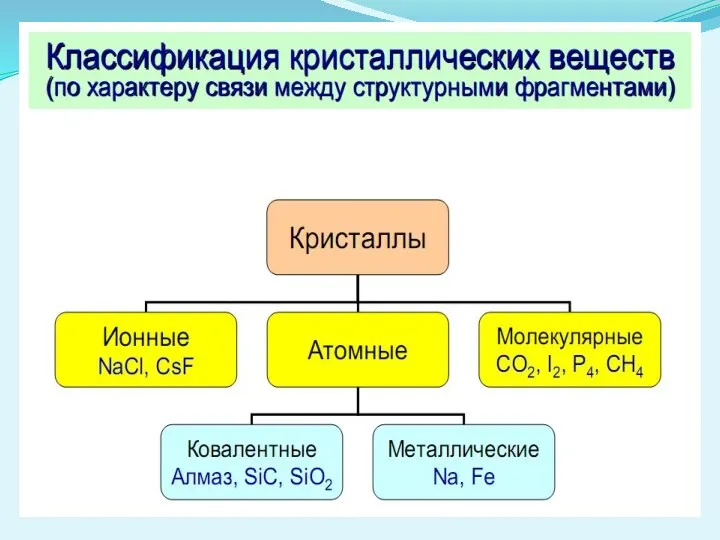
Слайд 3
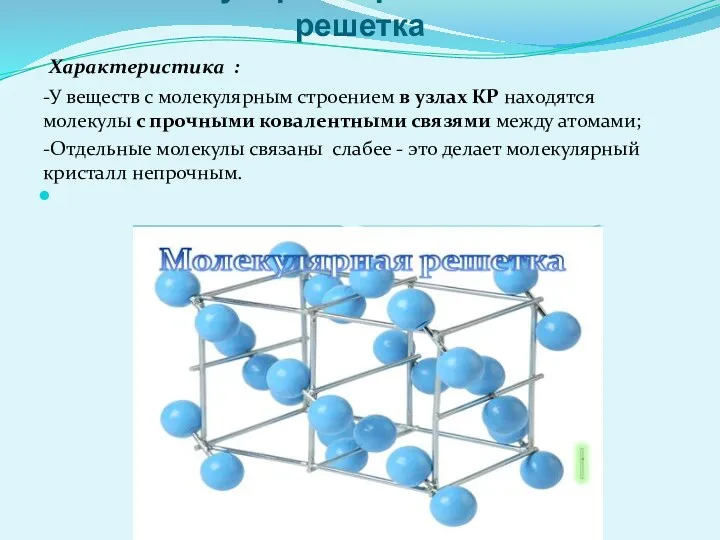
1. Молекулярная кристаллическая решетка
Характеристика :
-У веществ с молекулярным
строением в узлах КР находятся молекулы с прочными ковалентными связями между атомами;
-Отдельные молекулы связаны слабее - это делает молекулярный кристалл непрочным.
Слайд 4
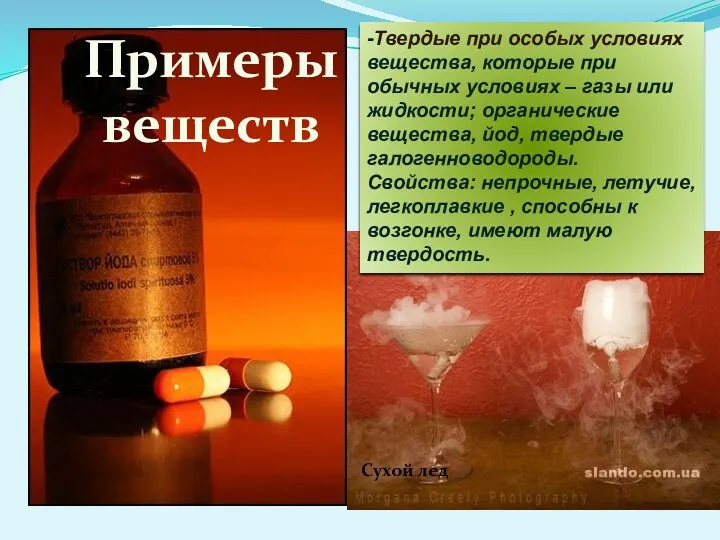
Примеры веществ
Сухой лед
-Твердые при особых условиях вещества, которые при обычных условиях
– газы или жидкости; органические вещества, йод, твердые галогенноводороды.
Свойства: непрочные, летучие, легкоплавкие , способны к возгонке, имеют малую твердость.
Слайд 5
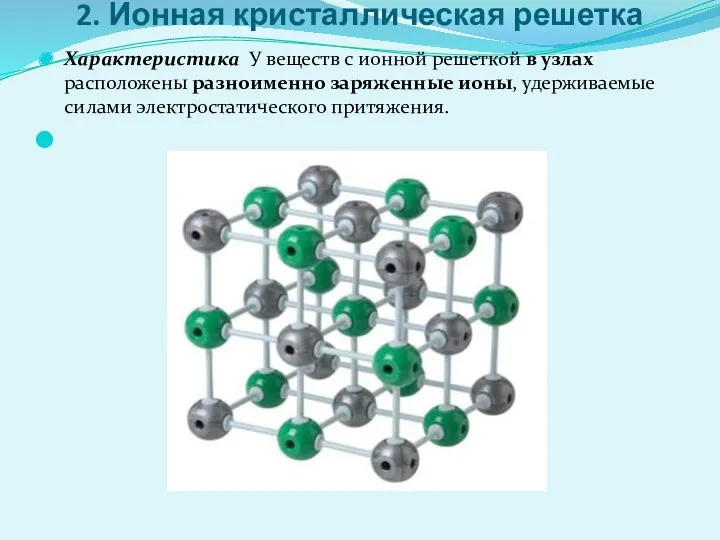
2. Ионная кристаллическая решетка
Характеристика У веществ с ионной решеткой в узлах
расположены разноименно заряженные ионы, удерживаемые силами электростатического притяжения.
Слайд 6

Примеры веществ
Соли, оксиды и гидроксиды типичных металлов
Свойства
Твердые, прочные, нелетучие, тугоплавкие
Слайд 7

3. Атомная кристаллическая решетка
Характеристика : В узлах атомной КР находятся атомы,
связанные прочными ковалентными связями в протяженную пространственную сеть. В этом случае структура отличается таким внутренним единством, что можно сказать, что весь кристалл представляет одну молекулу.
Слайд 8

Примеры веществ и свойства
Алмаз, кварц.
Свойства:
Те же, что и для ионной решетки,
но часто в превосходной степени – очень твердые, очень прочные и т.д.
Слайд 9
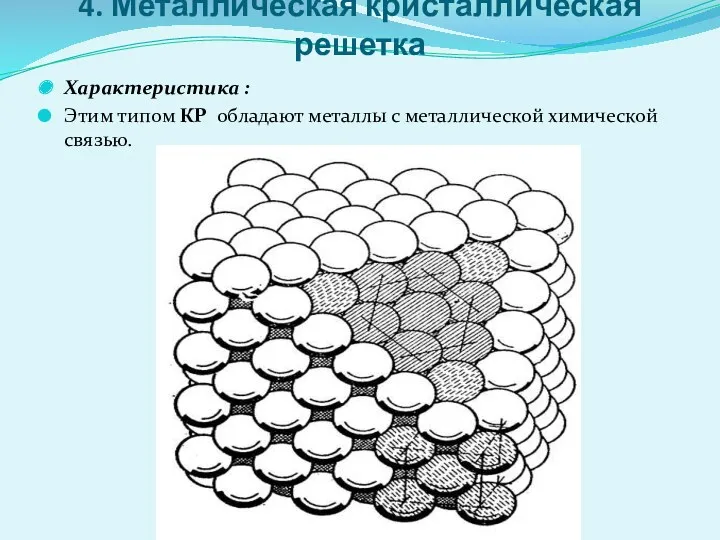
4. Металлическая кристаллическая решетка
Характеристика :
Этим типом КР обладают металлы с
металлической химической связью.
Слайд 10

Примеры веществ и свойства
Металлы и сплавы. Свойства:
-ковкие,
-пластичные,
-электро- и
-теплопроводные,
-имеют металлический блеск
Слайд 11
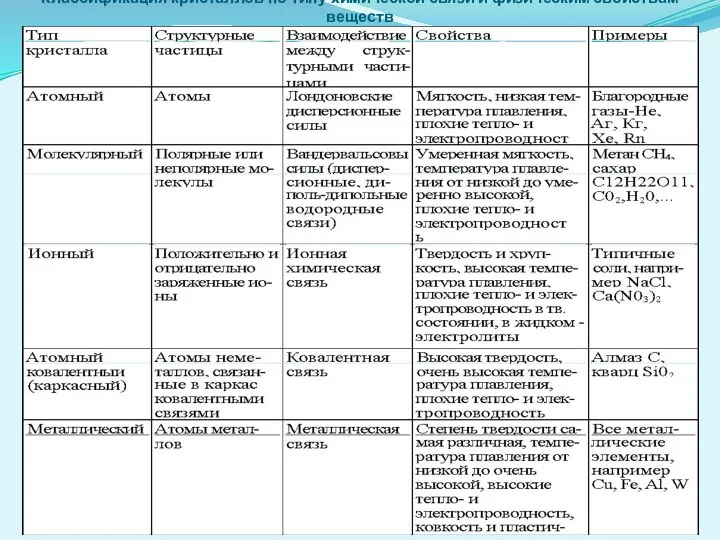
Классификация кристаллов по типу химической связи и физическим свойствам веществ
Слайд 12
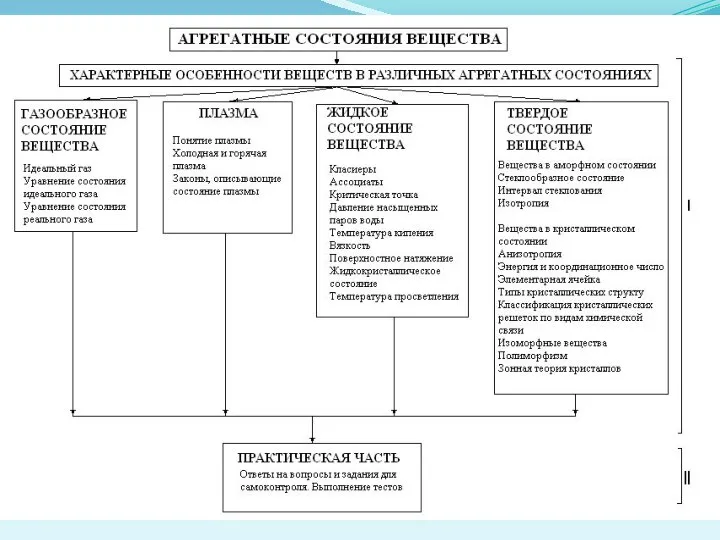
Слайд 13

1. Вид частиц в ионной решетке:
а) ионы
в) молекулы
б) атомы
г) атом-ионы
Слайд 14

2. Характер химической связи в атомной решетке:
а) металлическая
в) ионная
б) ковалентная
г) силы межмолекулярного взаимодействия
Слайд 15

3. Прочность связи в молекулярной решетке
а) очень прочная
в) слабая
б)
прочная
г) разной прочности
Слайд 16

4. Агрегатное состояние у веществ с ионной решеткой:
а) твердые
в) жидкие
б)
газы
Слайд 17

5. Вещества без определенной температуры плавления и закономерного расположения частиц называются:
а)
кристаллические
б) аморфные
Слайд 18

6. Очень тугоплавкими являются вещества с решеткой:
а) металлической
в) атомной
б) молекулярной
г) ионной
Слайд 19

7. Пластичностью обладают вещества с:
а) металлической
в) молекулярной
б) ионной
г)
атомной
Слайд 20

7. Пластичностью обладают вещества с:
а) металлической
в) молекулярной
б) ионной
г)
атомной
Слайд 21

8. Кремний имеет решетку:
а) молекулярную
в) ионную
б) атомную
г) металлическую
Слайд 22

9. Щелочи имеют решетку:
а) молекулярную
в) ионную
б) металлическую
г) атомную
Слайд 23

Повторение
Определите вид химической связи, составьте электронные формулы образования веществ: NH3, Li3N,
Cl2, Na2S, H2S, Mg.
Химическая связь ионная и ковалентная полярная в соединениях соответственно
1) сероводород и фторид серы (VI)
2) сульфид фосфора (V) и оксид натрия
3) хлорид рубидия и вода
4) оксид серы (IV) и кислород
В аммиаке и хлориде бария химическая связь соответственно
1) ионная и ковалентная полярная
2) ковалентная полярная и ионная
3) ковалентная неполярная и металлическая
4) ковалентная неполярная и ионная
Атомную кристаллическую решётку имеет
1) метан 3) кислород
2) водород 4) кремний






















 Газовые законы для идеальных и реальных газов. Лекция 1
Газовые законы для идеальных и реальных газов. Лекция 1 Фотоэлектрические и информационные свойства фоточувствительных карбазолилсодержащих олигомерных пленочных композитов
Фотоэлектрические и информационные свойства фоточувствительных карбазолилсодержащих олигомерных пленочных композитов Ископаемые углеводороды
Ископаемые углеводороды Методы прямого секвенирования белков (пептидов)
Методы прямого секвенирования белков (пептидов) Неметаллы. Обобщающий урок. 9 класс
Неметаллы. Обобщающий урок. 9 класс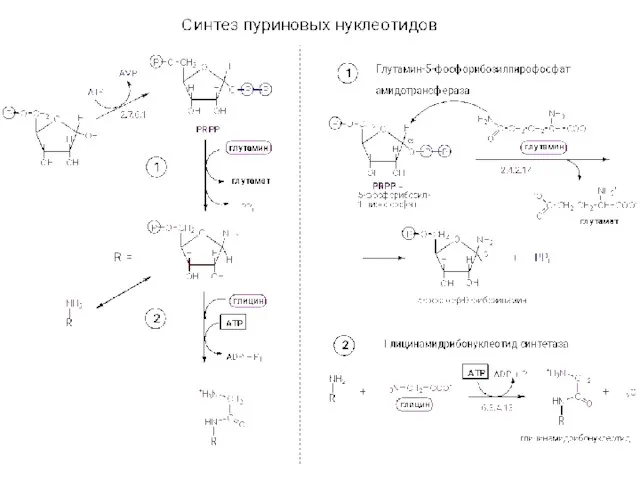 Синтез нуклеотидов
Синтез нуклеотидов Методы пробоотбора воздуха. Лекция 2
Методы пробоотбора воздуха. Лекция 2 Химическая стойкость тугоплавких металлов в различных реагентах
Химическая стойкость тугоплавких металлов в различных реагентах Соединения углерода
Соединения углерода The chemistri of life and the micro universe
The chemistri of life and the micro universe Определение химического элемента на основании расчетов по химическим реакциям
Определение химического элемента на основании расчетов по химическим реакциям Классификация органических соединений. Урок химии в 10 классе
Классификация органических соединений. Урок химии в 10 классе Теория радикалов (30 гг. XIX в Й.Берцелиус, Ю.Либих, Ж.Дюма)
Теория радикалов (30 гг. XIX в Й.Берцелиус, Ю.Либих, Ж.Дюма) Химическое равновесие. Азот и Фосфор. 9 класс
Химическое равновесие. Азот и Фосфор. 9 класс Миграция химических элементов (геохимическая миграция)
Миграция химических элементов (геохимическая миграция) Вычисление массы растворённого вещества, содержащегося в определённой массе раствора с известной массовой долей
Вычисление массы растворённого вещества, содержащегося в определённой массе раствора с известной массовой долей Кислородсодержащие соединения. Ароматические соединения
Кислородсодержащие соединения. Ароматические соединения Серная кислота
Серная кислота Трансмиссионные масла
Трансмиссионные масла Хімічні властивості кислот
Хімічні властивості кислот Неметаллы: атомы и простые вещества. Воздух. Кислород. Озон
Неметаллы: атомы и простые вещества. Воздух. Кислород. Озон Комплексные соединения
Комплексные соединения Кислоты в свете теории электролитической диссоциации (ТЭД), 8 класс
Кислоты в свете теории электролитической диссоциации (ТЭД), 8 класс Аналитическая химия. Предмет и задачи
Аналитическая химия. Предмет и задачи Теория электрической диссоциации
Теория электрической диссоциации NaOH. Гидроксид натрия
NaOH. Гидроксид натрия Углеводы Cn(H2O)m
Углеводы Cn(H2O)m Ансамбль пор в реальном твердом теле
Ансамбль пор в реальном твердом теле