Слайд 2

В кожному рядку виберіть речовину,яка відрізняється від двох інших.Вкажіть ознаку відмінності:
1)CaO, H2SO4, HCL
2)NaOH, MgCl2, Ca(OH)2
3)KOH, Ba(OH)2, Cu(OH)2
4)H2CO3, H2SO3, HNO3
Слайд 3
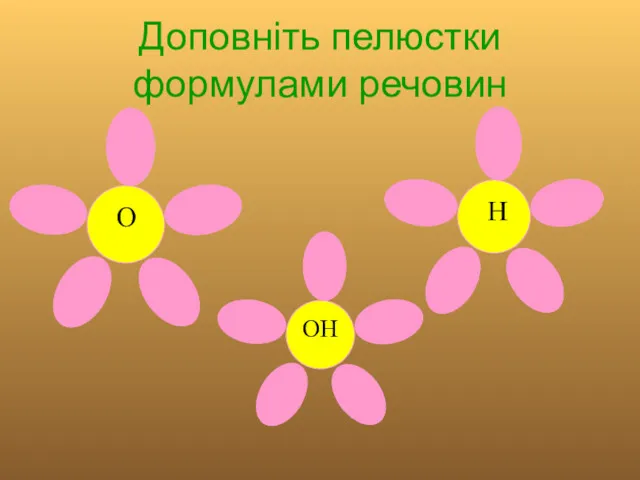
Доповніть пелюстки формулами речовин
Слайд 4
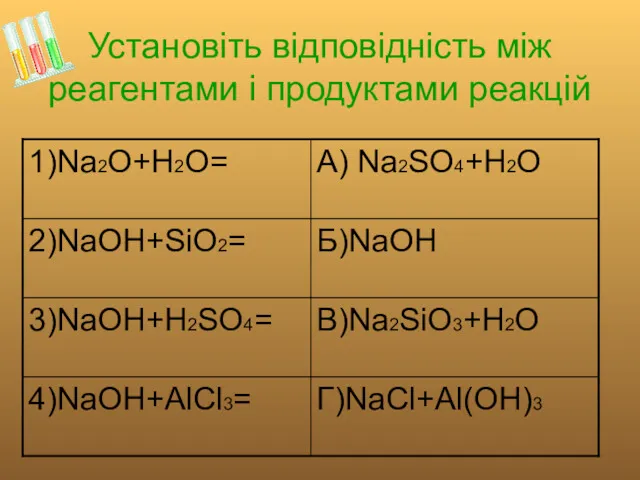
Установіть відповідність між реагентами і продуктами реакцій
Слайд 5

Вказати пропущені формули речовин у схемах хімічних перетворень:
1)… + HCl =>
CuCl2 + H2O
2)Mg(OH)2 + … => MgSO4 + H2O
3)K2O + H2SO4 =>… + H2O
4)Al(OH)3 =>… + H2O
Слайд 6

На запропоновані твердження дайте відповідь:
Так
Ні
Слайд 7

Слайд 8

Слайд 9

Тема уроку:
Хімічні властивості кислот
Слайд 10

Завдання уроку:
Розглянути хімічні властивості кислот;
Розвивати вміння застосовувати одержані знання в повсякденному
житті.
Слайд 11

“Має значення тільки те знання,яке використовується на практиці.”
Гордон Драйден
Слайд 12

Неухильно дотримуйтесь правил техніки безпеки при роботі з кислотами!
Слайд 13
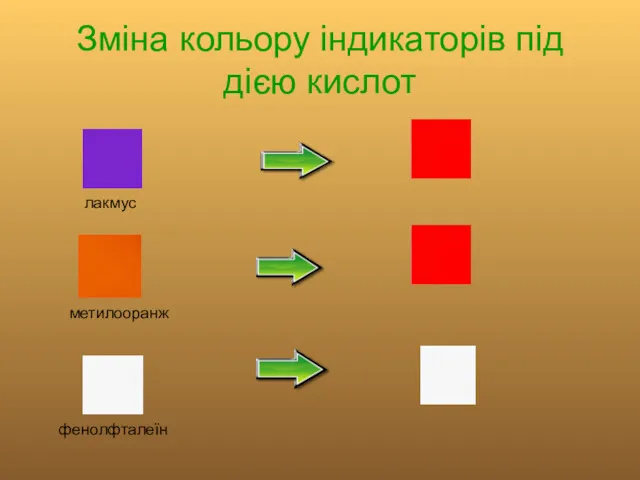
Зміна кольору індикаторів під дією кислот
лакмус
метилооранж
фенолфталеїн
Слайд 14

Роберт Бойл
(25.01.1627-30.12.1691)
Англійський хімік,фізик і філософ.
Слайд 15

Слайд 16

Слайд 17

Лакмус був відомий ще у Давньому Єгипті та Давньому Римі
Слайд 18

В харчовій промисловості визначають кислотність продукту
Слайд 19

На підприємствах кислотність визначають у такій продукції
Слайд 20

Кислотність грунтів впливає на врожайність
Слайд 21

Ряд активності металів
K Na Mg Al Zn Fe Ni Sn Pb(H2)Cu
Ag Hg Pt Au
М.М.Бекетов
Слайд 22

Слайд 23

Син М.М.Бекетова – Олексій, відомий архітектор,який створив архітектурний обік сучасного Харкова
Слайд 24

Назвіть шлях,який складають метали,що не витісняють водень з розчинів кислот
Слайд 25
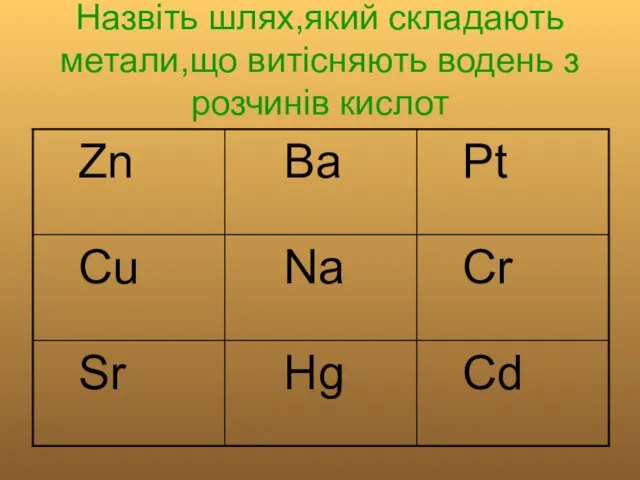
Назвіть шлях,який складають метали,що витісняють водень з розчинів кислот
Слайд 26

Допишіть рівняння можливих реакцій:
1)Mn + HCl =>
2)Cd + H2SO4 =>
3)Au
+ HI =>
4)Al + HBr =>
5)Hg + HCl =>
Слайд 27
Ніобій і тантал – метали хірургів
Слайд 28

Розв’язати задачу:
Яка маса залізного виробу може розчинитися в шлунковому сокові крокодила,якщо
в ньому міститься 3,65 г хлоридної кислоти?
Слайд 29

Слайд 30

Слайд 31

Засіб для лікування печії
Слайд 32

Яким буде забарвлення лакмусу в кислоті?
А)синім
Б)червоним
В)фиолетовим
Слайд 33

В яких випадках буде виділятися водень:
А)Zn + HCl =>
Б)Ag +
H2SO4 =>
В)Cu + H3PO4 =>
Слайд 34

Прізвище вченого,який вперше відкрив індикатори:
А)М.М.Бекетов
Б)Д.І.Менделєєв
В)Р.Бойль
Слайд 35

Вибрати реакцію заміщення:
А)MgO + 2HCl = MgCl2+H2O
Б)Zn+H2SO4=ZnSO4+ H2
В)Ca(OH)2+2HBr=CaBr2+2H2O
Слайд 36

Вибрати реакцію нейтралізації:
А)3KOH+H3PO4=K3PO4+3H2O
Б)Fe+2HCL=FeCl2+H2
В)Al2O3+6HBr=2AlBr3+3H2O
Слайд 37

Вкажіть метал,який не взаємодіє з розчином кислоти:
А)ртуть
Б)кальцій
В)марганець
Слайд 38

Картини стародавніх майстрів мають темну палітру,бо під дією H2S,що є у
повітрі,свинцеві білила перетворювалися на чорну сполуку PbS
Слайд 39

Допоможіть митцям добути цинкові білила в хімічній лабораторії за поданою схемою
Zn=>ZnCl2=>Zn(OH)2=>ZnO
Слайд 40

Домашнє завдання
Вивчити параграф 12
Письмово:
№112,114(рівняння реакцій),
№117(розв’язати задачу)







































 Химические свойства металлов
Химические свойства металлов Золото. Что о нём мы можем рассказать?
Золото. Что о нём мы можем рассказать? d-элементы
d-элементы Подготовка к ВПР по химии. 11 класс
Подготовка к ВПР по химии. 11 класс Метаболизм кетоновых тел. Метаболизм холестерина
Метаболизм кетоновых тел. Метаболизм холестерина Химический потенциал. Фазовые равновесия
Химический потенциал. Фазовые равновесия Кислотные дожди
Кислотные дожди The Molecules of Life
The Molecules of Life Цинк и его соединения
Цинк и его соединения Фосфор и его соединения
Фосфор и его соединения Химия воды
Химия воды Закономірності протікання хімічних реакцій
Закономірності протікання хімічних реакцій Классификация химических элементов
Классификация химических элементов Способы выражения состава раствора. Задача 7
Способы выражения состава раствора. Задача 7 НЮ 2.1.1. Металлы - общая характеристика
НЮ 2.1.1. Металлы - общая характеристика Гониометрическое исследование кристаллов
Гониометрическое исследование кристаллов Сплавы железа с углеродом: стали и чугуны
Сплавы железа с углеродом: стали и чугуны Багатоатомні насичені спирти. Фізичні та хімічні властивості. Добування і застосування
Багатоатомні насичені спирти. Фізичні та хімічні властивості. Добування і застосування Мінерали та гірські породи
Мінерали та гірські породи Серная кислота
Серная кислота Electrolysis
Electrolysis Вещества
Вещества Карбон қышқылдары, жіктелуі, сипаттамалары, таралуы
Карбон қышқылдары, жіктелуі, сипаттамалары, таралуы Аминокислоты 2
Аминокислоты 2 Метаболизм углеводов
Метаболизм углеводов Спектральные методы: атомная спектроскопия
Спектральные методы: атомная спектроскопия Валентность и степень окисления. Химическая связь
Валентность и степень окисления. Химическая связь Альдегіди. Карбонові кислоти. Одержання. Фізичні та хімічні властивості
Альдегіди. Карбонові кислоти. Одержання. Фізичні та хімічні властивості