Содержание
- 2. Аминокислоты Аминокисло́ты (аминокарбо́новые кисло́ты) — органические соединения, в молекуле которых одновременно содержатся карбоксильные и аминные группы.
- 3. Аминокислоты Аминокислоты могут рассматриваться как производные карбоновых кислот, в которых один или несколько атомов водорода заменены
- 4. Протеиногенные аминокислоты В процессе биосинтеза белка в полипептидную цепь включаются 20 протеиногенных, или стандартных α-аминокислот, кодируемых
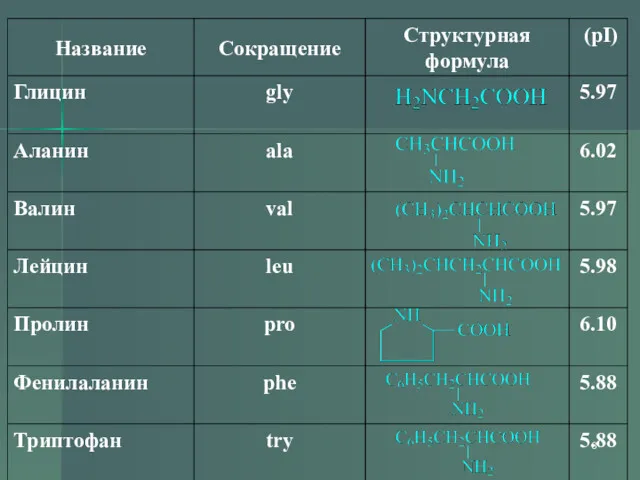
- 5. Классификация По радикалу Неполярные: глицин, аланин, валин, изолейцин, лейцин, пролин, метионин, фенилаланин, триптофан, Полярные незаряженные (заряды
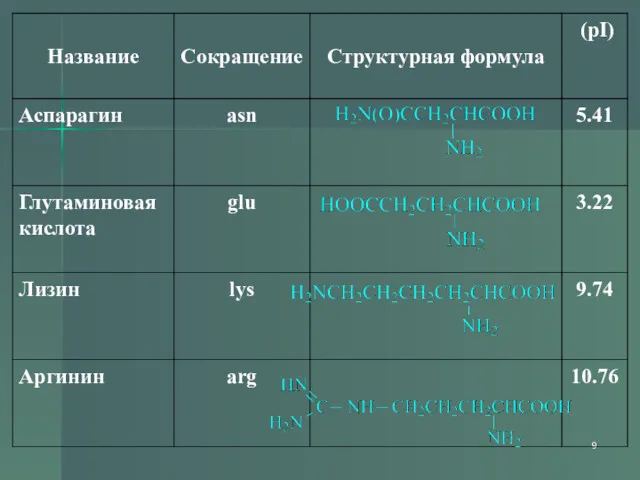
- 6. Классификация По функциональным группам Алифатические Моноаминомонокарбоновые: глицин, аланин, валин, изолейцин, лейцин Оксимоноаминокарбоновые: серин, треонин Моноаминодикарбоновые: аспартат,
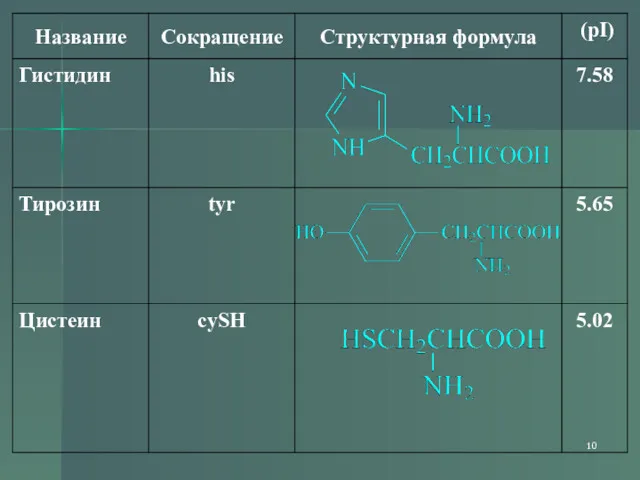
- 7. Классификация По функциональным группам Диаминомонокарбоновые: лизин, аргинин, несут в растворе положительный заряд Серосодержащие: цистеин, метионин Ароматические:
- 11. Незаменимые аминокислоты Незаменимыми называются аминокислоты, которые не могут быть синтезированы организмом из веществ, поступающих с пищей,
- 12. Незаменимые аминокислоты Следующие аминокислоты принято считать незаменимыми для организма человека: Лизин, Метионин, Фенилаланин, Триптофан, Треонин, Лейцин,
- 13. Для запоминания десяти незаменимых аминокислот существует мнемоническое правило: Лиза Метнула Фен в Трибуну, Трезвый Лейтенант Валялся
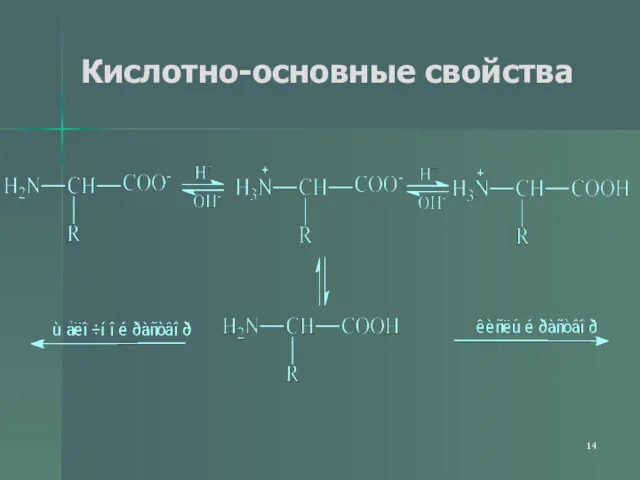
- 14. Кислотно-основные свойства
- 15. Кислотно-основные свойства не ионная форма; идеализированная аминокислота цвиттер-ион; аминокислота в твердом состоянии
- 16. Изоэлектрическая точка (рI) Изоэлектрической точкой называется такое значение pH, имеющее определенное значение для каждой аминокислоты, при
- 17. Способы получения аминокислот Аминирование α-галогензамещенных кислот
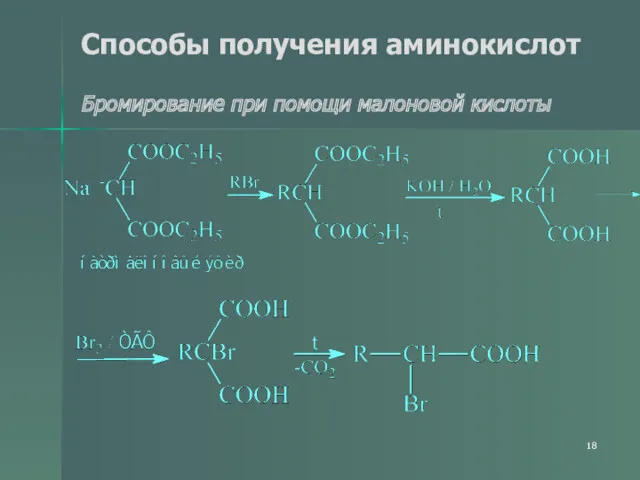
- 18. Способы получения аминокислот Бромирование при помощи малоновой кислоты
- 19. Способы получения аминокислот Синтез Штреккера–Зелинского
- 20. Способы получения аминокислот Алкилирование N-замещенных аминомалоновых эфиров Аминирование эфиров α-галоген-замещенных кислот (с помощью фталимида калия)
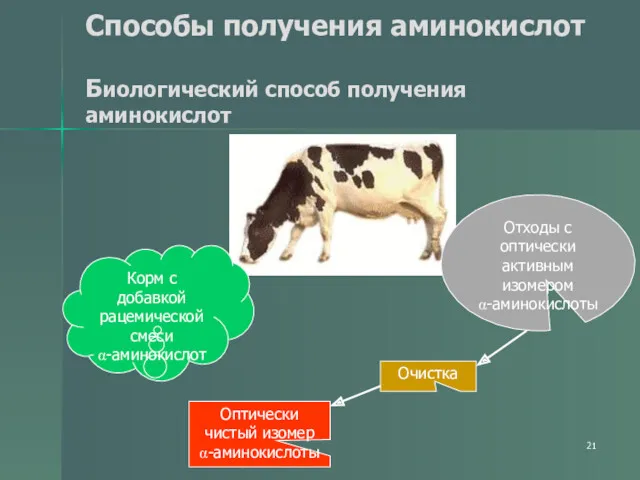
- 21. Способы получения аминокислот Биологический способ получения аминокислот Корм с добавкой рацемической смеси α-аминокислот Отходы с оптически
- 22. Химические свойства аминокислот Реакции аминогруппы Метод Ван-Слайка
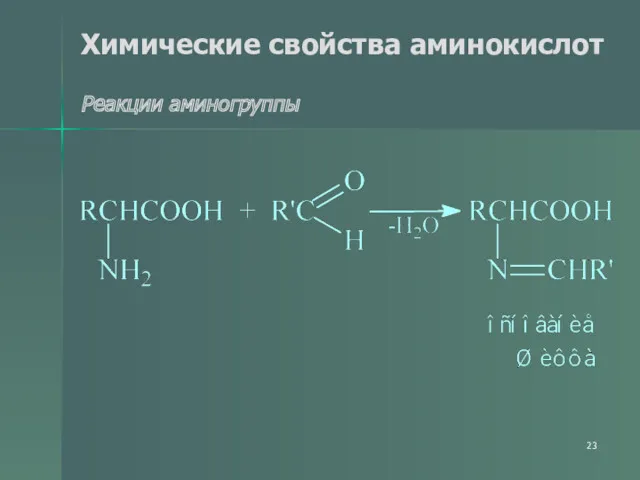
- 23. Химические свойства аминокислот Реакции аминогруппы
- 24. Химические свойства аминокислот Реакции карбоксильной группы
- 25. Химические свойства аминокислот Реакции карбоксильной группы
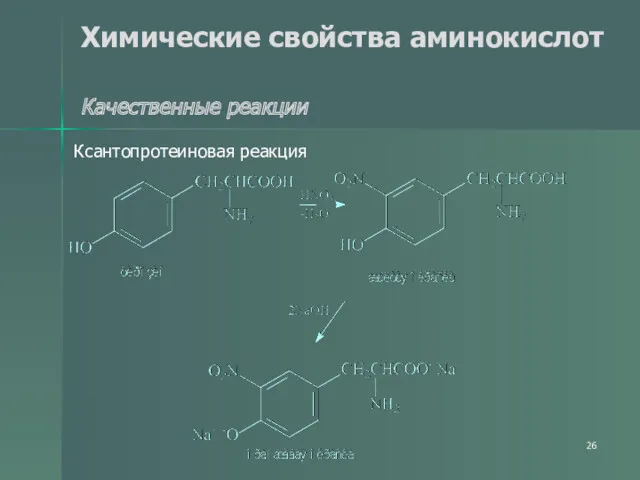
- 26. Химические свойства аминокислот Качественные реакции Ксантопротеиновая реакция
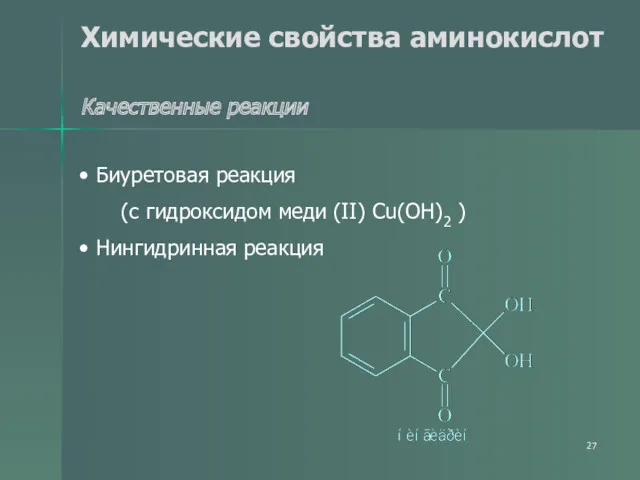
- 27. Химические свойства аминокислот Качественные реакции Биуретовая реакция (с гидроксидом меди (II) Cu(OH)2 ) Нингидринная реакция
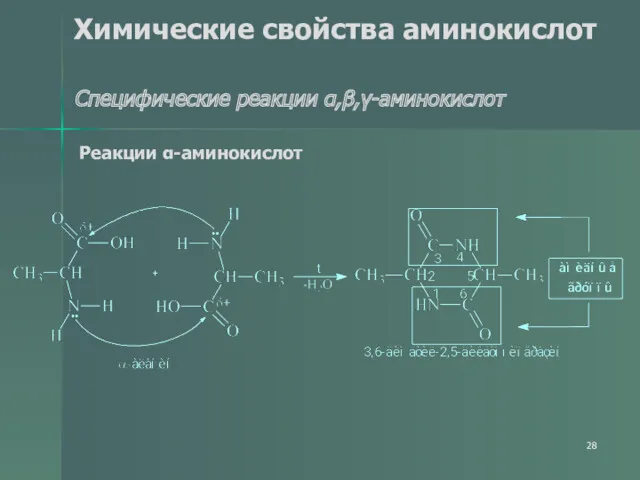
- 28. Химические свойства аминокислот Специфические реакции α,β,γ-аминокислот Реакции α-аминокислот
- 29. Химические свойства аминокислот Специфические реакции α,β,γ-аминокислот Реакции β-аминокислот
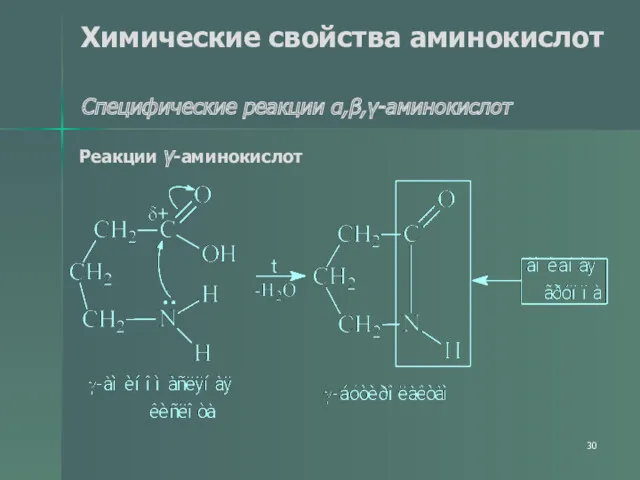
- 30. Химические свойства аминокислот Специфические реакции α,β,γ-аминокислот Реакции γ-аминокислот
- 31. Пептиды и белки Пептиды — соединения, построенные из нескольких остатков α-аминокислот, связанных амидной (пептидной) связью.
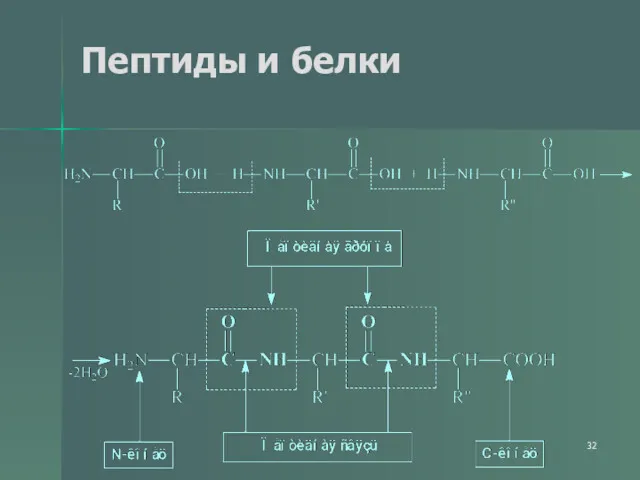
- 32. Пептиды и белки
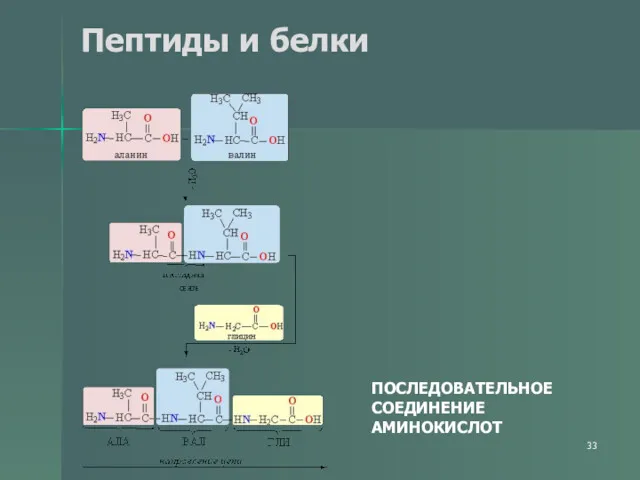
- 33. Пептиды и белки ПОСЛЕДОВАТЕЛЬНОЕ СОЕДИНЕНИЕ АМИНОКИСЛОТ
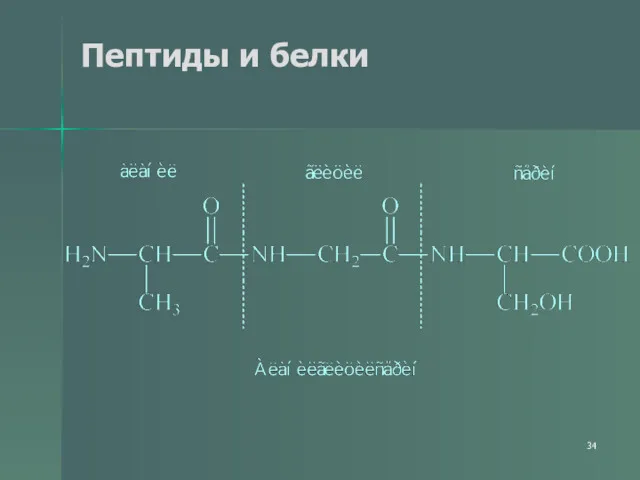
- 34. Пептиды и белки
- 35. Пептиды и белки Первичная структура белка инсулина.
- 36. Пептиды и белки Структура белков Первичная структура пептидов и белков — это последовательность аминокислотных остатков в
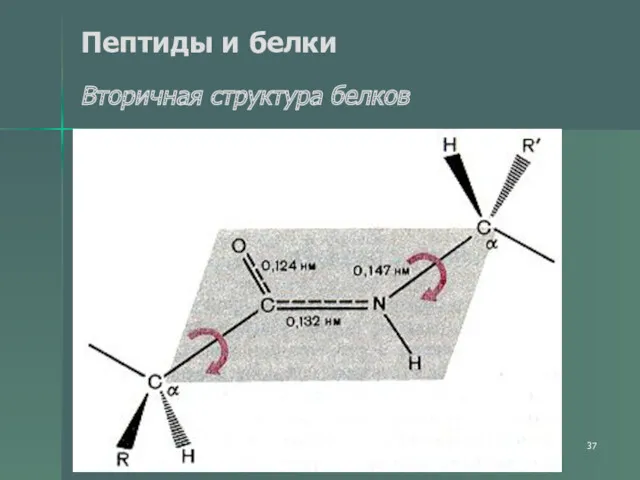
- 37. Пептиды и белки Вторичная структура белков
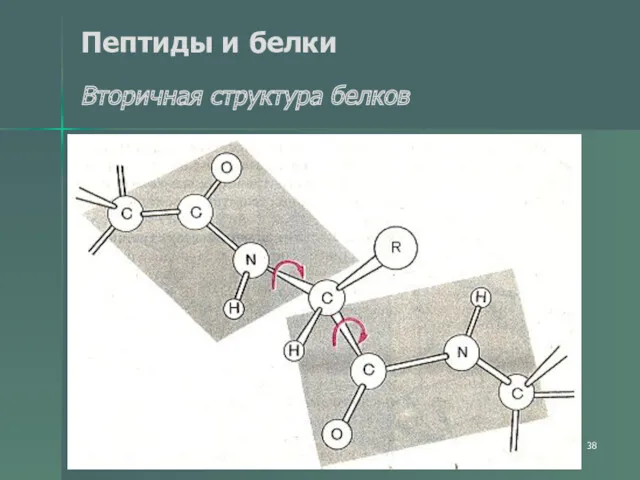
- 38. Пептиды и белки Вторичная структура белков
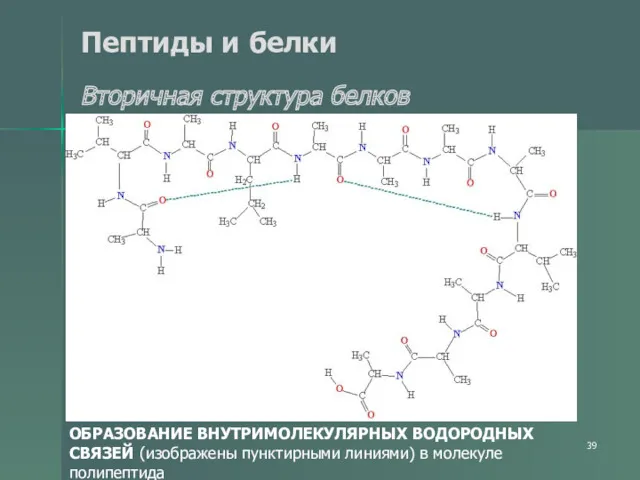
- 39. Пептиды и белки Вторичная структура белков ОБРАЗОВАНИЕ ВНУТРИМОЛЕКУЛЯРНЫХ ВОДОРОДНЫХ СВЯЗЕЙ (изображены пунктирными линиями) в молекуле полипептида
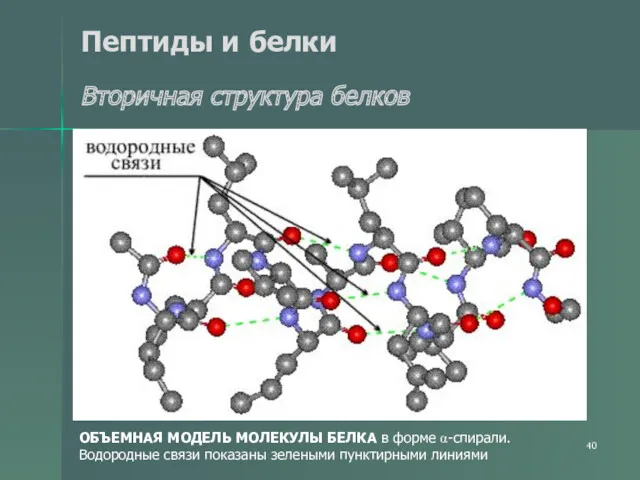
- 40. Пептиды и белки Вторичная структура белков ОБЪЕМНАЯ МОДЕЛЬ МОЛЕКУЛЫ БЕЛКА в форме α-спирали. Водородные связи показаны
- 41. Пептиды и белки Вторичная структура белков α-спираль молекулы белка
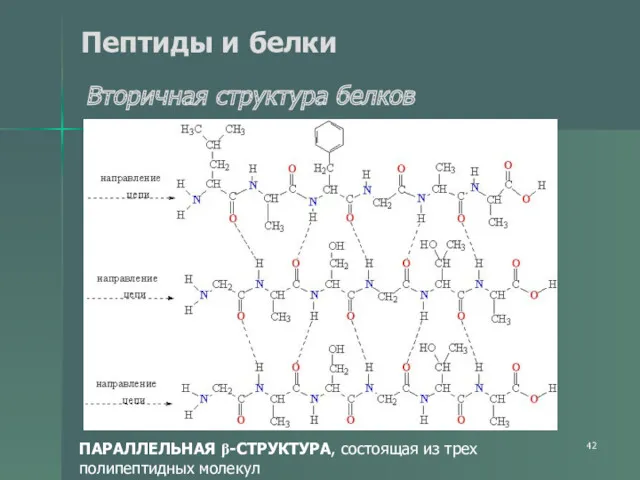
- 42. Пептиды и белки Вторичная структура белков ПАРАЛЛЕЛЬНАЯ β-СТРУКТУРА, состоящая из трех полипептидных молекул
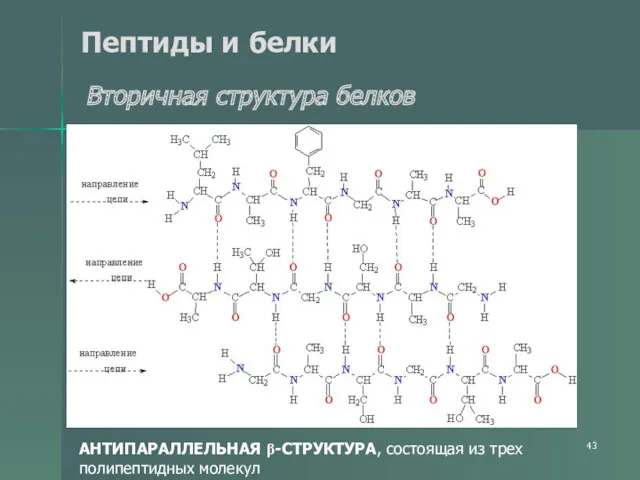
- 43. Пептиды и белки Вторичная структура белков АНТИПАРАЛЛЕЛЬНАЯ β-СТРУКТУРА, состоящая из трех полипептидных молекул
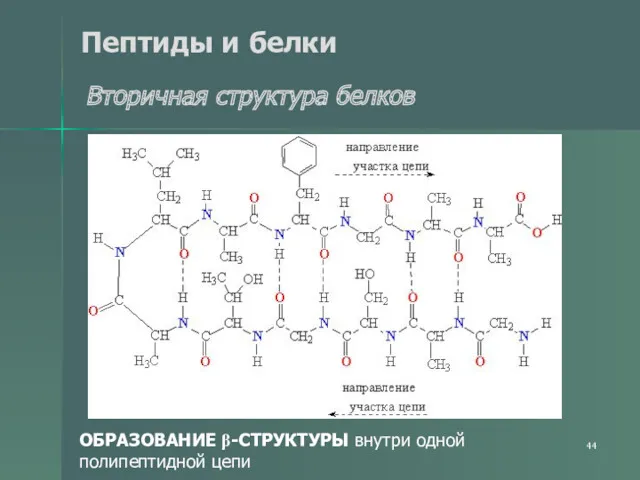
- 44. Пептиды и белки Вторичная структура белков ОБРАЗОВАНИЕ β-СТРУКТУРЫ внутри одной полипептидной цепи
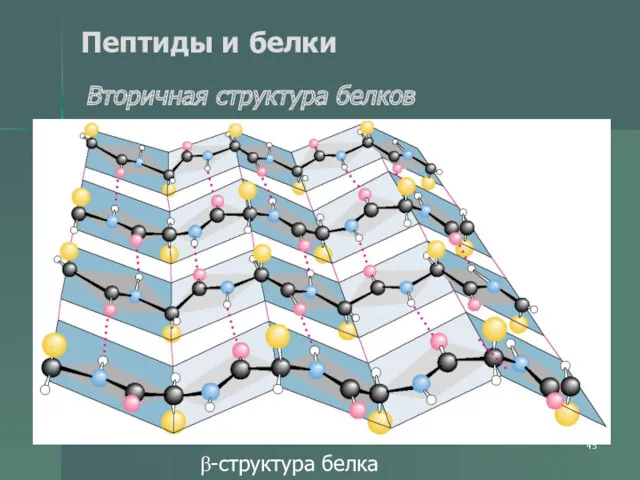
- 45. Пептиды и белки Вторичная структура белков β-структура белка
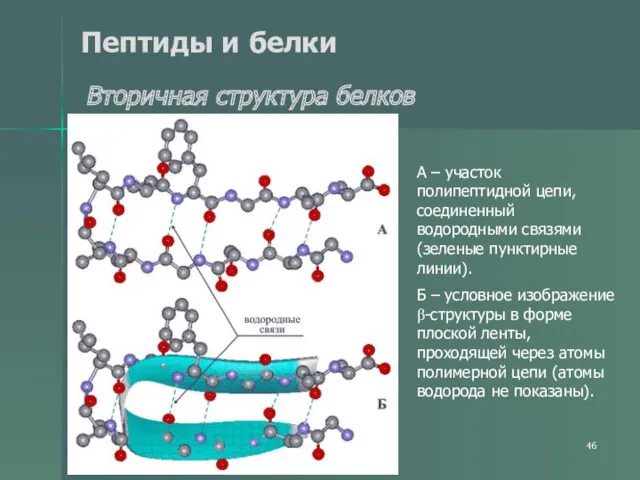
- 46. Пептиды и белки Вторичная структура белков А – участок полипептидной цепи, соединенный водородными связями (зеленые пунктирные
- 47. Пептиды и белки Вторичная структура белков Вторичная структура белка — это более высокий уровень структурной организации,
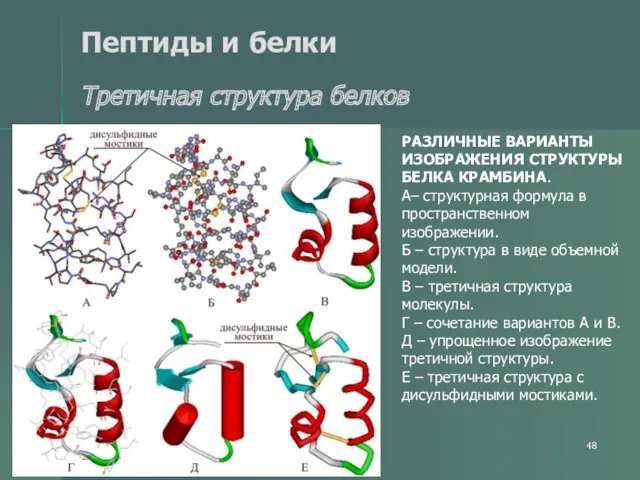
- 48. Пептиды и белки Третичная структура белков РАЗЛИЧНЫЕ ВАРИАНТЫ ИЗОБРАЖЕНИЯ СТРУКТУРЫ БЕЛКА КРАМБИНА. А– структурная формула в
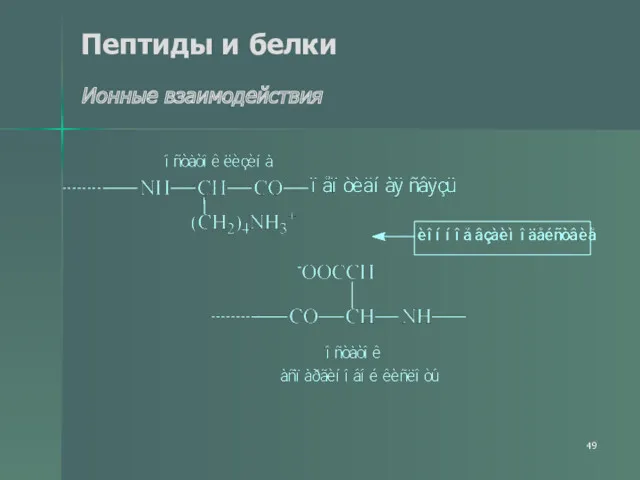
- 49. Пептиды и белки Ионные взаимодействия
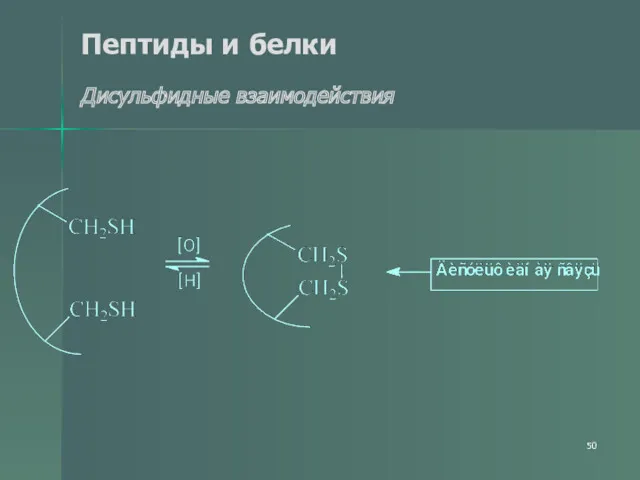
- 50. Пептиды и белки Дисульфидные взаимодействия
- 51. Пептиды и белки Глобулярные белки ГЛОБУЛЯРНАЯ СТРУКТУРА АЛЬБУМИНА (белок куриного яйца). В структуре помимо дисульфидных мостиков
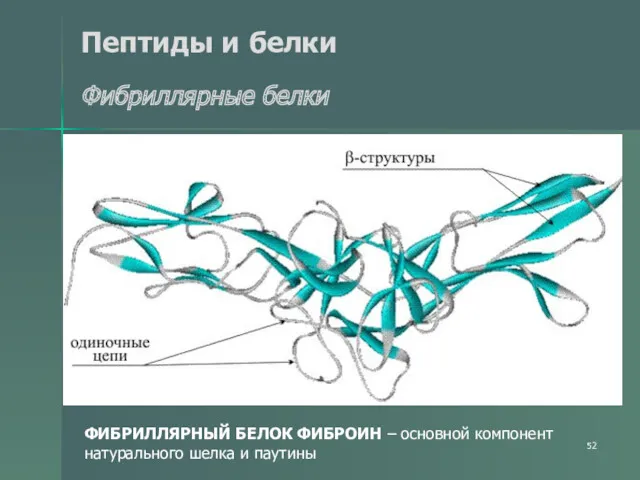
- 52. Пептиды и белки Фибриллярные белки ФИБРИЛЛЯРНЫЙ БЕЛОК ФИБРОИН – основной компонент натурального шелка и паутины
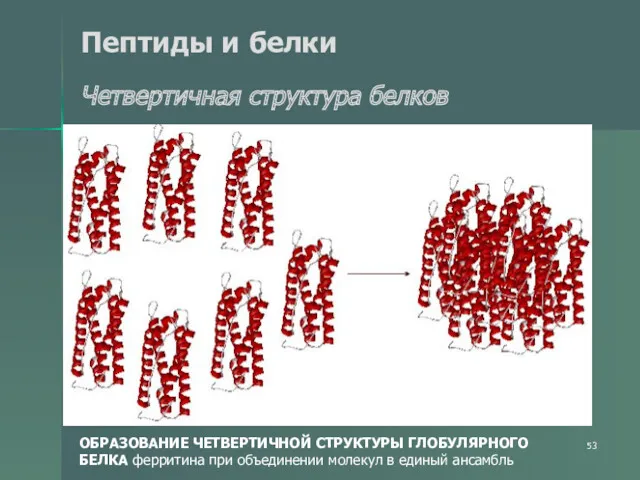
- 53. Пептиды и белки Четвертичная структура белков ОБРАЗОВАНИЕ ЧЕТВЕРТИЧНОЙ СТРУКТУРЫ ГЛОБУЛЯРНОГО БЕЛКА ферритина при объединении молекул в
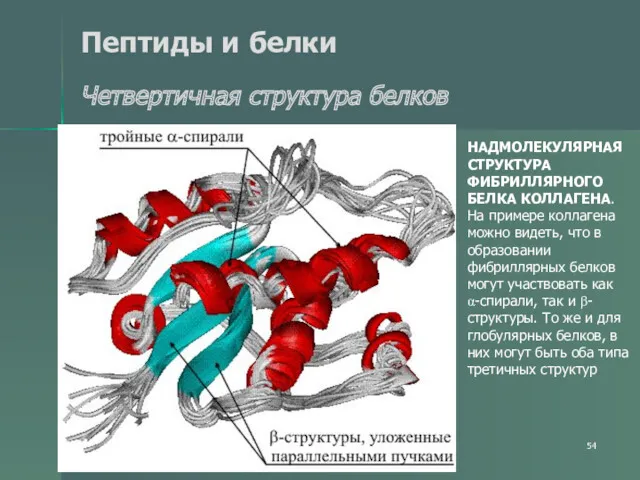
- 54. Пептиды и белки Четвертичная структура белков НАДМОЛЕКУЛЯРНАЯ СТРУКТУРА ФИБРИЛЛЯРНОГО БЕЛКА КОЛЛАГЕНА. На примере коллагена можно видеть,
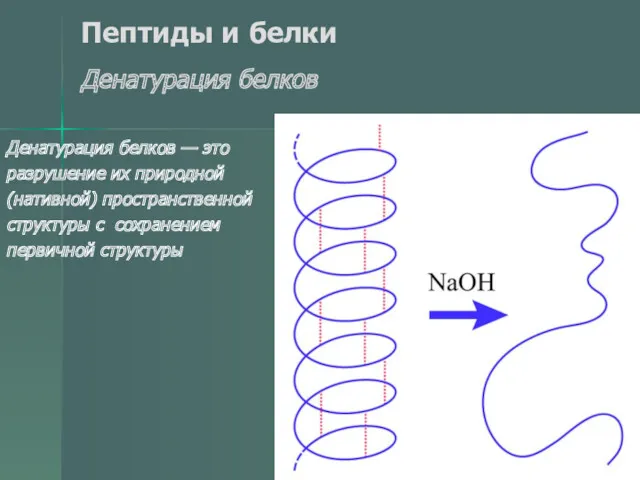
- 55. Пептиды и белки Денатурация белков Денатурация белков — это разрушение их природной (нативной) пространственной структуры с
- 57. Скачать презентацию
























 Полімери. Природні полімери
Полімери. Природні полімери Электролиз
Электролиз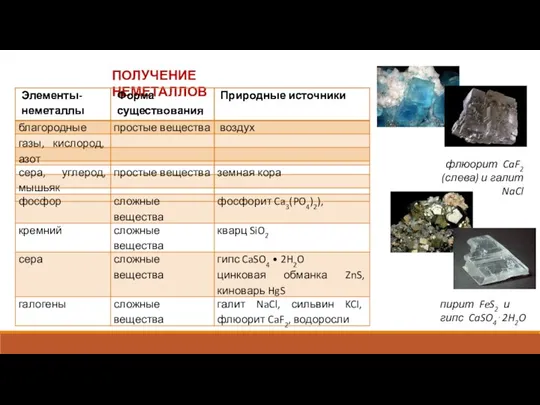 Получение неметаллов
Получение неметаллов Проблемный химический эксперимент как составная часть проблемного обучения химии
Проблемный химический эксперимент как составная часть проблемного обучения химии Химико-токсикологическое исследование отравлений отдельными лекарственными препаратами
Химико-токсикологическое исследование отравлений отдельными лекарственными препаратами Общие способы получения металлов
Общие способы получения металлов Основные синтетические полимеры
Основные синтетические полимеры Фосфонсірке қышқылының антипирендік қасиеттерін зерттеу
Фосфонсірке қышқылының антипирендік қасиеттерін зерттеу Гидролиз. Необратимый гидролиз
Гидролиз. Необратимый гидролиз От кулинарии — к кулинохимии
От кулинарии — к кулинохимии Основания. 8 класс
Основания. 8 класс Виды присадок к моторным топливам. Бензин
Виды присадок к моторным топливам. Бензин Марганец. Железо
Марганец. Железо Реакция Бэйлиса Хиллмана-Мориты
Реакция Бэйлиса Хиллмана-Мориты Измерение и оценка химического фактора. Лекция 9
Измерение и оценка химического фактора. Лекция 9 Реакции ионного обмена
Реакции ионного обмена Фенол. Состав молекулы фенола
Фенол. Состав молекулы фенола Количество вещества. 8 класс
Количество вещества. 8 класс Термические процессы нефтепереработки
Термические процессы нефтепереработки Метаболизм жирных кислот
Метаболизм жирных кислот Биологически активные вещества и их содержание в лекарственных растениях
Биологически активные вещества и их содержание в лекарственных растениях Высокомолекулярные соединения (ВМС) или полимеры
Высокомолекулярные соединения (ВМС) или полимеры Алкени і алкіни
Алкени і алкіни Живая» и «мёртвая» вода
Живая» и «мёртвая» вода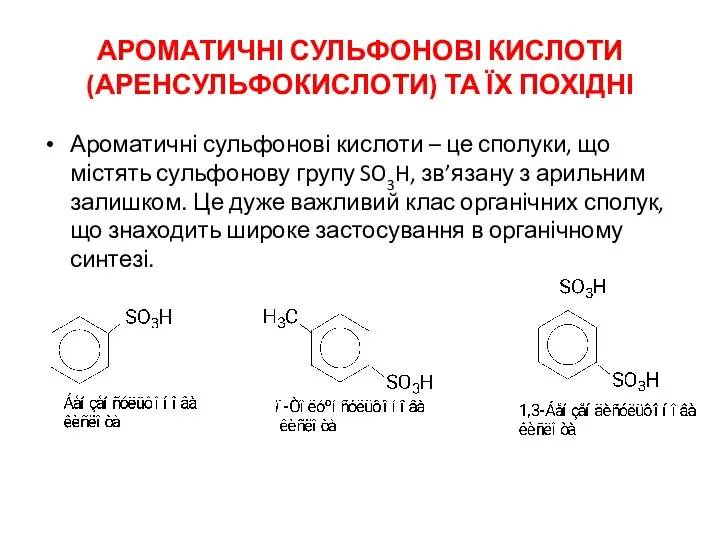 Ароматичні сульфонові кислоти (аренсульфокислоти) та їх похідні
Ароматичні сульфонові кислоти (аренсульфокислоти) та їх похідні Каталитический риформинг бензинов
Каталитический риформинг бензинов Подгруппа азота. 9 класс
Подгруппа азота. 9 класс Тайна великого открытия периодической таблицы
Тайна великого открытия периодической таблицы