Содержание
- 2. Элемент V группы главной подгруппы Элемент №7 типичный неметалл Элемент малого 2-ого периода +7 )2e )5e
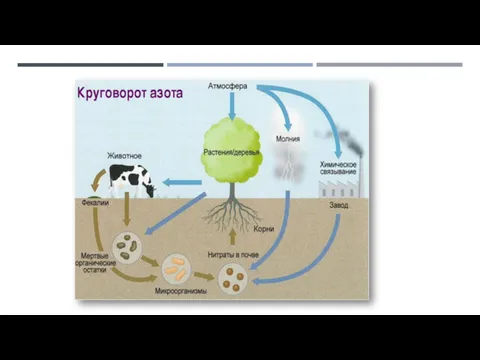
- 3. НАХОЖДЕНИЕ В ПРИРОДЕ По распространенности в земной коре азот занимает 17-е место, на его долю приходится
- 4. Азот присутствует во всех живых организмах (1-3% на сухую массу), являясь важнейшим биогенным элементом. Он входит
- 5. Молекула двухатомарная и очень прочная Структурная формула N N В нем молекулярная решетка и ковалентная неполярная
- 7. Азот — газ без цвета, запаха и вкуса. Мало растворим в воде (в 100 объемах воды
- 8. ХИМИЧЕСКИЕ СВОЙСТВА АЗОТА Азот реагирует с кислородом (при температуре электрической дуги) N2 + O2 =2NO 2.
- 9. ПОЛУЧЕНИЕ АЗОТА В ПРОМЫШЛЕННОСТИ: ФРАКЦИОННОЙ ПЕРЕГОНКОЙ ЖИДКОГО ВОЗДУХА ОАО «Невинномысский Азот" Завод по производству азота из
- 10. ПОЛУЧЕНИЕ АЗОТА В ЛАБОРАТОРИИ (РАЗЛОЖЕНИЕМ СОЛЕЙ АММОНИЯ) . Разложением нитрита аммония NH4NO2=N2 + 2H2O 2. Разложением
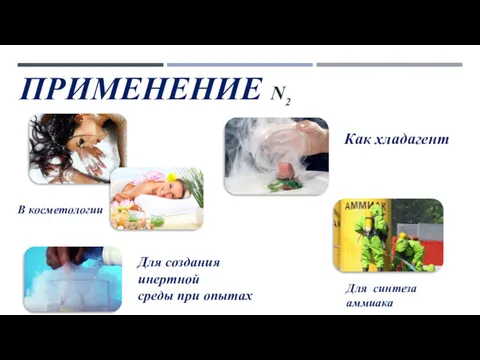
- 11. ПРИМЕНЕНИЕ N2 В косметологии Для создания инертной среды при опытах Как хладагент Для синтеза аммиака
- 13. Скачать презентацию








 Фенол қосылыстары
Фенол қосылыстары Антибиотики как ЛС
Антибиотики как ЛС Металлы и неметаллы
Металлы и неметаллы Основи. Гідроксиди Натрію і Кальцію
Основи. Гідроксиди Натрію і Кальцію Нобелевская премия по химии
Нобелевская премия по химии Высокоэффективная жидкостная хроматография
Высокоэффективная жидкостная хроматография Органические вещества
Органические вещества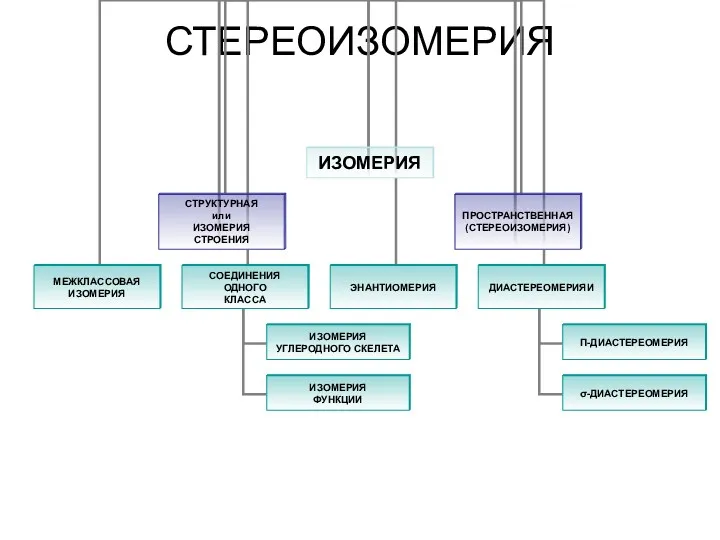 Стереоизомерия. Изомерия. Пространственная (стереоизомерия) углеродного скелета
Стереоизомерия. Изомерия. Пространственная (стереоизомерия) углеродного скелета Реакции ионного обмена в растворах электролитов. рH раствора как показатель кислотности среды
Реакции ионного обмена в растворах электролитов. рH раствора как показатель кислотности среды Вещества и их системы. Растворы. Массовая доля растворенного вещества. 11 класс
Вещества и их системы. Растворы. Массовая доля растворенного вещества. 11 класс Құймалар. Механикалық қоспа
Құймалар. Механикалық қоспа История развития и предмет исследования супрамолекулярной химии. Классификация супрамолекулярных соединений
История развития и предмет исследования супрамолекулярной химии. Классификация супрамолекулярных соединений Кремний и его соединения. Нахождение в природе
Кремний и его соединения. Нахождение в природе Реакция обменного разложения веществ водой - гидролиз
Реакция обменного разложения веществ водой - гидролиз Оксид серы(4). Сернистая кислота и её соли
Оксид серы(4). Сернистая кислота и её соли Кафедра химической технологии лекарственных веществ (ХТЛВ)
Кафедра химической технологии лекарственных веществ (ХТЛВ) Електролітична дисоціація
Електролітична дисоціація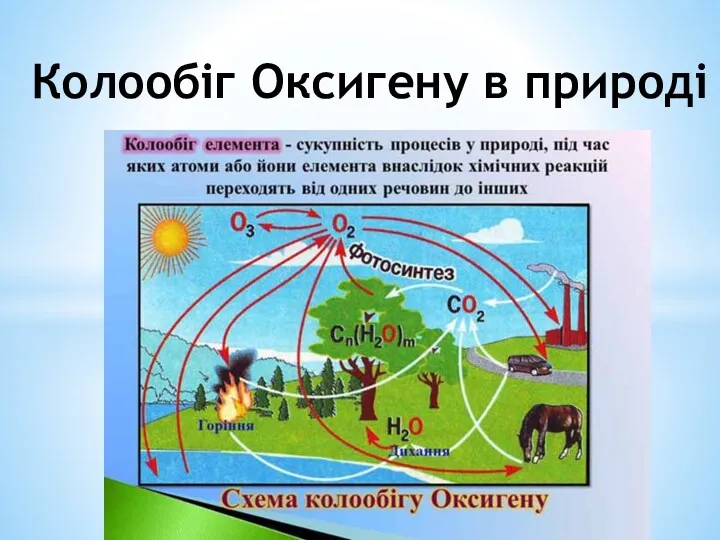 Колообіг оксигену в природі
Колообіг оксигену в природі Важнейшие реакции в органической химии
Важнейшие реакции в органической химии Хімія металургійних процесів. Теорія сплавів
Хімія металургійних процесів. Теорія сплавів Классификация химических реакций по механизму реакции
Классификация химических реакций по механизму реакции Көмірсутектер.Олардың жіктелуі, құрылысы,изомериясы және номенклатурасы
Көмірсутектер.Олардың жіктелуі, құрылысы,изомериясы және номенклатурасы Органическая химия. Этапы развития органической химии
Органическая химия. Этапы развития органической химии Элемент свинец Рb
Элемент свинец Рb Щелочи
Щелочи Спирты. Действие этанола на организм человека (10 класс)
Спирты. Действие этанола на организм человека (10 класс) Вирощування кристалів солей
Вирощування кристалів солей Термопластичные полимеры
Термопластичные полимеры