Слайд 2

Цель урока:
На этом уроке мы вспомним основные понятия этой темы;
Проведём опыты по испытанию веществ на электрическую проводимость и на признаки необратимых реакций;
Закрепим полученные знания, выполнив задания у доски.
Слайд 3

«Закончи предложение одним словом».
1. Положительнозаряженный электрод - ….
2. Отрицательнозаряженный электрод
- ….
3. Положительнозаряженные частицы -…
4. Отрицательнозаряженные частицы -…
5. Вещества, водные растворы или расплавы которых проводят электрический ток -…
6. Вещества, водные растворы или расплавы которых не проводят электрический ток -…
7. Процесс распада электролита на ионы при растворении или расплавлении вещества -…
8. Электролиты, при диссоциации которых в качестве катионов образуются только ионы водорода - …
9. Электролиты, при диссоциации образуются катионы металлов и анионы кислотных остатков - …
10. Электролиты, при диссоциации которых в качестве анионов образуются только гидроксид – ионы - …
Слайд 4
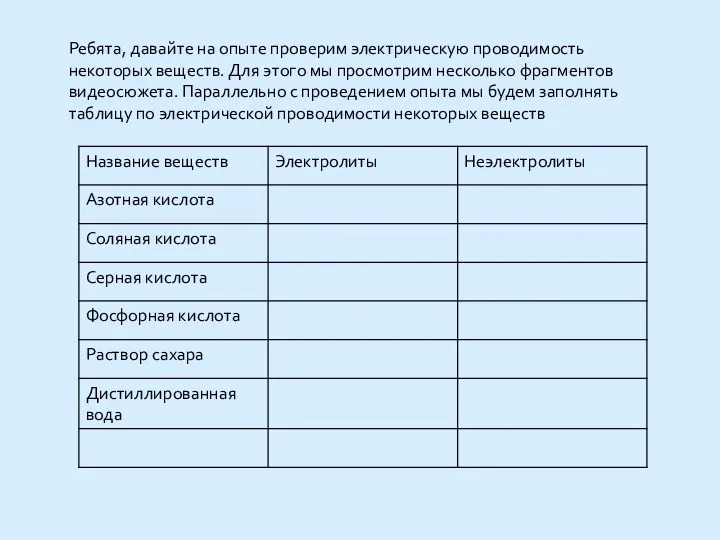
Ребята, давайте на опыте проверим электрическую проводимость некоторых веществ. Для этого
мы просмотрим несколько фрагментов видеосюжета. Параллельно с проведением опыта мы будем заполнять таблицу по электрической проводимости некоторых веществ
Слайд 5

Среди перечисленных формул выберите: электролиты и неэлектролиты.
CO2;
H2SO4;
CuCl2;
Fe(OH)3;
Al2(SO4)3;
H2SiO3;
NaOH;
CuO;
HCl;
BaSO4;
K2CO3
Слайд 6

Напишите уравнения электролитической диссоциации следующих кислот:
а) бромоводородной кислоты
б) серной
кислоты
в) фосфорной кислоты
г) сероводородной кислоты
д) азотной кислоты
Слайд 7

Напишите уравнения электролитической диссоциации следующих солей:
а) ZnCl2
б) Al(NO3)3
в) KНSO4
г) Na2CO3
д) KН2PO4
е) Fe(ОН)2Cl
Слайд 8

Химический эксперимент
Опыт№1 Взаимодействие сульфата меди(II) с хлоридом бария.
Налейте в пробирку сульфат
меди (II) и добавьте небольшое количество хлорида бария. Что произошло? Запишите уравнение реакции в молекулярном и ионном виде..
Опыт№2.Реакция нейтрализации. Взаимодействие гидроксида натрия с соляной кислотой.
Налейте в пробирку гидроксид натрия и добавьте 2– 3 капли метилоранжа и по каплям добавляйте раствор соляной кислоты. Что наблюдаете? Запишите уравнение реакции в молекулярном и ионном виде.
Опыт №3. Взаимодействие солей с кислотами.
В химический стакан поместите небольшой кусочек мела и добавьте раствор соляной кислоты. Что наблюдаете? Запишите уравнения в молекулярном и ионном виде.
Слайд 9

Тест «Выбери правильный ответ».
1. Катион - это: а) ион меди б)
атом серы в) ион серы г) атом меди.
2. Анион - это: а) ион натрия б) ион аммония в) карбонат-ион г) ион водорода.
3. Окраска фенолфталеина в растворе, полученном при взаимодействии калия с водой:
а) синяя б) малиновая в) жёлтая г) бесцветная.
4. Формула вещества, образующего при диссоциации сульфат-ионы:
а) Na2S б) SO3 в) Na2SO4 г) BaSO4
5 Формула вещества, образующего при диссоциации сульфат-ионы и ионы водорода:
а) KHS б) KHSO3 в) Na2S г) NaHSO4
Слайд 10

Задание на дом:
§§ 5-11
задачник: № 2-32, 2-41 стр. 21-22









 Факторы, влияющие на скорость химической реакции
Факторы, влияющие на скорость химической реакции Химиялық термодинамиканың негіздері. Негізгі түсініктері мен зандары. Термохимиялық есептеулер
Химиялық термодинамиканың негіздері. Негізгі түсініктері мен зандары. Термохимиялық есептеулер Медь, цинк, хром. Обобщающий урок
Медь, цинк, хром. Обобщающий урок Простые вещества неметаллы
Простые вещества неметаллы Теория электролитической диссоциации (ТЭД)
Теория электролитической диссоциации (ТЭД) Кто хочет стать отличником по химии. Игра
Кто хочет стать отличником по химии. Игра Apa în natură. Resursele de apă
Apa în natură. Resursele de apă Гетероатомные соединения нефти
Гетероатомные соединения нефти Снег и лед. Тайны твердой воды
Снег и лед. Тайны твердой воды Задача №5. Аккумулятор на основе железа
Задача №5. Аккумулятор на основе железа Химические свойства кислот в свете теории электролитической диссоциации
Химические свойства кислот в свете теории электролитической диссоциации Кислотно-основные свойства органических соединений
Кислотно-основные свойства органических соединений Химическая организация клетки
Химическая организация клетки Гидрирование альдегидов и кетонов
Гидрирование альдегидов и кетонов Фенолы. Классификация и номенклатура фенолов
Фенолы. Классификация и номенклатура фенолов Комплексные соединения и лигандообменные равновесия
Комплексные соединения и лигандообменные равновесия Углеводы. Моносахариды
Углеводы. Моносахариды Композиционные материалы
Композиционные материалы Искусственные полимеры. 10 класс
Искусственные полимеры. 10 класс Углеводороды – самые простые органические соединения
Углеводороды – самые простые органические соединения Алкины
Алкины Амфотерные соединения
Амфотерные соединения Кристаллические решетки
Кристаллические решетки Состав и свойства чая
Состав и свойства чая Физические и химические явления
Физические и химические явления Тепловий ефект хімічних реакцій. Екзотермічні і ендотермічні реакції. Термохімічні рівняння
Тепловий ефект хімічних реакцій. Екзотермічні і ендотермічні реакції. Термохімічні рівняння Значение пищи и ее состав
Значение пищи и ее состав Титан және оның қорытпалары. Титаннан жасалған құралдар
Титан және оның қорытпалары. Титаннан жасалған құралдар