Тепловий ефект хімічних реакцій. Екзотермічні і ендотермічні реакції. Термохімічні рівняння презентация
Содержание
- 2. Пригадаємо!
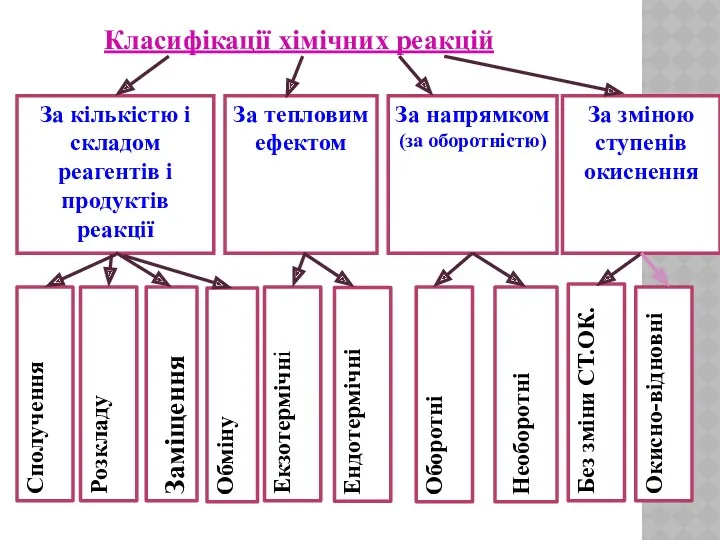
- 3. За кількістю і складом реагентів і продуктів реакції За тепловим ефектом За напрямком (за оборотністю) За
- 4. МЕТА УРОКУ: познайомитися з класифікацією реакцій за тепловим ефектом: з екзотермічними і ендотермічними реакціями; навчитися писати
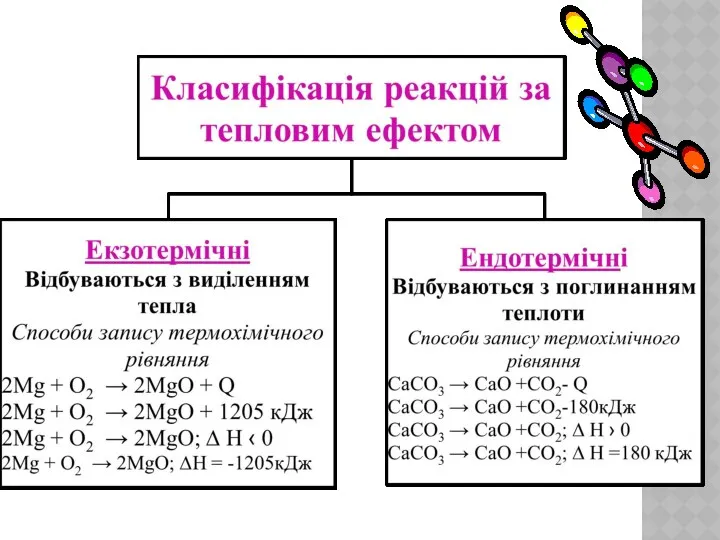
- 5. Тепловий ефект реакції – кількість теплоти, що виділяється чи поглинається під час хімічних реакції. Тепловий ефект
- 6. Термохімічні рівняння – хімічні рівняння, в яких зазначено кількість теплоти, що виділяється або поглинається.
- 8. Закріпи свої знання!
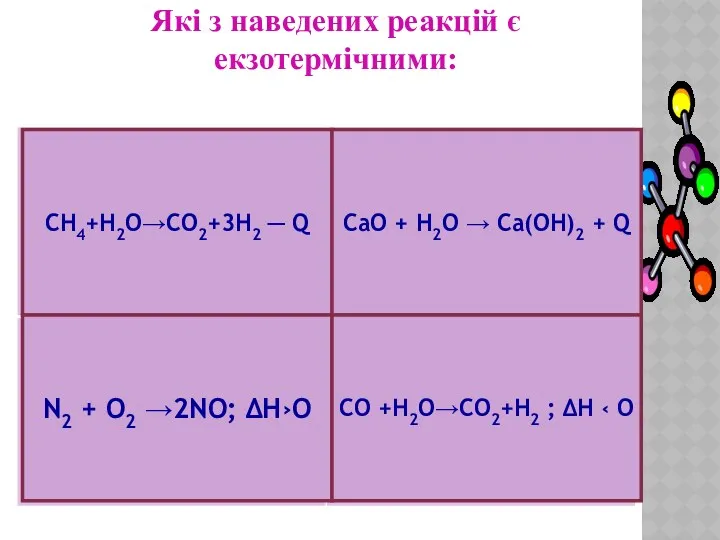
- 9. Які з наведених реакцій є екзотермічними: СН4+Н2О→СО2+3Н2 ─ Q N2 + O2 →2NO; ∆Н›О СаО +
- 10. Запишіть рівняння горіння водню. Тепловий ефект реакції дорівнює 572кдж. 2Н2 + О2 → 2Н2О + 572кДж
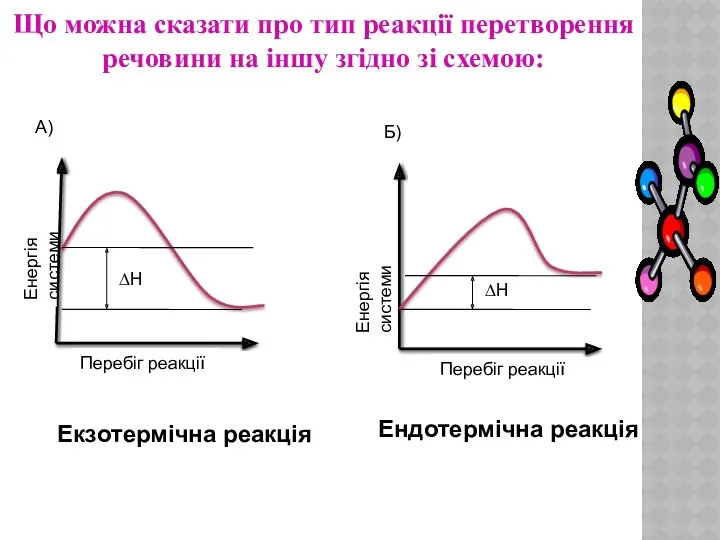
- 11. Що можна сказати про тип реакції перетворення речовини на іншу згідно зі схемою: Енергія системи Перебіг
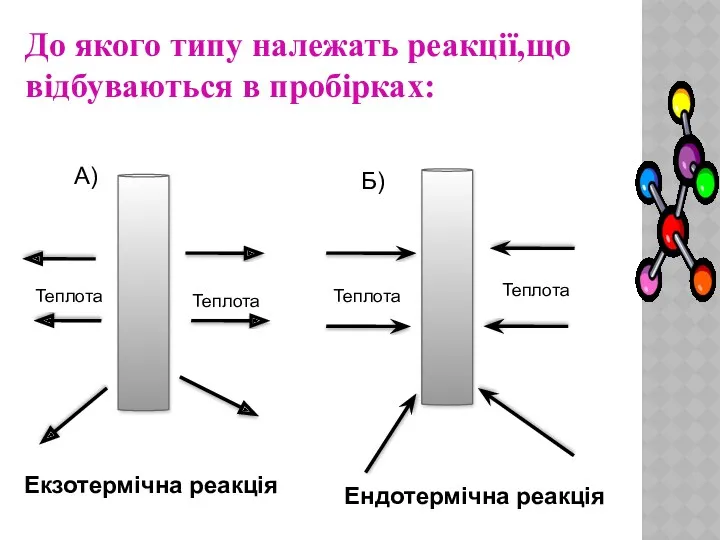
- 12. До якого типу належать реакції,що відбуваються в пробірках: А) Б) Теплота Теплота Теплота Теплота Екзотермічна реакція
- 15. Обчислення за термохімічними рівняннями №1. Скільки тепла виділиться в результаті спалювання 18г вугілля? №2. У результаті
- 17. Скачать презентацию









 Кремний и его соединения
Кремний и его соединения Центрифугирование
Центрифугирование Технология производства сложных полиэфиров
Технология производства сложных полиэфиров Сероводород
Сероводород Неметаллические материалы, используемые в машино- и приборостроении
Неметаллические материалы, используемые в машино- и приборостроении Алкины. Химические свойства и способы получения алкинов
Алкины. Химические свойства и способы получения алкинов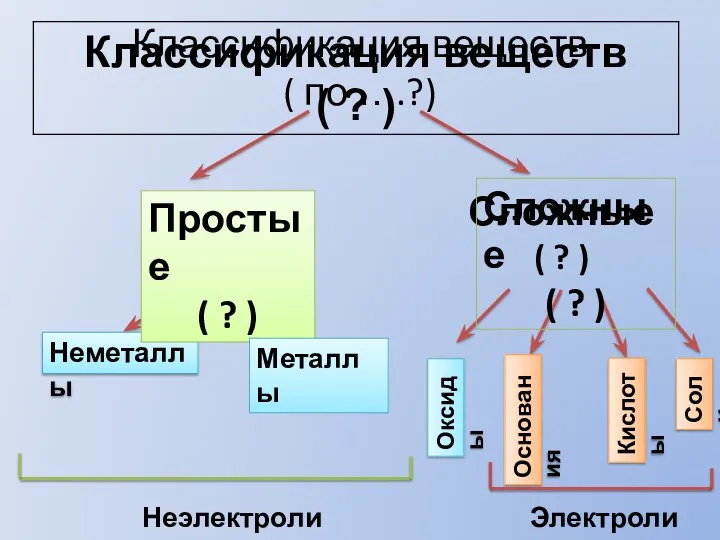 Классификация веществ
Классификация веществ Періодична система Д.І.Менделєєва
Періодична система Д.І.Менделєєва Алкены. Строение алкенов
Алкены. Строение алкенов i9tjjvxuvf7fj7k4drnlmj56tgok
i9tjjvxuvf7fj7k4drnlmj56tgok Получение и приминение этилена
Получение и приминение этилена Строение электронных оболочек атомов
Строение электронных оболочек атомов Углеводы. Общая формула углеводов Сn(H2O)m
Углеводы. Общая формула углеводов Сn(H2O)m Активные формы кислорода. Антиоксиданты их физиологическая роль
Активные формы кислорода. Антиоксиданты их физиологическая роль Хімічні властивості алканів
Хімічні властивості алканів Периодический закон и система элементов Д.И. Менделеева
Периодический закон и система элементов Д.И. Менделеева Азот
Азот Химиялық элемент алюминий
Химиялық элемент алюминий Алканы
Алканы Золото. Виды золота
Золото. Виды золота Получение, собирание и распознавание газов. Практическая работа
Получение, собирание и распознавание газов. Практическая работа Элементы пятой-А группы. Азот и фосфор
Элементы пятой-А группы. Азот и фосфор Виды вспомогательного оборудования химических производств
Виды вспомогательного оборудования химических производств Химическая взрывчатка
Химическая взрывчатка Чистые вещества и смеси. Состав смесей. Разделение смесей
Чистые вещества и смеси. Состав смесей. Разделение смесей Биологически важные вещества жиры
Биологически важные вещества жиры Галогенопроизводные углеводородов 1
Галогенопроизводные углеводородов 1 Спирти. Історична довідка
Спирти. Історична довідка