Содержание
- 2. ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОТ В СВЕТЕ ТЕОРИИ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ
- 3. КЛАССИФИКАЦИЯ КИСЛОТ
- 4. HCl HNO3 H2SO4 HSO4– → Н+ + Cl- → H+ + NO3– → H+ + HSO4–
- 5. Диссоциация многоосновной кислоты протекает главным образом по первой ступени, в меньшей степени по второй и лишь
- 7. ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОТ 1. Изменение цвета универсального индикатора в красный цвет.
- 8. ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОТ 2. Взаимодействие с Ме, стоящими в ряду напряжений до водорода (искл. H2SiO3, HNO3;
- 9. ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОТ 3. Взаимодействие с оксидами металлов: CaO + HNO3 →
- 10. ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОТ 4. Взаимодействие с основаниями: а) растворимыми: NaOH + H2SO4 → б) нерастворимыми: Fe(OH)3
- 11. 3KOH + FeCl3 = Fe(OH)3 + 3KCl 3K+ + 3OH— + Fe3+ + 3Cl— = Fe(OH)3
- 12. ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОТ 5. Взаимодействие с солями (реакция осуществима, если в результате выпадает осадок или выделяется
- 13. ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОТ 6. Нерастворимые кислоты при нагревании разлагаются: t H2SiO3 →
- 14. ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОТ 7. Реакции этерификации – образование сложных эфиров при взаимодействии спиртов с кислородсодержащими неорганическими
- 15. ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОТ 8. Окислительные свойства кислот проявляются при взаимодействии кислот с металлами. Взаимодействие азотной и
- 17. Скачать презентацию














 Анализ проб воды
Анализ проб воды Carbohydrates and their metabolism. Digestion of carbohydrates
Carbohydrates and their metabolism. Digestion of carbohydrates Химические свойства и получение алканов
Химические свойства и получение алканов Олово и свинец
Олово и свинец Күкірт қышқылы
Күкірт қышқылы Показатели химической обстановки при авариях на химически опасных объектах
Показатели химической обстановки при авариях на химически опасных объектах Жуғыш заттар және жуғыш әсері. 2 Лекция
Жуғыш заттар және жуғыш әсері. 2 Лекция Кристаллы и минералы
Кристаллы и минералы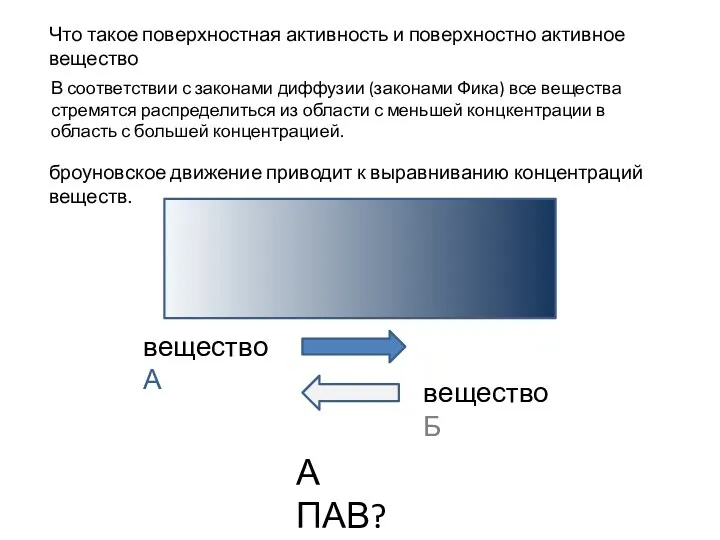 Поверхностная активность и поверхностно активное вещество
Поверхностная активность и поверхностно активное вещество Строение и свойства циклоалканов
Строение и свойства циклоалканов Химические реакции или химические явления
Химические реакции или химические явления Растворы ВМС
Растворы ВМС Констукционные и функциональные волокнистые композиты. Стекловолокно
Констукционные и функциональные волокнистые композиты. Стекловолокно Основные способы получения металлов
Основные способы получения металлов Расчет распределения пор по размерам из изотерм адсорбции
Расчет распределения пор по размерам из изотерм адсорбции Обчислення об'ємних відношень газів за хімічними рівняннями. Хімія. 9 клас
Обчислення об'ємних відношень газів за хімічними рівняннями. Хімія. 9 клас Установка гидрокрекинга
Установка гидрокрекинга Закономірності протікання хімічних реакцій
Закономірності протікання хімічних реакцій Арилалкиламины, гидроксифенилалкиламины и их производные
Арилалкиламины, гидроксифенилалкиламины и их производные Азотсодержащие органические соединения. Лекция 8
Азотсодержащие органические соединения. Лекция 8 Приёмы обращения с лабораторным оборудованием и основы техники безопасности
Приёмы обращения с лабораторным оборудованием и основы техники безопасности Особенности лантаноидов и актиноидов
Особенности лантаноидов и актиноидов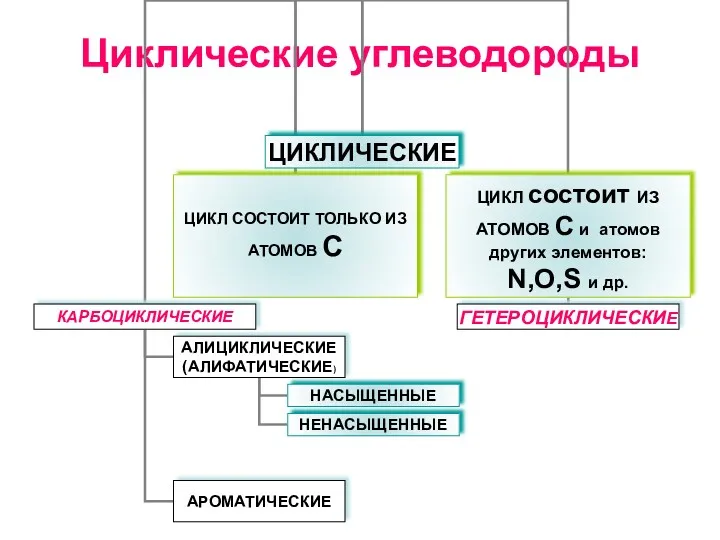 Циклические углеводороды
Циклические углеводороды Полимеры
Полимеры Кристаллические решетки
Кристаллические решетки Алкадиены: строение, номенклатура, гомологи, изомерия
Алкадиены: строение, номенклатура, гомологи, изомерия Соли, их классификация и свойства
Соли, их классификация и свойства Молярная масса вещества
Молярная масса вещества