Содержание
- 2. Алкадиены - ациклические углеводороды, содержащие в молекуле, две двойные связи между атомами углерода общая формула: CnH2n-2
- 3. Углеводороды содержащие две двойные связи ,находящиеся возле соседних атомов углерода. 1 2 3 4 СН2 =С=СН-СН3
- 4. Углеводороды содержащие две двойные связи ,между которыми находится одна одинарная связь. 1 2 3 4 5
- 5. Углеводороды содержащие две двойные связи ,между которыми находится несколько одинарных связей. 8 7 6 5 4
- 6. Номенклатура алкадиенов Правила: 1. Главная цепь должна содержать обе двойные связи. 2. Нумерацию ведут с того
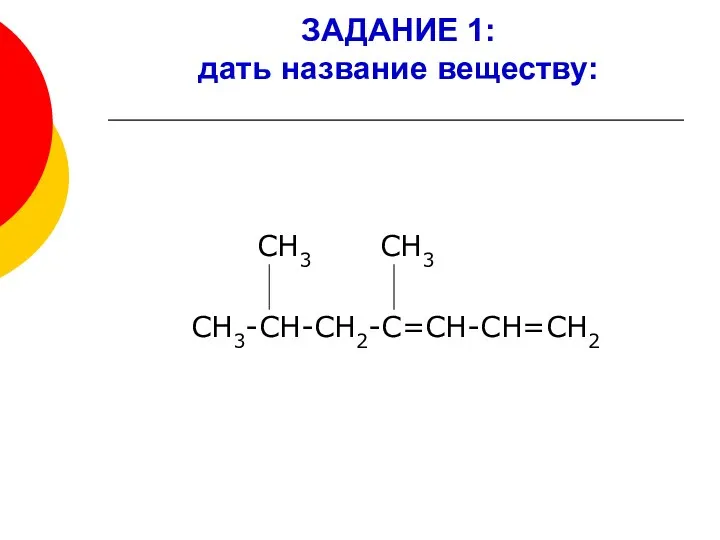
- 7. ЗАДАНИЕ 1: дать название веществу: СН3 СН3 СН3-СН-СН2-С=СН-СН=СН2
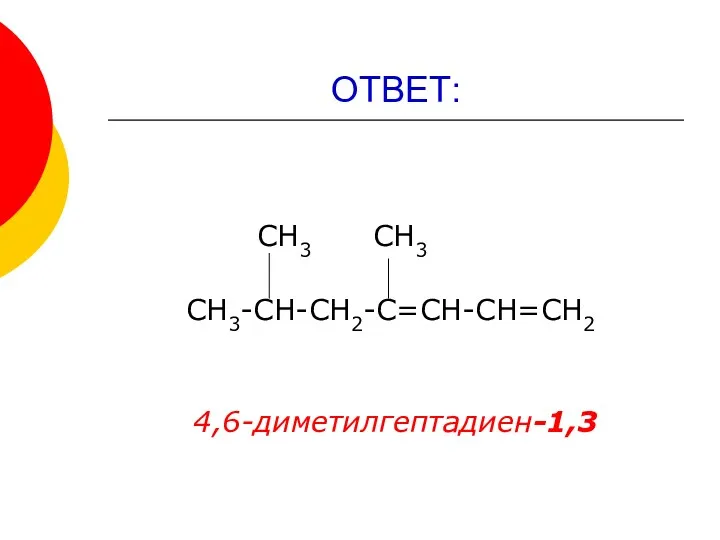
- 8. ОТВЕТ: СН3 СН3 СН3-СН-СН2-С=СН-СН=СН2 4,6-диметилгептадиен-1,3
- 9. ИЗОМЕРИЯ АЛКАДИЕНОВ 1. Структурная: а) изомерия углеродного скелета б) изомерия положения двойных связей. 2. Пространственная: а)цис-транс
- 10. ИЗОМЕРИЯ АЛКАДИЕНОВ
- 11. ПОЛУЧЕНИЕ АЛКАДИЕНОВ Двухстадийное дегидрирование алканов СН3-СН2-СН2-СН3 СН2=СН-СН=СН2+2Н2 бутан бутадиен -1, 3
- 12. ХИМИЧЕСКИЕ СВОЙСТВА Галогенирование 1 (неполное) СН2=СН-СН=СН2 + Br2 1, 2 - присоединение СН2-СН-СН=СН2 3,4 – дибромбутен-1
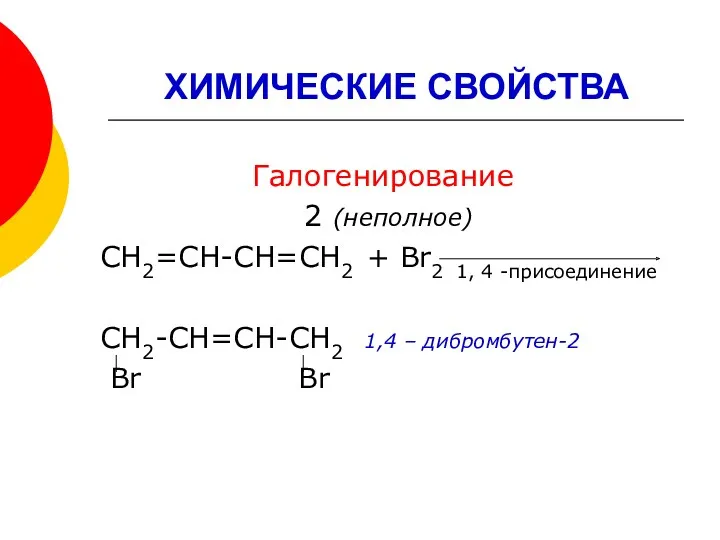
- 13. ХИМИЧЕСКИЕ СВОЙСТВА Галогенирование 2 (неполное) СН2=СН-СН=СН2 + Br2 1, 4 -присоединение СН2-СН=СН-СН2 1,4 – дибромбутен-2 Br
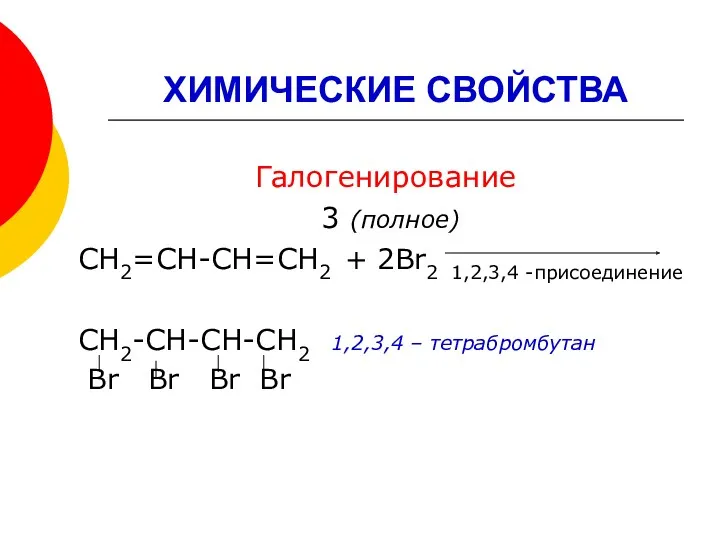
- 14. ХИМИЧЕСКИЕ СВОЙСТВА Галогенирование 3 (полное) СН2=СН-СН=СН2 + 2Br2 1,2,3,4 -присоединение СН2-СН-СН-СН2 1,2,3,4 – тетрабромбутан Br Br
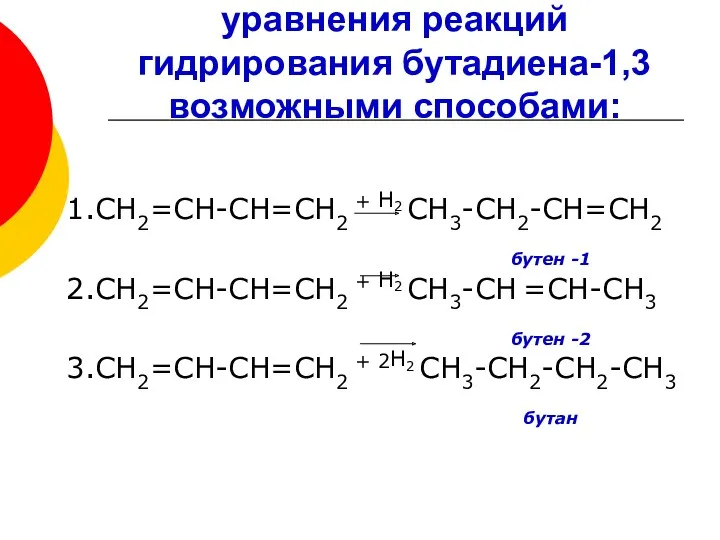
- 15. уравнения реакций гидрирования бутадиена-1,3 возможными способами: 1.СН2=СН-СН=СН2 + Н2 СН3-СН2-СН=СН2 бутен -1 2.СН2=СН-СН=СН2 + Н2 СН3-СН
- 16. ХИМИЧЕСКИЕ СВОЙСТВА Гидрогалогенирование (по правилу Марковникова) 1 стадия СН2=СН-СН=СН2 + НСI СН3-СН-СН=СН2 СI 3-хлорбутен -1
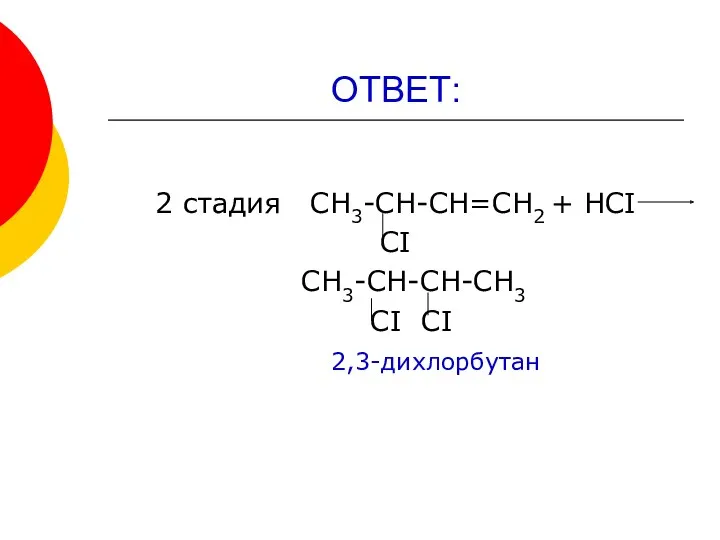
- 17. ОТВЕТ: 2 стадия СН3-СН-СН=СН2 + НСI СI СН3-СН-СН-СН3 СI СI 2,3-дихлорбутан
- 18. ХИМИЧЕСКИЕ СВОЙСТВА Полимеризация Полимеризация диеновых УВ приводит к образованию каучуков – полимеров, обладающих высокой эластичностью. бутадиен
- 19. История открытия каучука Родина каучука – Центральная и Южная Америка. Во влажных жарких тропиках, по берегам
- 20. История открытия каучука Если на коре дерева сделать надрез, то из ранки вытекает сок молочно-белого цвета,
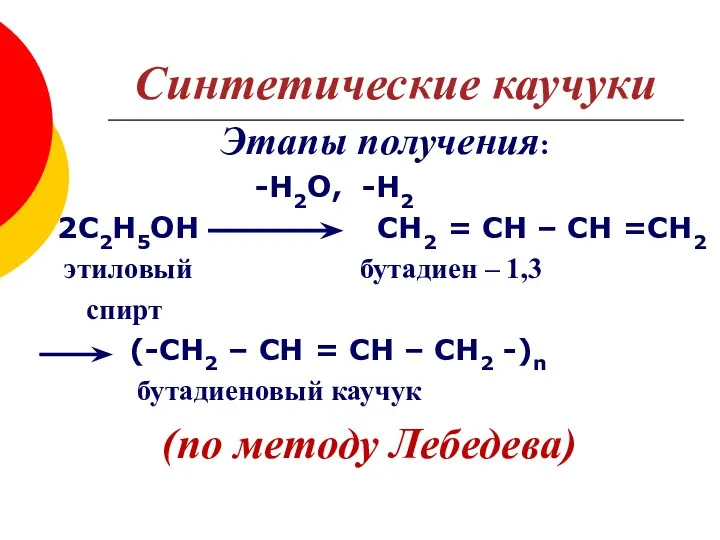
- 21. Синтетические каучуки Основателем первого в мире крупномасштабного производства синтетического каучука по праву считается русский ученый С.В.Лебедев.
- 22. Синтетические каучуки Этапы получения: -Н2О, -Н2 2С2Н5ОН СН2 = СН – СН =СН2 этиловый бутадиен –
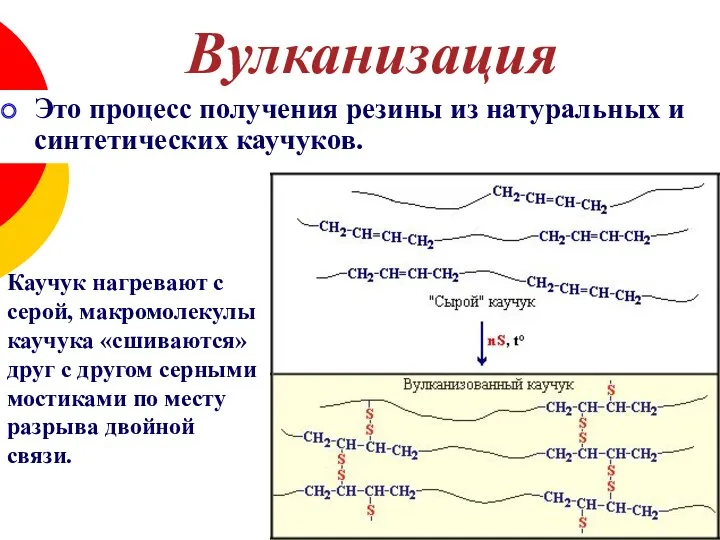
- 23. Это процесс получения резины из натуральных и синтетических каучуков. Каучук нагревают с серой, макромолекулы каучука «сшиваются»
- 24. Применение
- 25. СПАСИБО ЗА Внимание!!!
- 27. Скачать презентацию
















 Хімічні властивості металів
Хімічні властивості металів Карбоновые кислоты. Тест
Карбоновые кислоты. Тест Материаловедение. Основные задачи материаловедения
Материаловедение. Основные задачи материаловедения Электролитическая диссоциация. Вещества в растворах
Электролитическая диссоциация. Вещества в растворах Общая электронная теория восстановления и окисления металлов
Общая электронная теория восстановления и окисления металлов Фосфор. Урок в 9 классе
Фосфор. Урок в 9 классе Химические свойства кислот
Химические свойства кислот Кристаллические решетки
Кристаллические решетки Пробоотбор других ООС. Лекция 3
Пробоотбор других ООС. Лекция 3 Дисперсные системы в атмосфере
Дисперсные системы в атмосфере Хром. Физические и химические свойства
Хром. Физические и химические свойства Титан және оның қорытпалары. Титанның физика-химиялық қасиеттері
Титан және оның қорытпалары. Титанның физика-химиялық қасиеттері Химический факультет
Химический факультет Химия как компонент системы естественнонаучного образования
Химия как компонент системы естественнонаучного образования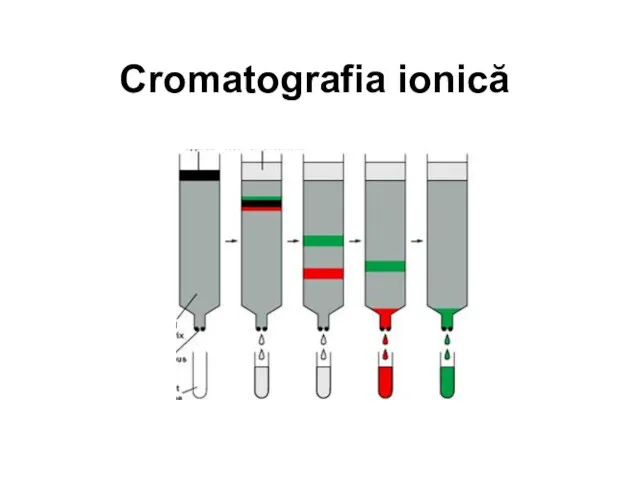 Cromatografia ionică
Cromatografia ionică Основні класи неорганічних сполук
Основні класи неорганічних сполук Алюминий и сплавы на его основе
Алюминий и сплавы на его основе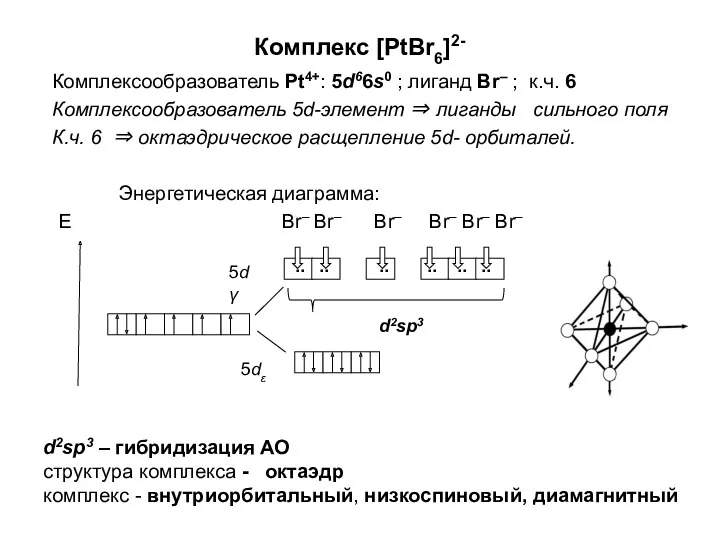 Комплексообразователь. (Лекция 5)
Комплексообразователь. (Лекция 5) Как и где используется соляная кислота
Как и где используется соляная кислота Электрохимические процессы
Электрохимические процессы Кислород. Атом кислорода
Кислород. Атом кислорода Тепловой эффект химических реакций. 8 класс
Тепловой эффект химических реакций. 8 класс Классификация и общая характеристика механизмов образования свободных радикалов и активных форм кислорода
Классификация и общая характеристика механизмов образования свободных радикалов и активных форм кислорода Гранулометрический состав горных пород
Гранулометрический состав горных пород Дезодоранты. Антиперспиранты
Дезодоранты. Антиперспиранты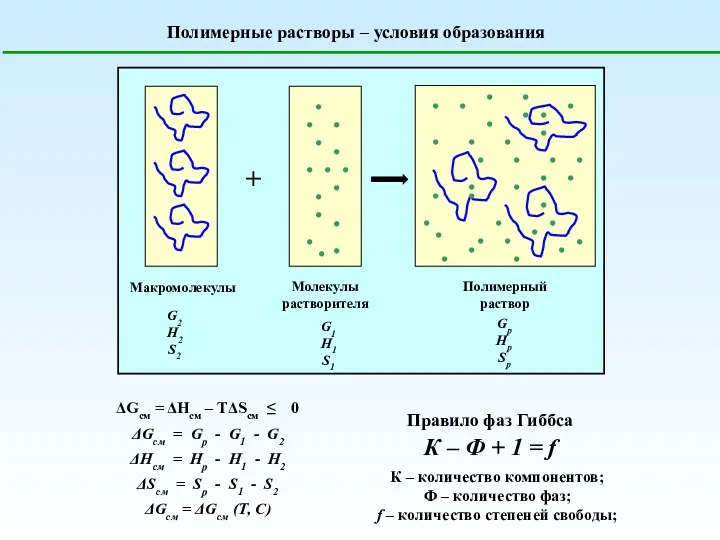 Полимерные растворы. Условия образования
Полимерные растворы. Условия образования Химиялық тепе-теңдік
Химиялық тепе-теңдік Неметаллы. Общая характеристика неметаллов
Неметаллы. Общая характеристика неметаллов