Содержание
- 2. 1. Теория электролитической диссоциации (ТЭД). В 1887г. Шведский учёный С.Аррениус для объяснения особенностей водных растворов веществ
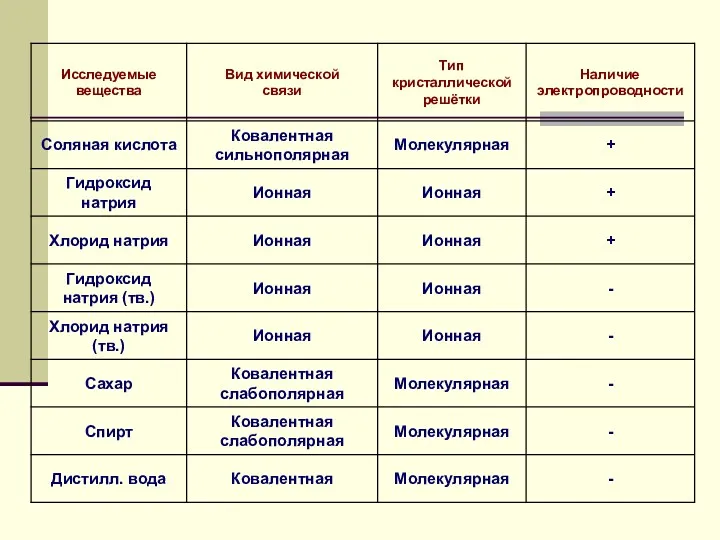
- 3. 1) вода 2) соляная кислота 3) гидроксид натрия 4) сульфат меди 5) хлорид натрия 6) сахар,
- 5. Современное содержание ТЭД можно свести к четырем основным положениям. I-е положение: Все вещества по их способности
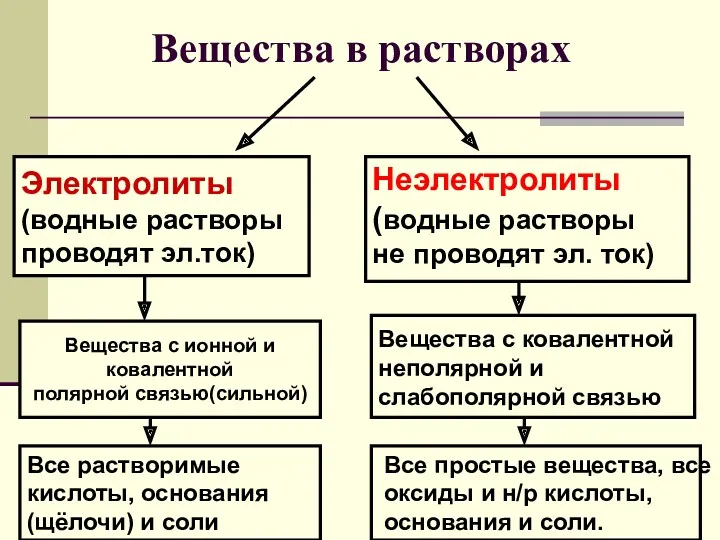
- 6. Вещества в растворах Электролиты (водные растворы проводят эл.ток) Неэлектролиты (водные растворы не проводят эл. ток) Вещества
- 7. II-е положение ТЭД В растворах электролиты диссоциируют ( распадаются ) на положительные и отрицательные ионы. Процесс
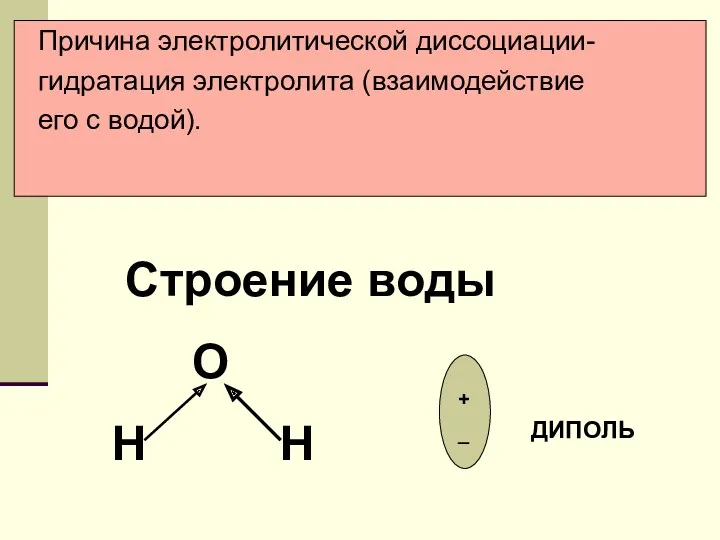
- 8. Причина электролитической диссоциации- гидратация электролита (взаимодействие его с водой). Строение воды О Н Н + _
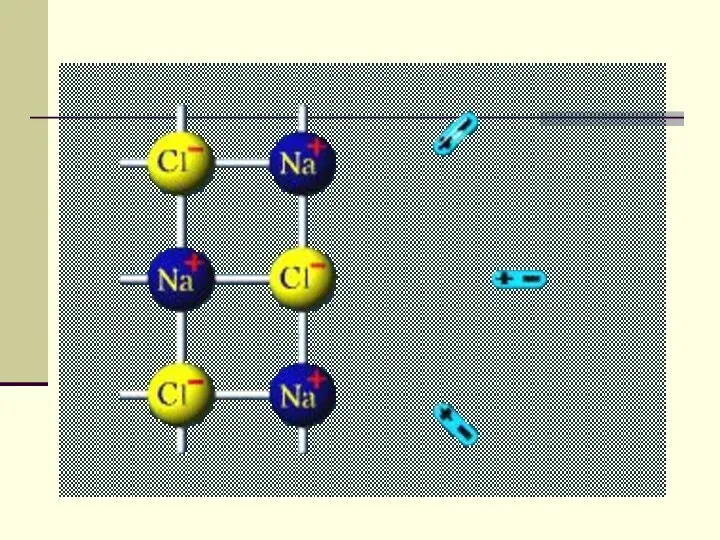
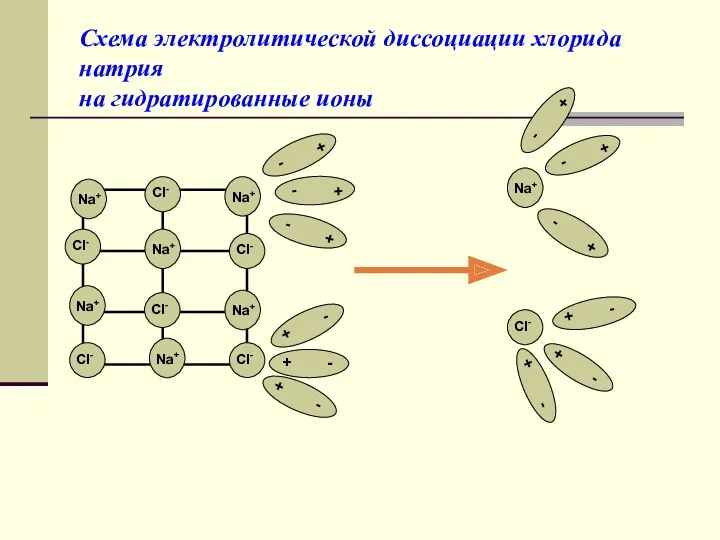
- 10. Схема электролитической диссоциации хлорида натрия на гидратированные ионы
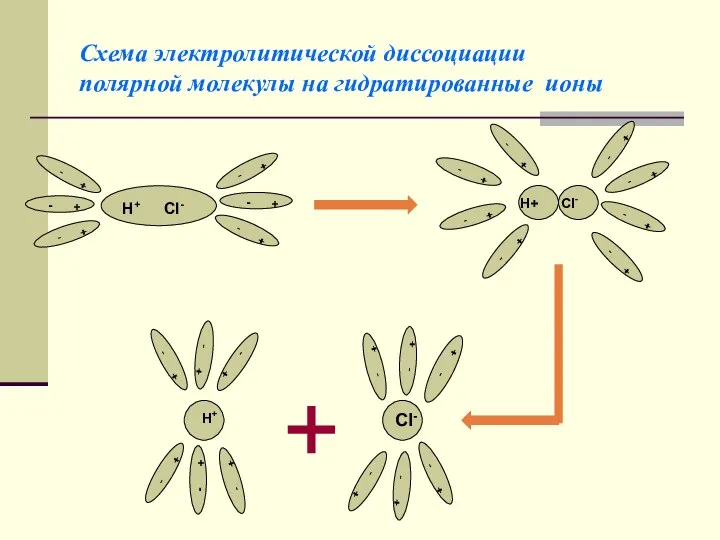
- 11. Схема электролитической диссоциации полярной молекулы на гидратированные ионы
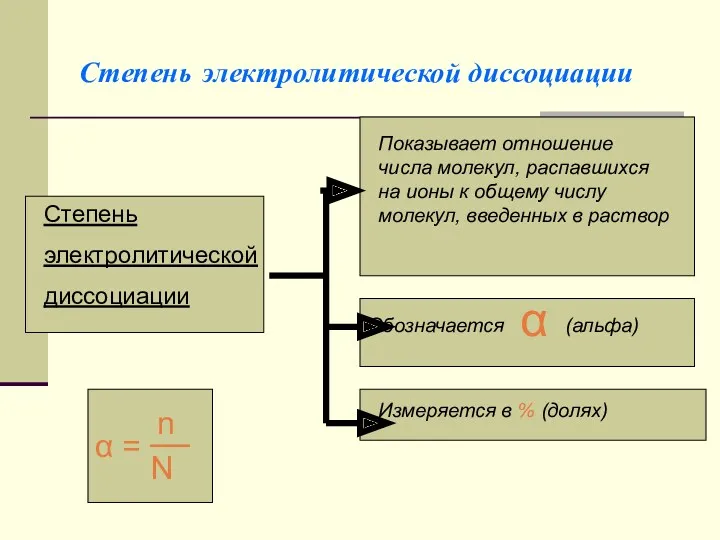
- 12. Степень электролитической диссоциации Степень электролитической диссоциации Показывает отношение числа молекул, распавшихся на ионы к общему числу
- 13. Степень диссоциации зависит от: природы вещества концентрации раствора температуры
- 15. Скачать презентацию





 Основи. Гідроксиди Натрію і Кальцію
Основи. Гідроксиди Натрію і Кальцію Метал конструкциялық материалдар
Метал конструкциялық материалдар Nucleic acids
Nucleic acids Курс Материаловедение. Введение
Курс Материаловедение. Введение Основные электрохимические процессы
Основные электрохимические процессы Изомерия. Виды изомерии
Изомерия. Виды изомерии Кислород, азот, водород и инертные газы. Раздел 3
Кислород, азот, водород и инертные газы. Раздел 3 Скорость химических реакций. Факторы, влияющие на скорость химической реакции
Скорость химических реакций. Факторы, влияющие на скорость химической реакции Стирка по научному
Стирка по научному Гальваникалық элементтер
Гальваникалық элементтер Выращивание кристалла медного купороса CuSO4*5Н2О в разных условиях
Выращивание кристалла медного купороса CuSO4*5Н2О в разных условиях Stirring in liquid media
Stirring in liquid media Химические реакции
Химические реакции Лабораторные исследования состава и физико-химических свойств нефти
Лабораторные исследования состава и физико-химических свойств нефти Физические и химические свойства воды
Физические и химические свойства воды Белки. 9 класс
Белки. 9 класс Количественный анализ. Титриметрический анализ
Количественный анализ. Титриметрический анализ Кристалічні ґратки. Залежність фізичних властивостей речовини від типів кристалічних ґраток
Кристалічні ґратки. Залежність фізичних властивостей речовини від типів кристалічних ґраток Галогены (солеобразующие)
Галогены (солеобразующие) Цветные маталлы и сплавы
Цветные маталлы и сплавы Стратегия органического синтеза
Стратегия органического синтеза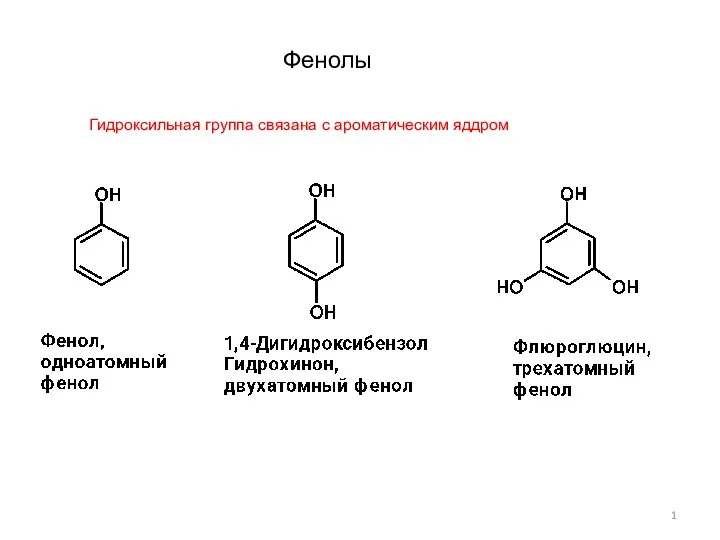 Фенолы-1
Фенолы-1 Курс коллоидной химии
Курс коллоидной химии Амины
Амины Глицерин. Основные способы получения
Глицерин. Основные способы получения Реакции ионного обмена. Ионное произведение воды. Водородный показатель. Индикаторы
Реакции ионного обмена. Ионное произведение воды. Водородный показатель. Индикаторы Строение и свойства циклоалканов
Строение и свойства циклоалканов Кислотно-основное титрование
Кислотно-основное титрование