Содержание
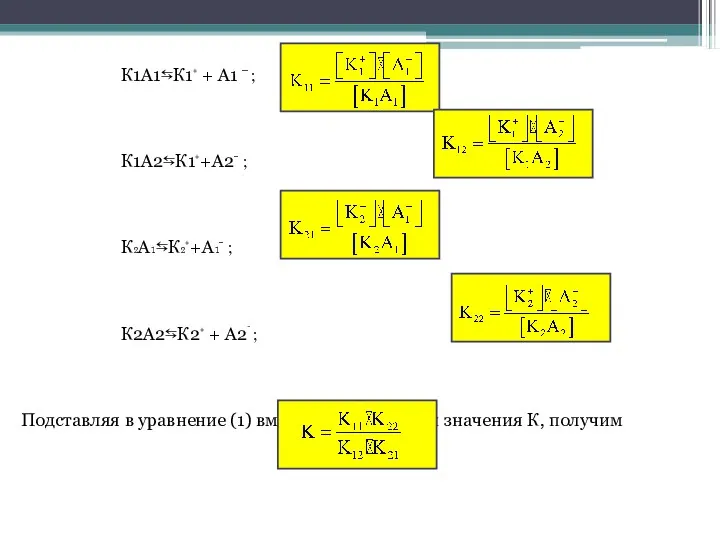
- 2. К1А1⇆К1⁺ + А1 − ; К1А2⇆К1⁺+А2⁻ ; К₂А₁⇆К₂⁺+А₁⁻ ; К2А2⇆К2⁺ + А2⁻ ; Подставляя в уравнение
- 3. Если К>1, т.е. К₁₁· К₂₂ > К₁₂·К₂₁, то равновесие смещено вправо (легче идёт прямая реакция). Если
- 4. В виде ионов записывают формулы: сильных кислот (HClO4, H2SO4, HNO3, HI и др.); сильных оснований (щелочей
- 5. В виде молекул записывают формулы: воды; слабых кислот (HNO2, HCN, H2CO3, H2SO3, CH3COOH и др.); слабых
- 6. Реакции обмена в растворах принято изображать тремя уравнениями: NaOH + HСl = NaCl + H2O –
- 7. Составим молекулярное и ионное уравнения реакции между нитратом серебра (I) и хлоридом натрия: AgNO3 + NaCl
- 8. Составим молекулярное и ионное уравнения реакции нейтрализации между растворами гидроксида натрия и серной кислоты: 2NaOH +
- 9. Составим молекулярное и ионное уравнения реакции между растворами гидроксида кальция и хлорида аммония: Ca(OH)2 + 2NH4Cl
- 10. 4. Реакции, протекающие с образованием комплексного иона Составим молекулярное и ионное уравнения реакции между растворами йодида
- 11. Если среди исходных веществ имеются слабые электролиты или малорастворимые вещества, то такие реакции являются обратимыми, т.е.
- 12. Если исходными веществами реакций обмена являются сильные электролиты, которые при взаимодействии не образуют малорастворимых или малодиссоциирующих
- 13. Ионное произведение воды Вода является слабым электролитом, который диссоциирует на ионы: H₂O ⇄ H⁺ + OH⁻
- 14. Ионное произведение воды – постоянная величина, как для чистой воды, так и водных растворов различных электролитов,
- 15. Водородный показатель По кислотно-основным свойствам растворы обычно делят на кислые, нейтральные и щелочные. Это лишь качественная
- 16. Расчет рН в растворах сильных и слабых кислот 1. Поскольку диссоциация сильной кислоты (HNO3, HCl, H2SO4,
- 17. Расчет рН в растворах сильных и слабых оснований 1. Диссоциация сильного основания (LiOH, NaOH, KOH, RbOH,
- 18. Пример. Считая диссоциацию гидроксида калия в воде полной, вычислите PН 0,001 М раствора KOH. Решение. Определяем
- 19. Индикаторы Значение pH растворов можно экспериментально определить при помощи кислотно-основных индикаторов – веществ, которые изменяю окраску
- 21. Скачать презентацию

















 Формирование системы знаний о веществе. Лекция 14-15
Формирование системы знаний о веществе. Лекция 14-15 Катиониты. Классификация катионитов
Катиониты. Классификация катионитов Роль хімічних знань у пізнанні природи
Роль хімічних знань у пізнанні природи Физические и химические явления. Признаки и условия протекания химических реакций
Физические и химические явления. Признаки и условия протекания химических реакций Фотохимический смог
Фотохимический смог Подготовка обучающихся к выполнению заданий КИМ ЕГЭ по химии при изучении темы Гидролиз
Подготовка обучающихся к выполнению заданий КИМ ЕГЭ по химии при изучении темы Гидролиз Галогены
Галогены Электронная природа химической связи. Кристаллические и аморфные вещества
Электронная природа химической связи. Кристаллические и аморфные вещества Обмен индивидуальных аминокислот
Обмен индивидуальных аминокислот Нуклеопротеины
Нуклеопротеины Реакции деструкции макромолекул
Реакции деструкции макромолекул Подгруппа серы и ее соединения
Подгруппа серы и ее соединения Физико-химические свойства поливинилового спирта и поливинилформаля
Физико-химические свойства поливинилового спирта и поливинилформаля Электролитическая диссоциация
Электролитическая диссоциация Химическая лаборатрия. Химический состав растений
Химическая лаборатрия. Химический состав растений Аммиак. 9 класс
Аммиак. 9 класс Использование горюче-смазочных материалов в автотранспорте
Использование горюче-смазочных материалов в автотранспорте Превращение веществ
Превращение веществ Железо. Строение атома, химические и физические свойства. Урок №1
Железо. Строение атома, химические и физические свойства. Урок №1 Протолитическая теория кислот и оснований. Протолитическое равновесие. Буферные растворы. Лекция 01
Протолитическая теория кислот и оснований. Протолитическое равновесие. Буферные растворы. Лекция 01 Технология монокристаллов и особо чистых веществ
Технология монокристаллов и особо чистых веществ Жиры
Жиры Атом. Модели строения атома
Атом. Модели строения атома Классы неорганических веществ (лекция № 4)
Классы неорганических веществ (лекция № 4) Соединения щелочных металлов
Соединения щелочных металлов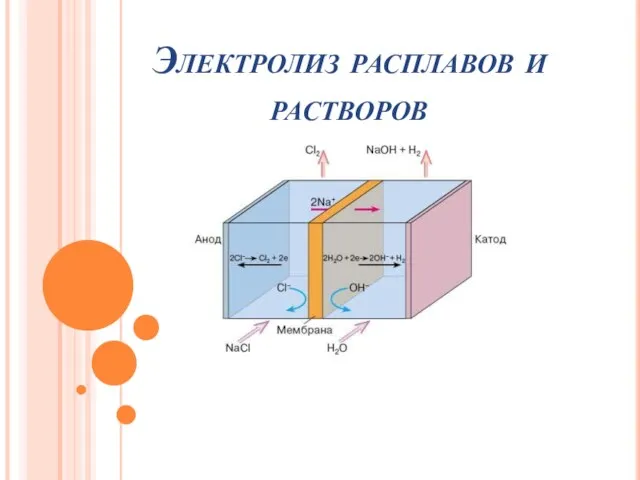 Электролиз расплавов и растворов
Электролиз расплавов и растворов Молярная масса вещества
Молярная масса вещества Метаболизм кетоновых тел. Метаболизм холестерина
Метаболизм кетоновых тел. Метаболизм холестерина