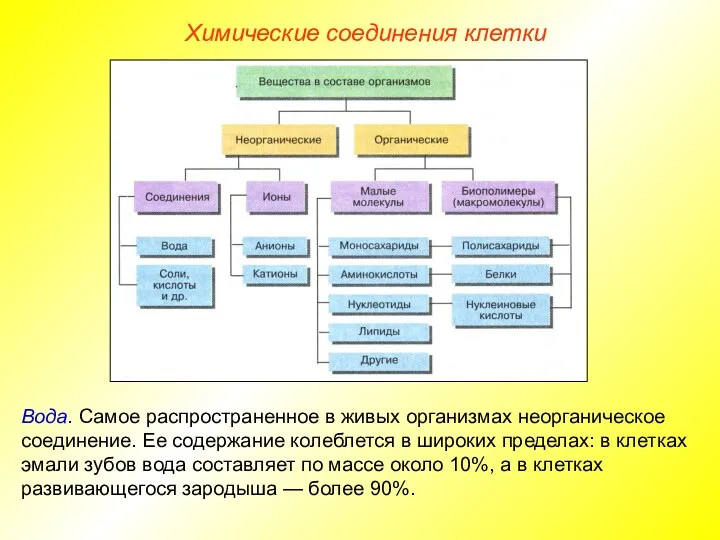
Является основой внутренней и внутриклеточной среды;
Обеспечивает транспорт веществ;
Обеспечивает поддержание
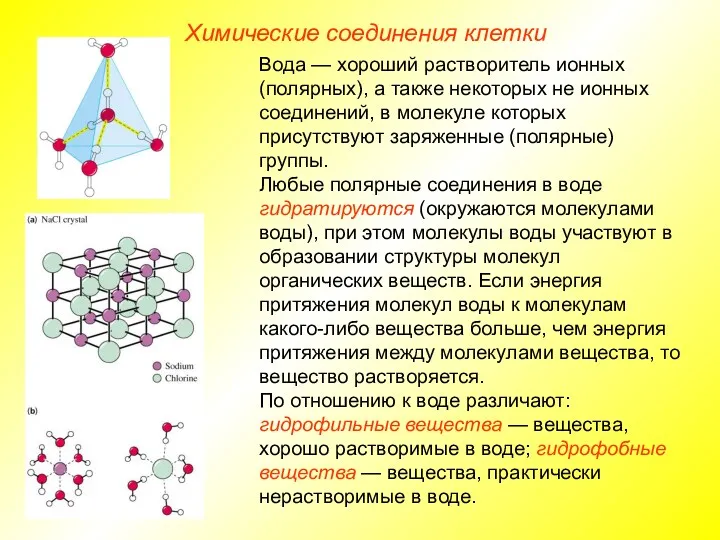
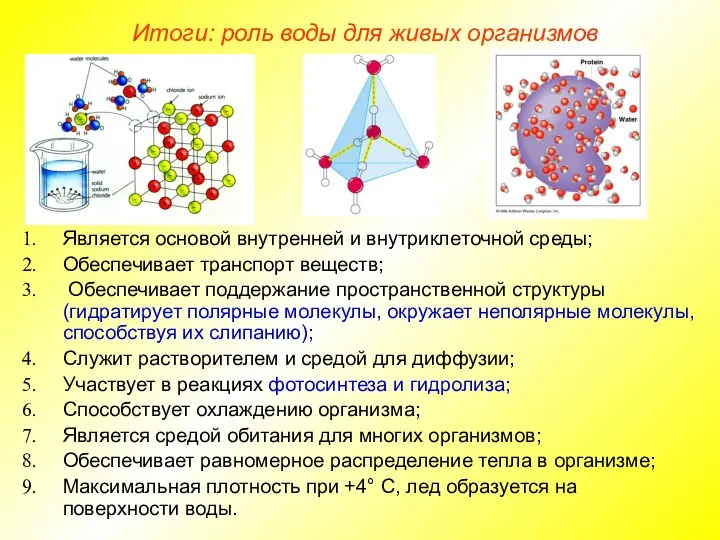
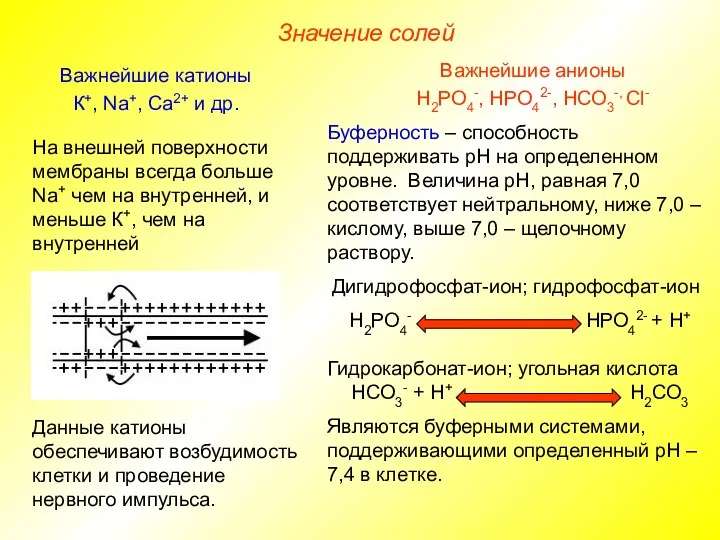
пространственной структуры (гидратирует полярные молекулы, окружает неполярные молекулы, способствуя их слипанию);
Служит растворителем и средой для диффузии;
Участвует в реакциях фотосинтеза и гидролиза;
Способствует охлаждению организма;
Является средой обитания для многих организмов;
Обеспечивает равномерное распределение тепла в организме;
Максимальная плотность при +4° С, лед образуется на поверхности воды.
Итоги: роль воды для живых организмов




 Protein and amino acid metabolism
Protein and amino acid metabolism Спирты. Лекция
Спирты. Лекция Свойства НЦ
Свойства НЦ Марганец. Железо
Марганец. Железо Фосфор и его соединения
Фосфор и его соединения Основні класи неорганічних сполук
Основні класи неорганічних сполук Спектроскопия лазерных кристаллов
Спектроскопия лазерных кристаллов Соли: карбонаты, галоиды, сульфаты
Соли: карбонаты, галоиды, сульфаты Основы электрохимии
Основы электрохимии Генетическая связь между классами неорганических соединений
Генетическая связь между классами неорганических соединений Теплові прояви механічної, електричної та хімічної енергії
Теплові прояви механічної, електричної та хімічної енергії Окислительно-восстановительные реакции. Лабораторная работа
Окислительно-восстановительные реакции. Лабораторная работа Получение высокодисперсных проводящих оксидов - носителей платинового катализатора для низкотемпературных топливных элементов
Получение высокодисперсных проводящих оксидов - носителей платинового катализатора для низкотемпературных топливных элементов Смог и его виды
Смог и его виды Окисно-відновні реакції у природі і промисловості
Окисно-відновні реакції у природі і промисловості Каменный уголь. Фенол
Каменный уголь. Фенол Оксиды. Бинарное соединение. Степень окисления у неметаллов
Оксиды. Бинарное соединение. Степень окисления у неметаллов Алкадиены
Алкадиены Химия и повседневная жизнь человека
Химия и повседневная жизнь человека Электрохимические накопители энергии
Электрохимические накопители энергии Непредельные углеводороды
Непредельные углеводороды Mercury. Mercury cycle
Mercury. Mercury cycle Валентність хімічних елементів
Валентність хімічних елементів Реакции ионного обмена
Реакции ионного обмена Коллоидная химия
Коллоидная химия Природный и попутный нефтяные газы
Природный и попутный нефтяные газы Алкины. Гомологический ряд
Алкины. Гомологический ряд Физические и химические явления. Условия течения и признаки химических реакций
Физические и химические явления. Условия течения и признаки химических реакций