Слайд 2

ХИМИЧЕСКИЕ РЕАКЦИИ - превращения одних веществ в другие, отличные по химическому
составу и (или) строению.
При химических реакциях обязательно происходит изменение веществ, при котором рвутся старые и образуются новые связи между атомами.
Слайд 3

ХИМИЧЕСКОЕ УРАВНЕНИЕ – запись химической реакции с помощью формул реагентов с
указанием их относительных количеств (в молях).
Закон сохранения массы веществ (1756 год.): Масса веществ, вступивших в реакцию, равна массе веществ, получившихся в результате её.
Слайд 4

ПРИЗНАКИ ХИМИЧЕСКИХ РЕАКЦИЙ
Мы можем судить о протекании химической реакции по различным
сопровождающим ее признакам.
Выделение (поглощение) тепла; свечение.
Изменение окраски.
Выпадение осадка.
Растворение осадка.
Выделение газа.
Слайд 5

ОПЫТ: ОБУГЛИВАНИЕ САХАРА, ДРЕВЕСИНЫ
Концентрированная серная кислота (H2SO4) – сильный окислитель.
C+2H2SO4→CO2↑+2SO2↑+H2O
Слайд 6

Реакция обмена:
Na2CO3+ CaCl2↑→Ca CO3↓+2NaCl
ОПЫТ: ВЫПАДЕНИЕ ОСАДКА
Слайд 7

ОПЫТ: РАСТВОРЕНИЕ ОСАДКА, ВЫДЕЛЕНИЕ ГАЗА
Реакция обмена:
CaCO3+2HCl→ CaCl2+ CO2↑+ H2O
Слайд 8

ГОРЕНИЕ, физико-химический процесс, при котором превращение вещества сопровождается интенсивным выделением энергии
и тепло- и массообменом с окружающей средой.
Слайд 9

Слайд 10

Слайд 11

ПРОВЕРЬ СЕБЯ!!!
Составь уравнения реакций и укажи, какой признак реакции характеризует каждую
из них:
NaOH+H2SO4→
CuCl2+KOH→
H2SO4+Cu(OH)2→
K2CO3+HCl→










 Угарный газ
Угарный газ Коррозия и защита строительных материалов
Коррозия и защита строительных материалов Простые вещества. Игра Счастливый случай
Простые вещества. Игра Счастливый случай Химия в повседневной жизни человека
Химия в повседневной жизни человека Жидкокристаллические композиты ЖКК. Керамические композиционные материалы (ККМ). Углерод-углеродные композиционные (УУКМ)
Жидкокристаллические композиты ЖКК. Керамические композиционные материалы (ККМ). Углерод-углеродные композиционные (УУКМ)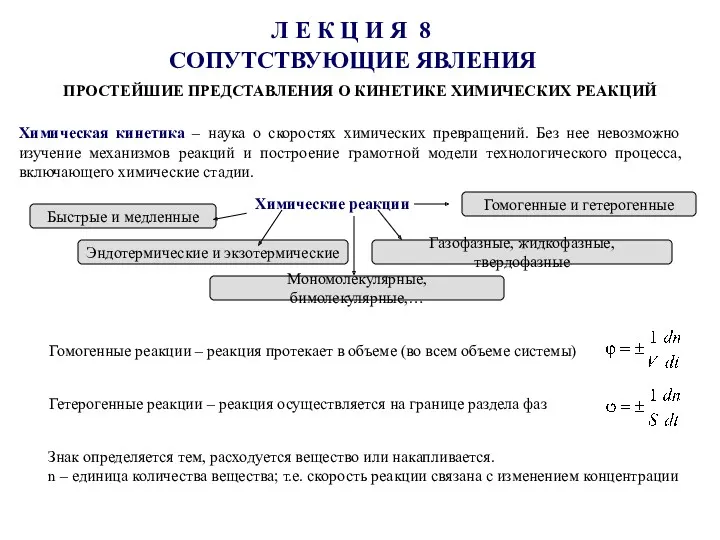 Простейшие представления о кинетике химических реакций
Простейшие представления о кинетике химических реакций Органическая химия
Органическая химия Кинетическое уравнение математическая запись закона действующих масс
Кинетическое уравнение математическая запись закона действующих масс Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Необоротні і оборотні хімічні процеси. Хімічна рівновага
Необоротні і оборотні хімічні процеси. Хімічна рівновага Химический элемент V группы: сурьма
Химический элемент V группы: сурьма Интоксикация ртутью
Интоксикация ртутью Качественные реакции на органические вещества
Качественные реакции на органические вещества Crystal Defects and Noncrystalline Structure–Imperfection
Crystal Defects and Noncrystalline Structure–Imperfection Аномальные свойства воды – основа жизни на Земле
Аномальные свойства воды – основа жизни на Земле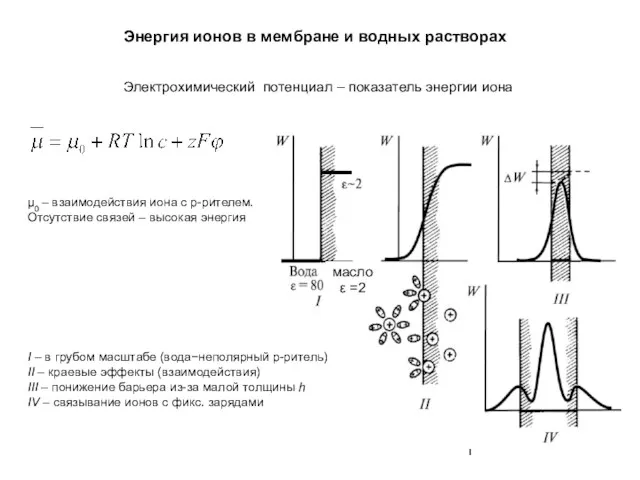 Энергия ионов в мембране и водных растворах
Энергия ионов в мембране и водных растворах Основные особенности композитов по сравнению с традиционными материалами
Основные особенности композитов по сравнению с традиционными материалами Карбонильные соединения
Карбонильные соединения Углерод. Физические и химические свойства
Углерод. Физические и химические свойства Химическая связь
Химическая связь Металлы II группы главной подгруппы
Металлы II группы главной подгруппы Паровые зоны в гидротермальных системах
Паровые зоны в гидротермальных системах Алкадиены. Диеновые углеводороды
Алкадиены. Диеновые углеводороды Состояние атмосферного воздуха в Ярославской области
Состояние атмосферного воздуха в Ярославской области Теплота горения
Теплота горения Ionic polymerization
Ionic polymerization Химия. Изучение жиров
Химия. Изучение жиров Сутектік көрсеткіш ph. Тұздар гидролизі
Сутектік көрсеткіш ph. Тұздар гидролизі