Содержание
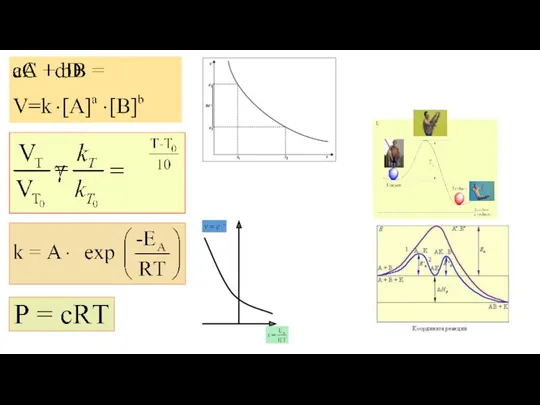
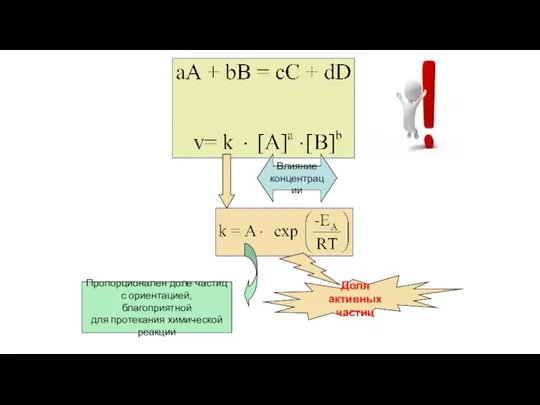
- 2. Кинетическое уравнение математическая запись закона действующих масс
- 3. Расчет температурного коэффициента
- 4. Уравнение Аррениуса k – константа скорости химической реакции (константа в уравнении основного постулата кинетики) ЕА –
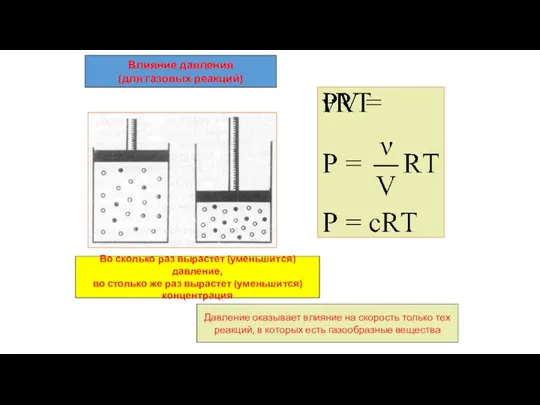
- 7. Во сколько раз вырастет (уменьшится) давление, во столько же раз вырастет (уменьшится) концентрация Давление оказывает влияние
- 9. Задача 1. Найти значение константы скорости реакции если при начальных концентрациях [А]0=0,05 и [В]0=0,01 М скорость
- 12. Скачать презентацию





 Стратегия химической промышленности
Стратегия химической промышленности Chemical reaction rate. Influence of conditions on the rate of chemical reactions. Catalysis. Topic 3.2
Chemical reaction rate. Influence of conditions on the rate of chemical reactions. Catalysis. Topic 3.2 Химия в повседневной жизни человека
Химия в повседневной жизни человека Емтихан сұрақтары
Емтихан сұрақтары Managing chemicals. Green chemistry for every laboratory
Managing chemicals. Green chemistry for every laboratory Классификация химических реакций
Классификация химических реакций 20230419_azot
20230419_azot Органикалық қосылыстар
Органикалық қосылыстар Хозяйственные товары из пластических масс
Хозяйственные товары из пластических масс Металлы побочных подгрупп
Металлы побочных подгрупп Периодический закон и система элементов Д.И. Менделеева
Периодический закон и система элементов Д.И. Менделеева Минералы горных пород
Минералы горных пород Охрана труда в кабинете (лаборатории) химии образовательного учреждения
Охрана труда в кабинете (лаборатории) химии образовательного учреждения Водородная связь
Водородная связь Хроматография. Классификации хроматографических методов
Хроматография. Классификации хроматографических методов Амины. Анилин
Амины. Анилин Шкала не Мооса
Шкала не Мооса Растворы. Лекция №4
Растворы. Лекция №4 Оценка опасности взрыва горючих газов
Оценка опасности взрыва горючих газов Хімічні властивості насичених одноатомних спиртів. Одержання етанолу
Хімічні властивості насичених одноатомних спиртів. Одержання етанолу Нефть, её производство, авиационное и дизельное топливо
Нефть, её производство, авиационное и дизельное топливо Органическая химия. Лекция 13
Органическая химия. Лекция 13 Положение металлов в периодической системе. Металлическая связь. Металлическая решетка. Общие физические свойства металлов
Положение металлов в периодической системе. Металлическая связь. Металлическая решетка. Общие физические свойства металлов Вуглеводні. Підсумковий урок 9 клас
Вуглеводні. Підсумковий урок 9 клас Химия. D-элементтер
Химия. D-элементтер сложные эфиры
сложные эфиры Күрделі белоктар
Күрделі белоктар Простые вещества. Сложные вещества
Простые вещества. Сложные вещества