Содержание
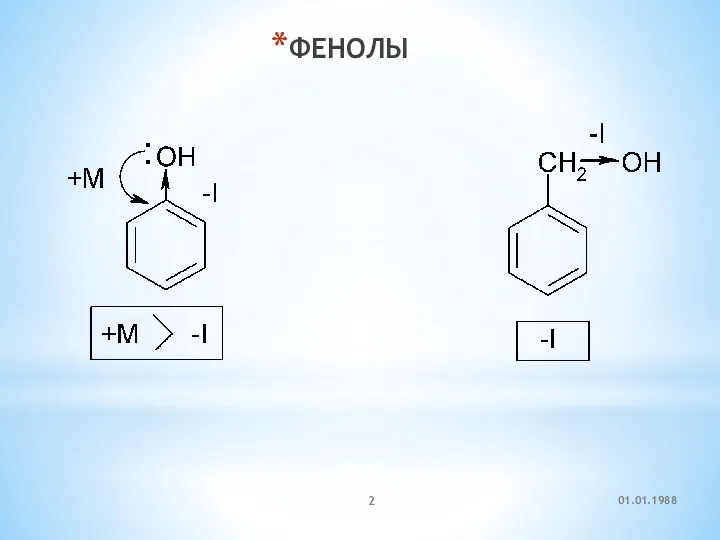
- 2. ФЕНОЛЫ 01.01.1988
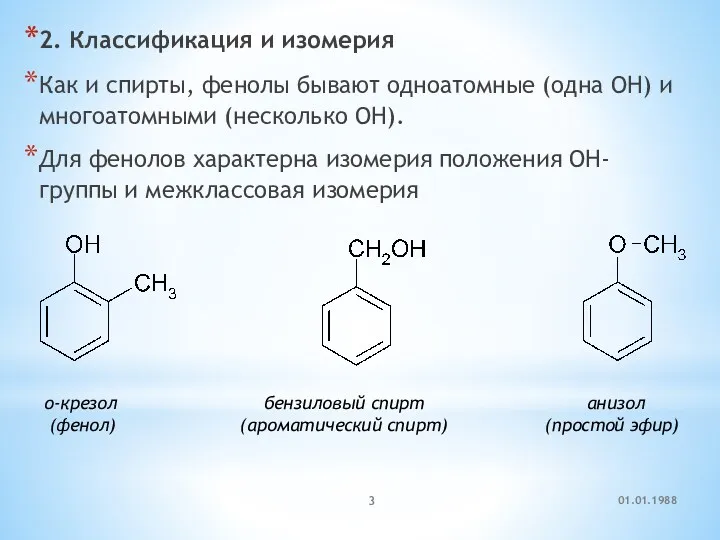
- 3. 2. Классификация и изомерия Как и спирты, фенолы бывают одноатомные (одна OH) и многоатомными (несколько OH).
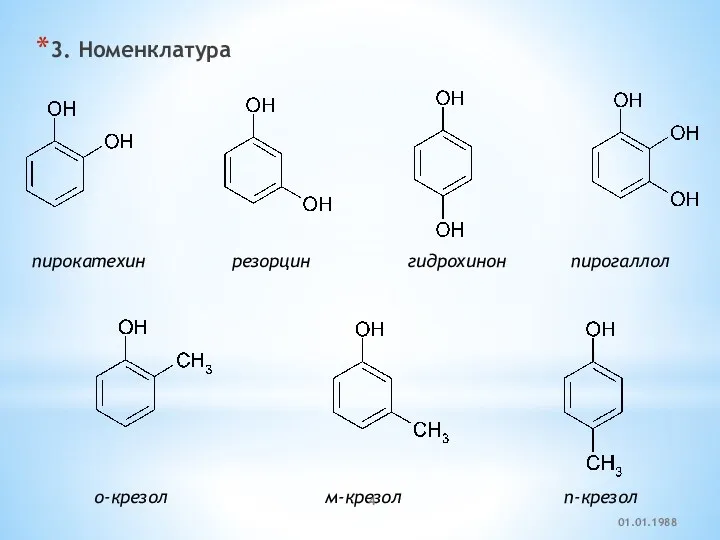
- 4. 3. Номенклатура пирокатехин резорцин гидрохинон пирогаллол о-крезол м-крезол п-крезол 01.01.1988
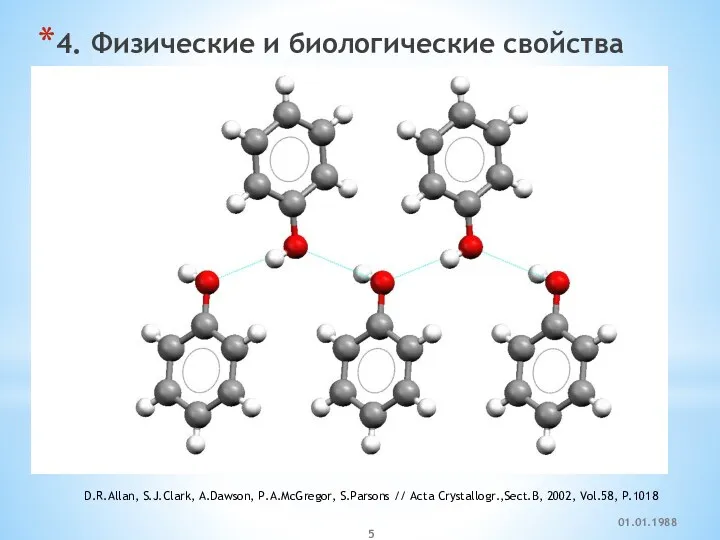
- 5. 4. Физические и биологические свойства D.R.Allan, S.J.Clark, A.Dawson, P.A.McGregor, S.Parsons // Acta Crystallogr.,Sect.B, 2002, Vol.58, P.1018
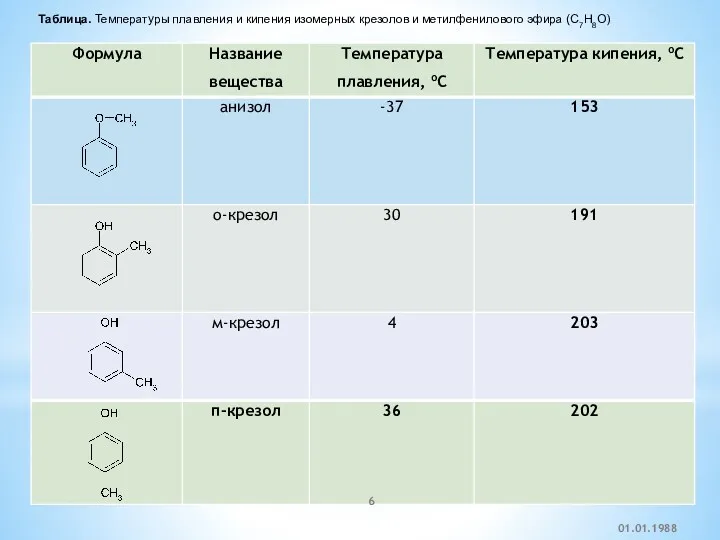
- 6. Таблица. Температуры плавления и кипения изомерных крезолов и метилфенилового эфира (C7H8O) 01.01.1988
- 7. Фенол очень токсичен, при попадании на кожу вызывает ожоги. Фенол обладает хорошими дезинфицирующими свойствами; это было
- 8. 01.01.1988
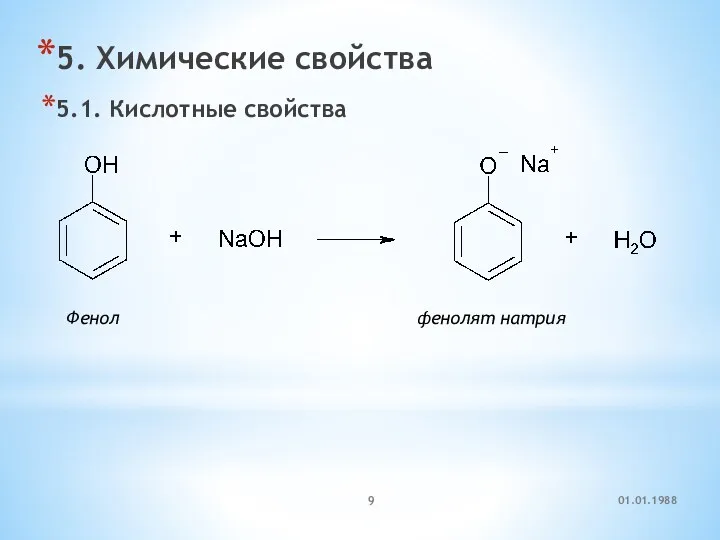
- 9. 5. Химические свойства 5.1. Кислотные свойства Фенол фенолят натрия 01.01.1988
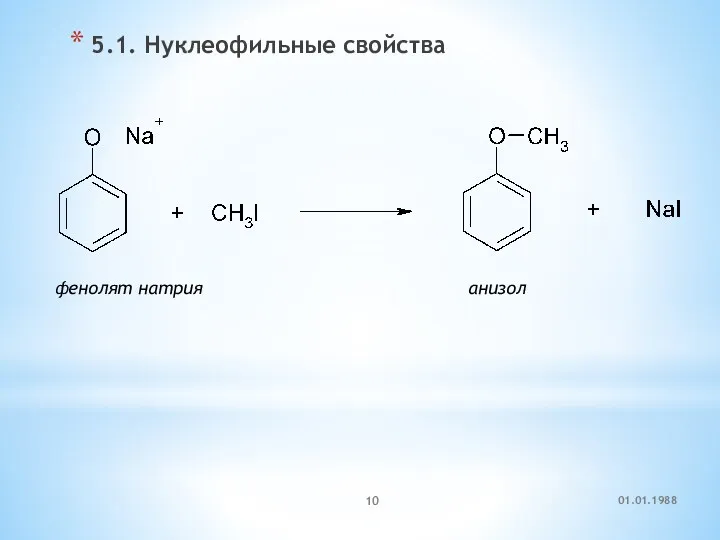
- 10. 5.1. Нуклеофильные свойства фенолят натрия анизол 01.01.1988
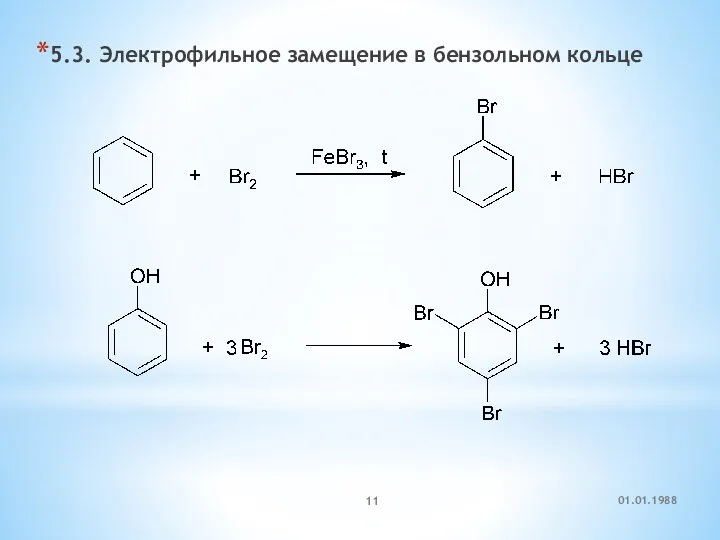
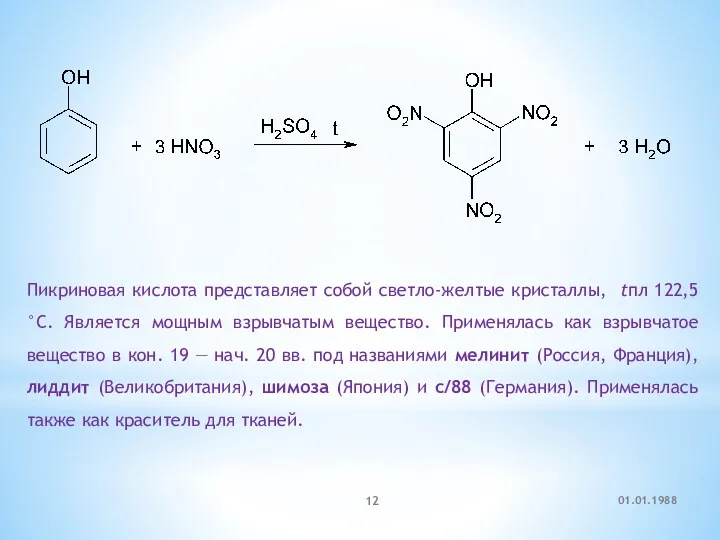
- 11. 5.3. Электрофильное замещение в бензольном кольце 01.01.1988
- 12. Пикриновая кислота представляет собой светло-желтые кристаллы, tпл 122,5 °С. Является мощным взрывчатым вещество. Применялась как взрывчатое
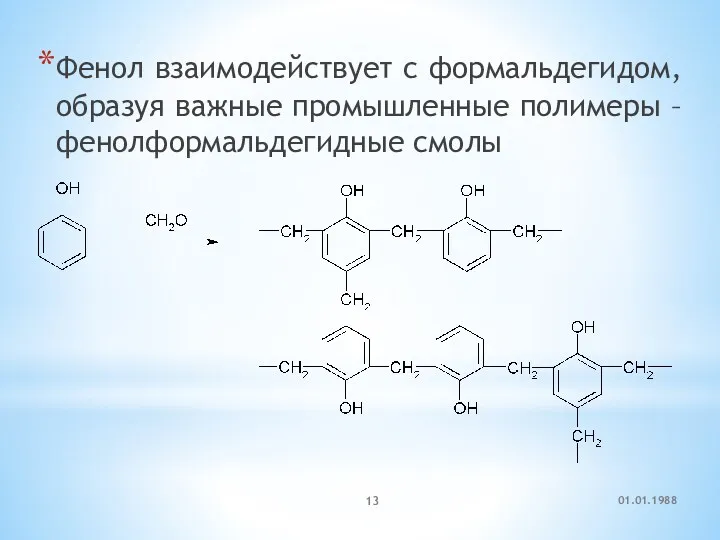
- 13. Фенол взаимодействует с формальдегидом, образуя важные промышленные полимеры – фенолформальдегидные смолы 01.01.1988
- 14. 01.01.1988 Фенолформальдегидные смолы являются вязкими жидкостями или твердыми веществами. Отвержденные фенолоформальдегидные смолы обладают электроизоляционными и механическими
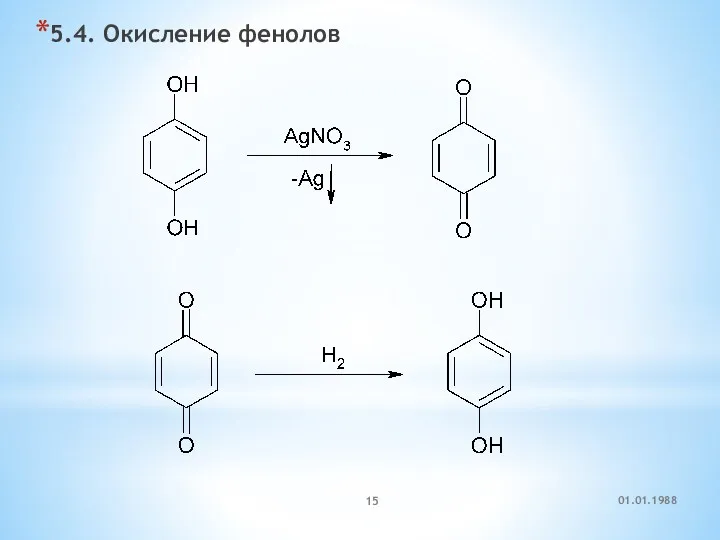
- 15. 5.4. Окисление фенолов 01.01.1988
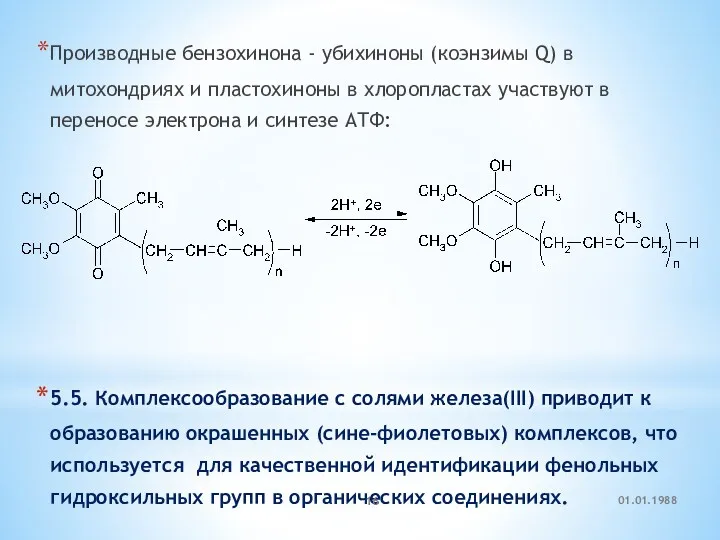
- 16. Производные бензохинона - убихиноны (коэнзимы Q) в митохондриях и пластохиноны в хлоропластах участвуют в переносе электрона
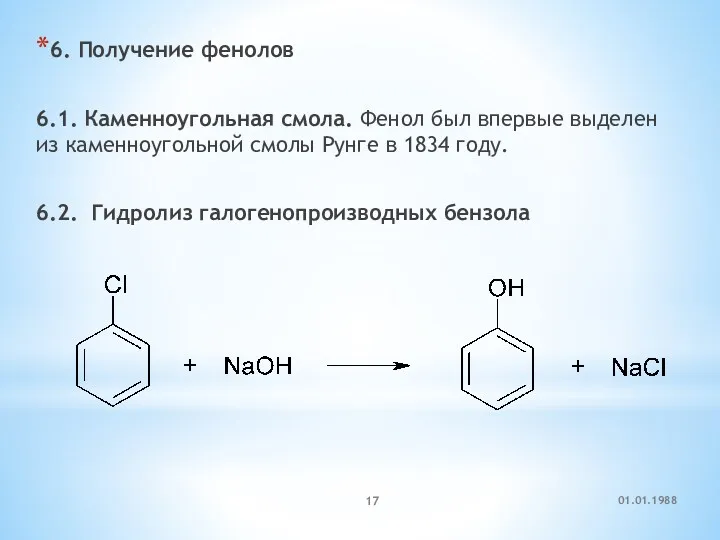
- 17. 6. Получение фенолов 6.1. Каменноугольная смола. Фенол был впервые выделен из каменноугольной смолы Рунге в 1834
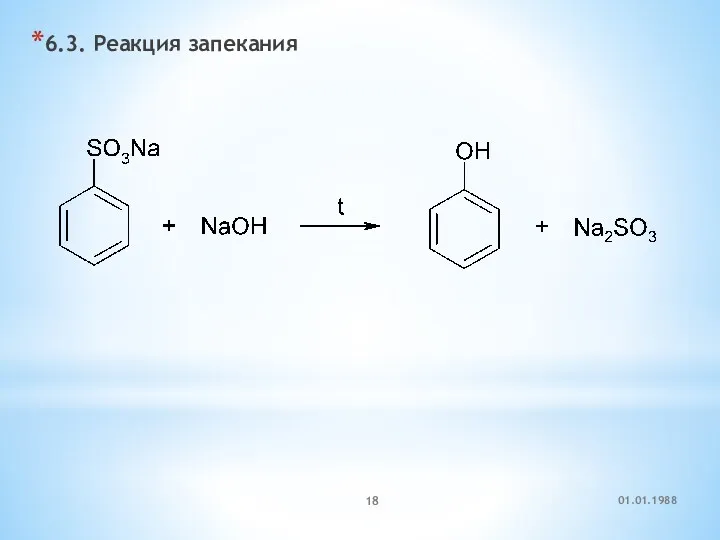
- 18. 6.3. Реакция запекания 01.01.1988
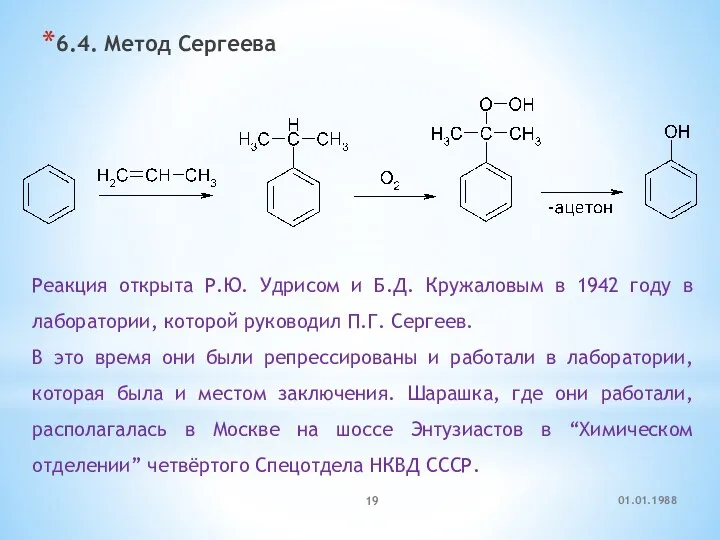
- 19. 6.4. Метод Сергеева Реакция открыта Р.Ю. Удрисом и Б.Д. Кружаловым в 1942 году в лаборатории, которой
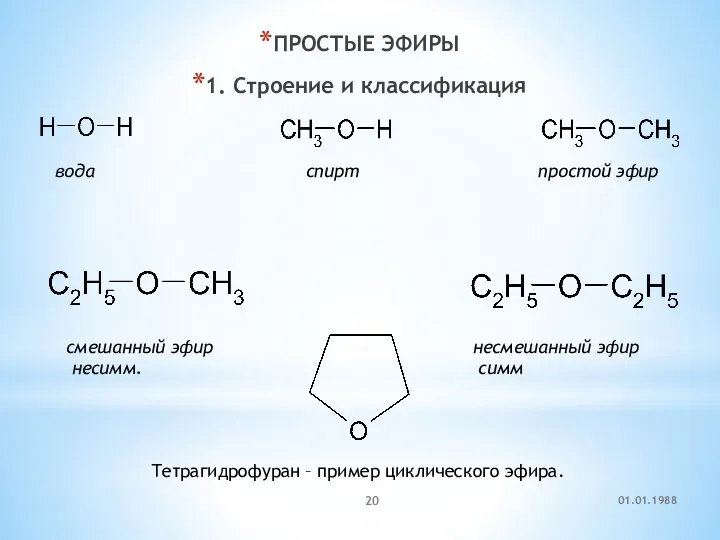
- 20. ПРОСТЫЕ ЭФИРЫ 1. Строение и классификация вода спирт простой эфир смешанный эфир несмешанный эфир несимм. симм
- 21. 2. Номенклатура Обычно простые эфиры называют по радикально-функциональной номенклатуре, перечисляя радикалы в виде прилагательного и добавляя
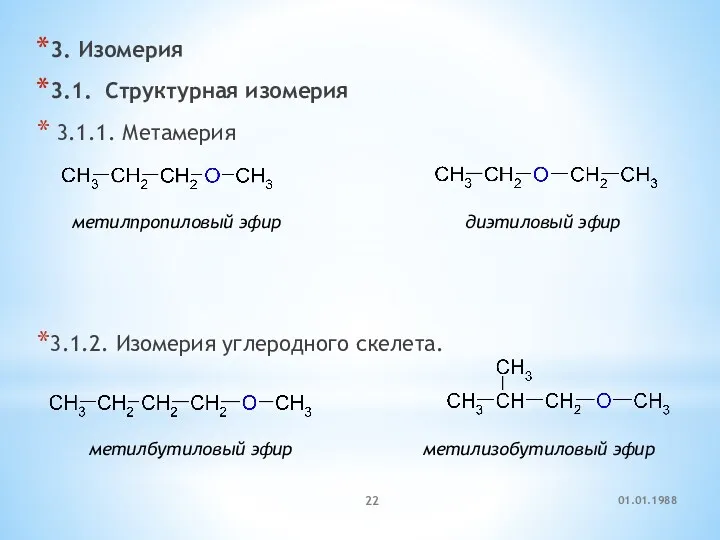
- 22. 3. Изомерия 3.1. Cтруктурная изомерия 3.1.1. Метамерия 3.1.2. Изомерия углеродного скелета. метилпропиловый эфир диэтиловый эфир метилбутиловый
- 23. 3.1.3. Межклассовая изомерия этанол диметиловый эфир 01.01.1988
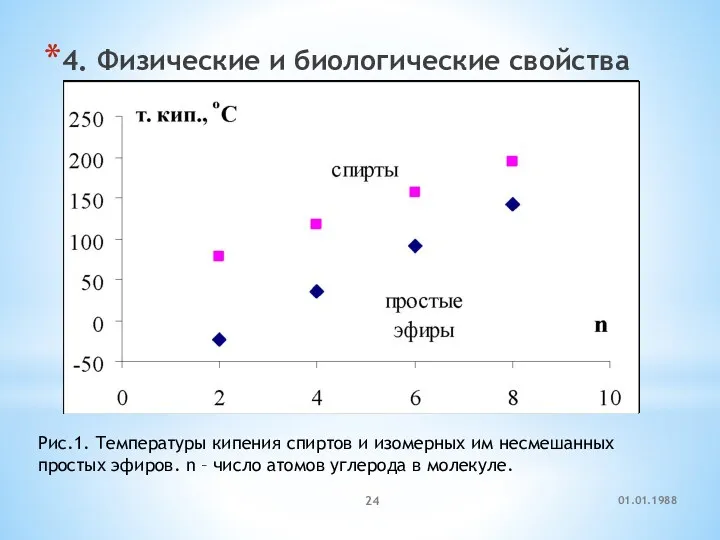
- 24. 4. Физические и биологические свойства Рис.1. Температуры кипения спиртов и изомерных им несмешанных простых эфиров. n
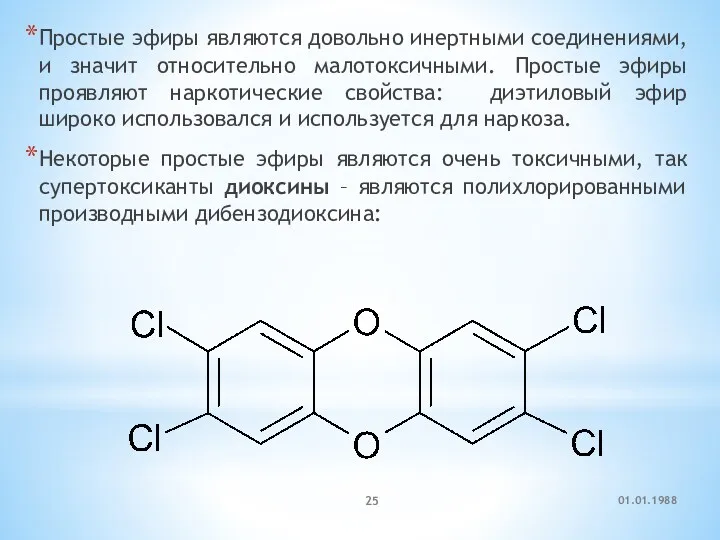
- 25. Простые эфиры являются довольно инертными соединениями, и значит относительно малотоксичными. Простые эфиры проявляют наркотические свойства: диэтиловый
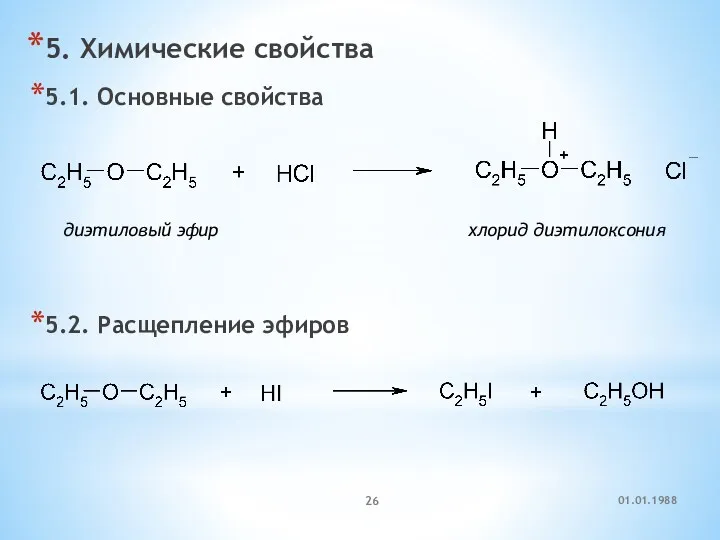
- 26. 5. Химические свойства 5.1. Основные свойства 5.2. Расщепление эфиров диэтиловый эфир хлорид диэтилоксония 01.01.1988
- 27. 5.3. Окисление эфиров При длительном контакте с кислородом в эфире накапливаются чрезвычайно взрывчатые гидроперекиси, которые могут
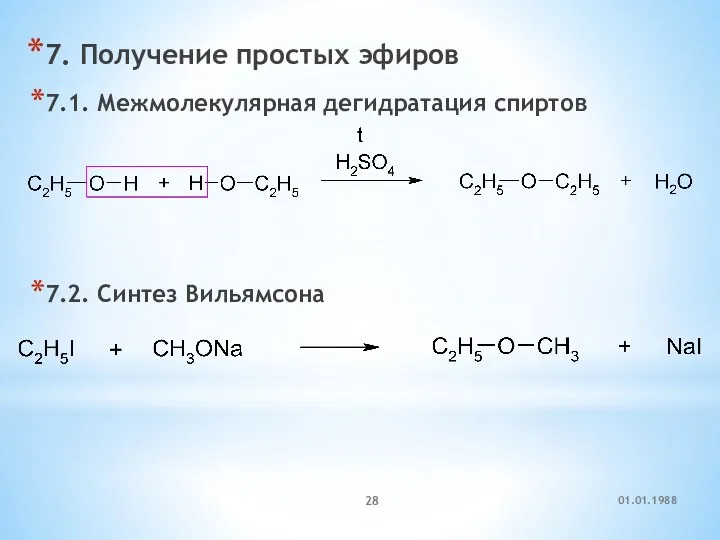
- 28. 7. Получение простых эфиров 7.1. Межмолекулярная дегидратация спиртов 7.2. Синтез Вильямсона 01.01.1988
- 30. Скачать презентацию






 Обмен хромопротеинов в организме
Обмен хромопротеинов в организме Серная кислота. ОХТ, лекция №7
Серная кислота. ОХТ, лекция №7 Возраст в геологии
Возраст в геологии Серная кислота и её свойства
Серная кислота и её свойства Альтернативная елочка из кристаллов
Альтернативная елочка из кристаллов Химическая взрывчатка
Химическая взрывчатка Нитраттарды қолдану
Нитраттарды қолдану Ағзаның барлық жасушасындағы белок алмасу. Аминқышқылдарының дезаминденуі, пурин және пиримидиндердің ыдырауынан
Ағзаның барлық жасушасындағы белок алмасу. Аминқышқылдарының дезаминденуі, пурин және пиримидиндердің ыдырауынан Основи. Хімія
Основи. Хімія Cromatografie de lichide de inalta performanta cuplata cu spectrometrie de masă
Cromatografie de lichide de inalta performanta cuplata cu spectrometrie de masă Обмен нуклеопротеинов
Обмен нуклеопротеинов Теория сплавов
Теория сплавов Окислительно-восстановительные реакции. Урок в 11 классе
Окислительно-восстановительные реакции. Урок в 11 классе Сплавы железа с углеродом: стали и чугуны
Сплавы железа с углеродом: стали и чугуны Применение родия (Rh)
Применение родия (Rh)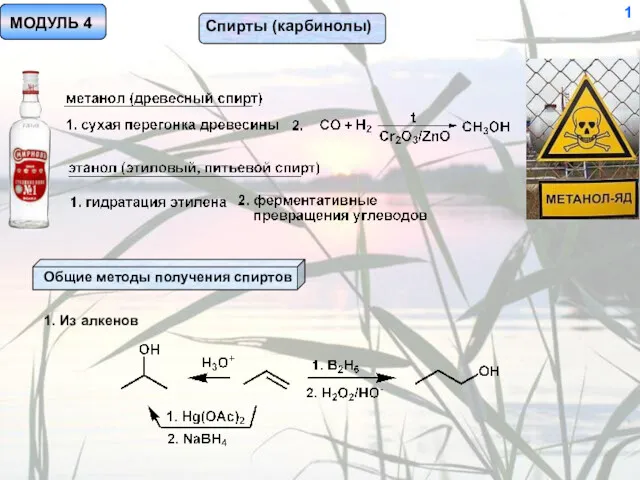 Спирты (карбинолы)
Спирты (карбинолы) Гідроліз солей
Гідроліз солей Щелочные металлы. Периодическая система химических элементов Д.И. Менделеева
Щелочные металлы. Периодическая система химических элементов Д.И. Менделеева Застосування неметалів
Застосування неметалів Биогенные элементы периодической системы
Биогенные элементы периодической системы Тепловой эффект химической реакции
Тепловой эффект химической реакции Металдар мен құймалар әр түрлі заттармен жанасқанда, олармен әрекеттесіп, химиялық қосылыстар түзеді
Металдар мен құймалар әр түрлі заттармен жанасқанда, олармен әрекеттесіп, химиялық қосылыстар түзеді Кислотно-основное титрование
Кислотно-основное титрование Карбоновые кислоты
Карбоновые кислоты Минералогия литофильных редких элементов. Цезий и рубидий
Минералогия литофильных редких элементов. Цезий и рубидий Одноатомные и многоатомные спирты
Одноатомные и многоатомные спирты Самоспалахування. Фактори, що впливають на температуру самоспалахування. Лекція 5
Самоспалахування. Фактори, що впливають на температуру самоспалахування. Лекція 5 Периодические изменения свойств химических элементов
Периодические изменения свойств химических элементов