Содержание
- 2. Циклоалканы циклопаpафины нафтены цикланы полиметилены предельные углеводороды с замкнутой (циклической) углеродной цепью.
- 3. Цель урока: Рассмотреть отличительные особенности циклопарафинов Знать физические и химические свойства циклопарафинов в сравнении с предельными
- 4. Понятие о циклопарафинах: если от молекулы бутана СН3 - CH2 – CH 2 – CH3 отщепить
- 5. Что произойдёт с остатком молекулы? атомы углерода, соединившись за счёт Крайние свободных связей, образуют замкнутую структуру:
- 6. Такие углеводороды называются циклоалканами (циклопарафинами)
- 7. Молекулы циклопарафинов могут содержать боковые цепи:
- 8. Структурные формулы циклоалканов обычно записывают в сокращенном виде, используя геометрическую форму цикла и опуская символы атомов
- 9. Являются ли данные углеводороды насыщенными? Почему? Какова общая формула циклопарафинов? CnH2n Почему у циклопарафинов на два
- 10. Строение циклоалканов
- 11. Сходство с предельными углеводородами: Каждый атом углерода в ЦИКЛОАЛКАНАХ находится в состоянии sp3-гибридизации и образует четыре
- 12. sp3-гибридизациия
- 13. Отличие от предельных: Углы между связями зависят от размера цикла: чем меньше цикл, тем меньше угол,
- 14. Простейший циклоалкан – циклопpопан С3Н6 – представляет собой плоский трехчленный карбоцикл Валентные углы в циклопропане и
- 16. Остальные циклы имеют неплоское строение вследствие стремления атомов углерода к образованию тетраэдрических валентных углов.
- 17. Это приводит к большой напряженности таких циклов и их стремлению к раскрытию под действием реагентов.
- 18. Изомерия циклоалканов: -структурная -пространственная -межклассовая
- 19. Структурная, связанная с: изомерией боковых цепей:
- 20. -числом углеродных атомов в кольце:например, для циклоалкана С5Н10 существуют вещества:
- 21. -положением заместителей в кольце
- 22. Межклассовая с алкенами
- 23. Пространственная изомерия (геометрическая цис-транс-изомерия) у некоторых замещённых циклоалканов объясняется отсутствием свободного вращения вокруг связей С –
- 25. Названия циклоалканов: По правилам международной номенклатуры в циклоалканах главной считается цепь углеродных атомов, образующих цикл. Название
- 26. Как назвать циклопарафин 1,2-диметилциклобутан, а не 2,3-диметилциклобутан, или 3,4-диметилциклобутан.
- 27. Физические свойства: Температура плавления, кипения и плотность больше, чем у соответствующих алканов; Чем больше размер цикла,
- 28. Физические свойства некоторых циклоалканов: Соединение t°пл., t°кип., Циклопропан -126,9 -33 Метилциклопропан -177,2 0,7 Циклобутан - 80
- 29. Химические свойства циклоалканов Зависят от размера цикла, определяющего его устойчивость.
- 30. Низшие циклоалканы (циклопропан и циклобутан) склонны к реакциям присоединения, т.е. сходны в этом отношении с алкенами.
- 31. Гидрирование. Циклопропан, циклобутан и даже циклопентан могут присоединять водород, давая соответствующие нормальные алканы. Присоединение происходит при
- 32. Галогенирование и гидрогалогенирование Циклопропан и его производные присоединяют галогены и галогеноводороды:
- 33. Для циклоалканов (С5 и выше) характерны реакции замещения.
- 34. Дегидрирование при нагревании с катализаторами (образуются ароматические углеводороды)
- 35. Полное окисление (горение) с образованием воды и углекислого газа t0 2 С5Н10 + 15 О2 10
- 36. Получение циклоалканов. 1. При переработке нефти, (отсюда одно из названий – нафтены), выделяют главным образом циклоалканы
- 37. Этим путем можно получать циклоалканы заданного строения. Например, для синтеза 1,3-диметилциклопентана следует использовать 1,5-дигалоген-2,4-диметилпентан:
- 38. Циклогексан и его гомологи получают гидрированием бензола и его гомологов
- 39. Применение циклоалканов. Циклопентан, циклогексан, метилциклогексан, их производные при ароматизации нефти превращаются в ароматические у.в. Циклопропан –
- 41. Скачать презентацию






































 Карбоновые кислоты. Тест
Карбоновые кислоты. Тест Кремний и его соединения
Кремний и его соединения Водородная связь
Водородная связь Природные источники углеводородов, их переработка, применение и экологические проблемы
Природные источники углеводородов, их переработка, применение и экологические проблемы Металлы и их свойства. Способы получения
Металлы и их свойства. Способы получения Органическая химия. Вещества
Органическая химия. Вещества Магматизм. (Лекция 6)
Магматизм. (Лекция 6) Кислород
Кислород Спроби класифікації хімічних елементів
Спроби класифікації хімічних елементів Алкены (олефины, этиленовые углеводороды)
Алкены (олефины, этиленовые углеводороды) Прочность полимеров
Прочность полимеров Амфотерные органические и неорганические соединения
Амфотерные органические и неорганические соединения Буферные растворы
Буферные растворы Місце хімії серед наук про природу
Місце хімії серед наук про природу Химические волокна
Химические волокна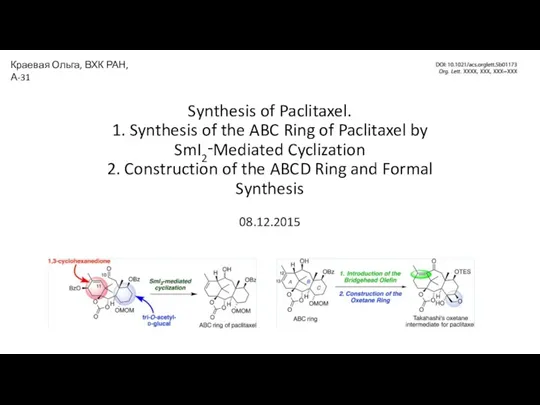 Synthesis of Paclitaxel
Synthesis of Paclitaxel Строение атома. 8 класс
Строение атома. 8 класс Лекция 3. Разновидности химических связей
Лекция 3. Разновидности химических связей Витамины. Ашылу тарихы
Витамины. Ашылу тарихы ГИА-9 Химия. А4
ГИА-9 Химия. А4 Массовая и объемная доли компонентов смеси (раствора)
Массовая и объемная доли компонентов смеси (раствора) Классификация органических соединений, углеводородов
Классификация органических соединений, углеводородов Рідкі кристали
Рідкі кристали Спирты
Спирты Химические уравнения
Химические уравнения Вещества молекулярного и немолекулярного строения
Вещества молекулярного и немолекулярного строения Применение алюминия и его сплава в машиностроении
Применение алюминия и его сплава в машиностроении Химическая связь. 8 класс
Химическая связь. 8 класс