Содержание
- 2. “Все изменения,которые случаются в действительности,находятся в таком состоянии,что сколь от одного тела отнимается,столько прибавляется к другому,так
- 3. Современная формулировка закона сохранения массы веществ: Масса веществ,вступивших в химическую реакцию,равна массе веществ,получившихся в результате её.
- 5. Химическое уравнение – запись химической реакции при помощи химических формул веществ и коэффициентов.
- 6. Пример: Составить уравнение реакции взаимодействия фосфора и кислорода.
- 7. 1. В левой части уравнения записать формулы исходных веществ (Формулы простых газообразных веществ состоят из двух
- 8. 2. В правой части уравнения записать формулы продуктов реакции. 3. Определить атомов, какого элемента в левой
- 9. 4. Соединить фигурной стрелкой атомы этого элемента в левой и правой частях. = P O2 +
- 10. 5. Определить Н.О.К. чисел атомов в левой и правой частях уравнения. 6. Записать Н.О.К. в квадратике
- 11. 7.Разделить Н.О.К. на число атомов каждого соединенного элемента. 8. Записать полученный коэффициент перед формулой. = P
- 12. 9. Определить, есть ли еще не уравненные (не соединенные атомы): а) Если есть, то вернись к
- 13. Расставьте коэффициенты в уравнениях химических реакций: 1) Na+Cl2→NaCl 2) Al+S→Al2S3 3) Ba+O2→BaO 4) P + Cl2
- 14. «Единственный путь, ведущий к знанию, - это деятельность» Б.Шоу
- 16. Скачать презентацию
 Щелочноземельные металлы Положение в периодической таблице
Щелочноземельные металлы Положение в периодической таблице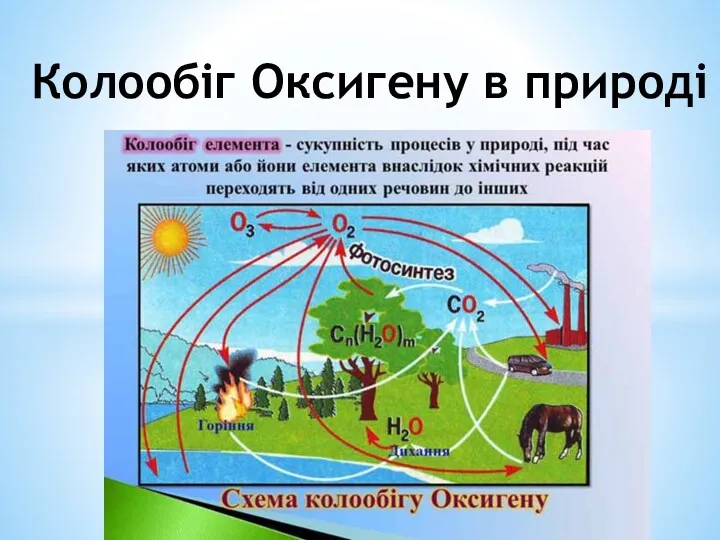 Колообіг оксигену в природі
Колообіг оксигену в природі Кислоты. Серная кислота-H₂SO₄
Кислоты. Серная кислота-H₂SO₄ Прикладная химия. Теплоперенос в химических реакторах и теплообменники
Прикладная химия. Теплоперенос в химических реакторах и теплообменники Химическая связь
Химическая связь λ-MnO2 as material with pseudocapacitive properties
λ-MnO2 as material with pseudocapacitive properties Металлы побочных подгрупп. Марганец. Хром. (Лекция 15)
Металлы побочных подгрупп. Марганец. Хром. (Лекция 15) Фенолы. Классификация и номенклатура фенолов
Фенолы. Классификация и номенклатура фенолов Basic concepts and laws of chemical thermodynamics
Basic concepts and laws of chemical thermodynamics Сполуки неметалічних елементів з Гідрогеном
Сполуки неметалічних елементів з Гідрогеном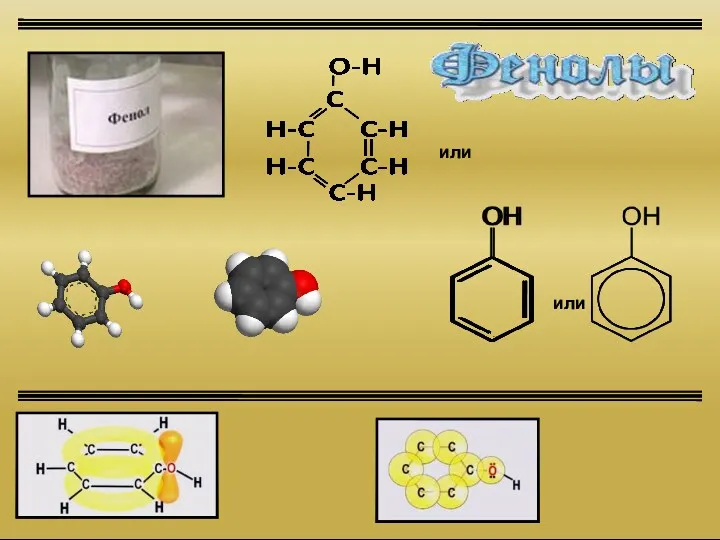 Фенолы
Фенолы Кондуктометрия. Кондуктометрия әдісі. Электрохимиялық әдістер
Кондуктометрия. Кондуктометрия әдісі. Электрохимиялық әдістер Оксид серы (IV). Сернистая кислота и её соли
Оксид серы (IV). Сернистая кислота и её соли Оксиды
Оксиды Сложные эфиры. Жиры. Мыла. (10 класс)
Сложные эфиры. Жиры. Мыла. (10 класс) Продолжение лекции Химическая связь
Продолжение лекции Химическая связь Электрохимия. Окислительно-восстановительные реакции
Электрохимия. Окислительно-восстановительные реакции Сероводород. Сульфиды
Сероводород. Сульфиды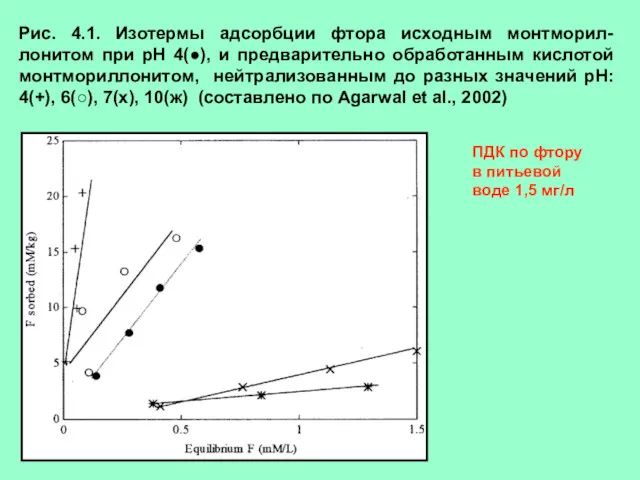 Содержание ионов в растворе
Содержание ионов в растворе Атомы и молекулы. Простые и сложные вещества. 6 класс
Атомы и молекулы. Простые и сложные вещества. 6 класс Качественные реакции на функциональные группы. Классификация функциональных групп
Качественные реакции на функциональные группы. Классификация функциональных групп Ask the right question to find the best answer
Ask the right question to find the best answer Резина и её свойства . Полимеры и их использование
Резина и её свойства . Полимеры и их использование Кислоты. Общая характеристика, химические свойства
Кислоты. Общая характеристика, химические свойства Классификация химических реакций
Классификация химических реакций Генетическая взаимосвязь органических веществ. Задание 38
Генетическая взаимосвязь органических веществ. Задание 38 БАЗ синтездеудің химиялық технологиясы Синтетикалық түсінік
БАЗ синтездеудің химиялық технологиясы Синтетикалық түсінік Своя игра Знаешь ли ты химические элементы?
Своя игра Знаешь ли ты химические элементы?