Содержание
- 2. Общие понятия термодинамики Термодинамика – наука, изучающая превращения различных форм энергии друг в друга и устанавливающая
- 3. Термодинамика базируется на четырех основных законах, именуемых нулевым, первым, вторым и третьим законами (началами) термодинамики. Нулевое
- 4. ПОНЯТИЯ ТД Система – тело или группа тел, находящихся во взаимодействии и мысленно обособляемых от окружающей
- 5. Виды систем Гомогенная (однородная) система не имеет внутри поверхностей раздела, отделяющих отдельные ее части (фазы), различающиеся
- 6. Процесс Процесс – переход системы из одного состояния в другое. При этом происходит изменение всех термодинамических
- 7. Состояние системы – это совокупность всех физических и химических свойств системы. Состояние системы описывают термодинамические функции.
- 8. Дипольный момент Теплота (Q) – это внешнее проявление энергообмена частиц в результате хаотичных столкновений между ними.
- 9. Первый закон (начало) термодинамики. Внутренняя энергия системы. Энтальпия системы Первый закон (начало) термодинамики является количественной формулировкой
- 10. Первый закон имеет несколько равноценных формулировок, но все они выражают и ту же суть: неуничтожимость и
- 11. Третья формулировка: Количество теплоты, полученное системой, идет на изменение ее внутренней энергии и совершение работы против
- 12. Внутренняя энергия (U) – это энергия, которая в скрытом виде заключена в каждом теле и зависит
- 13. Тепловой эффект реакции Тепловой эффект реакции можно измерить опытным путем, и определить изменение запаса внутренней энергии
- 14. Наряду с внутренней энергией в термодинамике часто используют термодинамическую функцию состояния – энтальпию системы. Энтальпия системы
- 15. Как для любой функции состояния, для энтальпии системы нельзя определить абсолютное значение, а можно определить только
- 16. Термохимия. Тепловые эффекты химических реакций Любые химические процессы, а также ряд физических превращений веществ (испарение, конденсация,
- 17. Тепловым эффектом химической реакции называется теплота, которая выделяется или поглощается в ходе химической реакции. Стандартным тепловым
- 18. Эндотермические это реакции, при которых происходит поглощение теплоты из окружающей среды. При этом запас внутренней энергии
- 19. Изохорным (QV) тепловым эффектом называют количество теплоты, которое выделяется или поглощается в ходе данного процесса при
- 20. Во всех случаях преобразование части внутренней (химической) энергии в тепловую (или другие виды) и наоборот, тепловой
- 21. С термохимическими уравнениями можно производить все алгебраические действия: складывать, вычитать, умножать, переносить члены и т.д. Тепловые
- 22. Теплотой образования данного соединения называется количество выделяющейся или поглотившейся теплоты при образовании 1 моля его из
- 23. Закон Гесса и следствия из него На основе многочисленных экспериментальных исследований русским академиком Г. И. Гессом
- 24. Из закона Гесса вытекают следствия: 1.Тепловой эффект разложения какого-либо химического соединения равен по абсолютной величине и
- 25. 2. Если совершаются две реакции, приводящие из различных начальных состояний к одинаковым конечным, то разность тепловых
- 26. 3. Если совершаются две реакции, приводящие из одинаковых начальных состояний к различным конечным, то разность между
- 27. 4. Тепловой эффект реакции равен сумме теплот образования продуктов реакции минус сумма теплот образования исходных веществ
- 28. 5. Тепловой эффект реакции равен сумме теплот сгорания исходных веществ минус сумма теплот сгорания продуктов реакции
- 29. Основные формулировки второго закона (начала) термодинамики Первый закон термодинамики характеризует количественное и качественное преобразование внутренней энергии,
- 30. Основные формулировки второго начала термодинамики: Постулат Клаузиуса: теплота не может самопроизвольно переходить от менее нагретого тела
- 31. Свободная и связанная энергии. Энтропия системы Любая форма энергии может полностью преобразовываться в теплоту, но теплота
- 32. Принцип минимума свободной энергии В ходе химической реакции свободная энергия уменьшается и при данных условиях достигает
- 33. Если ΔF > 0, то процесс идет самопроизвольно в обратном направлении; если ΔF если ΔF =
- 34. Энтропия Энтропия – это термодинамическая функция состояния, которая служит мерой неупорядоченности (беспорядка) состояния системы. Состояние системы
- 35. В отличие от других термодинамических функций, можно определить не только изменение, но и абсолютное значение энтропии.
- 36. В изолированных системах самопроизвольно идут такие процессы, которые сопровождаются возрастанием энтропии: ΔS > 0. Это одна
- 37. В общем случае, если ΔS > 0, то процесс идет самопроизвольно в прямом направлении; если ΔS
- 38. Энергия Гиббса, энергия Гельмгольца и направленность химических реакций Энтальпийный и энтропийный факторы, характеризующие две противоположные тенденции
- 39. Энергия Гельмгольца – это максимальная работа, которую может совершить система при равновесном проведении процесса при постоянных
- 40. Энергия Гиббса (Гельмгольца) служит критерием самопроизвольного протекания химической реакции при изобарно-изотермических (изохорно-изотермических) процессах. Химическая реакция принципиально
- 41. При стандартных условиях величины ΔG0 и ΔF0 – справочные. Для реакции общего вида аA + вB
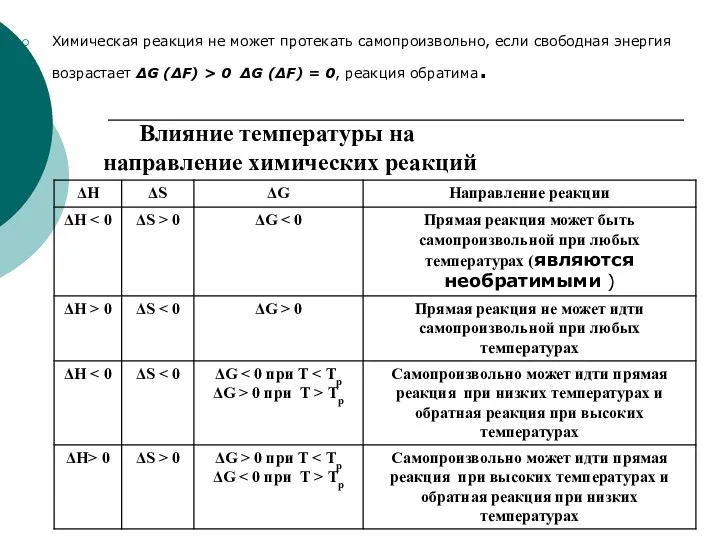
- 42. Химическая реакция не может протекать самопроизвольно, если свободная энергия возрастает ΔG (ΔF) > 0 ΔG (ΔF)
- 43. Для определения температуры (Тр), выше которой происходит смена знака энергии Гиббса реакции, можно воспользоваться условием Тр
- 45. Скачать презентацию









































 Физическая химия дисперсных систем. Лекция 7
Физическая химия дисперсных систем. Лекция 7 Нуклеиновые кислоты. Нуклеотиды
Нуклеиновые кислоты. Нуклеотиды Адсорбция-фазалар бөлу беттерінде жүретін бір компоненттің екінші компонентке сіңуі
Адсорбция-фазалар бөлу беттерінде жүретін бір компоненттің екінші компонентке сіңуі Обобщение по теме Основные классы неорганических веществ. 8 класс
Обобщение по теме Основные классы неорганических веществ. 8 класс Генетическая связь между классами органических веществ
Генетическая связь между классами органических веществ Химические уравнения Закон сохранения массы веществ
Химические уравнения Закон сохранения массы веществ Соли и их свойства
Соли и их свойства Соединения железа
Соединения железа The main purpose of flour
The main purpose of flour Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Растворы. Типы растворов
Растворы. Типы растворов Катализ и катализаторы
Катализ и катализаторы Полимерные материалы, пластмассы и изделия из них
Полимерные материалы, пластмассы и изделия из них Дендример, или арборол
Дендример, или арборол Механизм реакции
Механизм реакции Күрделі эфирлер
Күрделі эфирлер Основні поняття матеріального балансу. Розрахунок об’єму повітря та продуктів згоряння при горінні речовин та матеріалів
Основні поняття матеріального балансу. Розрахунок об’єму повітря та продуктів згоряння при горінні речовин та матеріалів Химическая кинетика
Химическая кинетика Влияние катализатора на скорость химической реакции. Катализ
Влияние катализатора на скорость химической реакции. Катализ Азотсодержащие органические соединения. Аминокислоты (часть 2)
Азотсодержащие органические соединения. Аминокислоты (часть 2) Характер затвердевания
Характер затвердевания Студенттің өзіндік жұмысы
Студенттің өзіндік жұмысы Карбоновые кислоты
Карбоновые кислоты Материаловедение. Химические волокна
Материаловедение. Химические волокна Оксиди: поняття, склад і назви, фізичні властивості, поширеність у природі, використання
Оксиди: поняття, склад і назви, фізичні властивості, поширеність у природі, використання Механизмы органических реакций
Механизмы органических реакций Гидролиз органических и неорганических веществ
Гидролиз органических и неорганических веществ История развития контролируемой радикальной полимеризации. Управление ростом полимерной цепи нитроксильными радикалами
История развития контролируемой радикальной полимеризации. Управление ростом полимерной цепи нитроксильными радикалами