Содержание
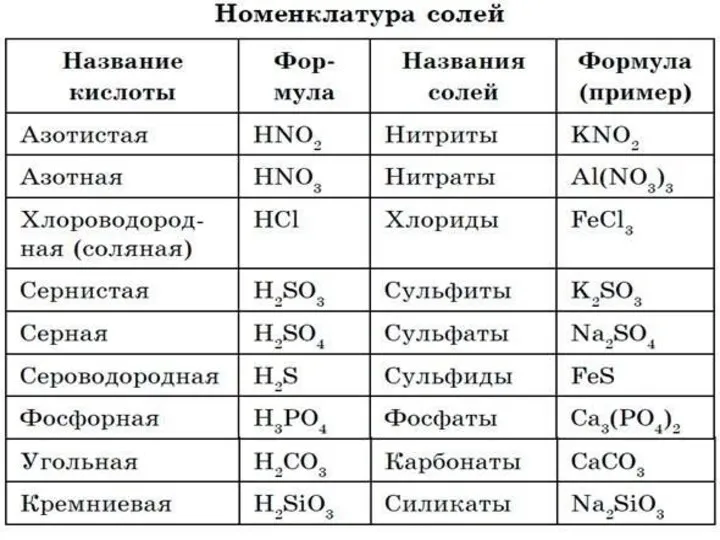
- 2. Соли - это сложные вещества, состоящие из ионов металлов и кислотного остатка.
- 4. Кислотный остаток образуется, если в формуле кислоты убрать атомы водорода. Заряд кислотного остатка определяется числом атомов
- 5. Алгоритм (1) называния соли по формуле. 1. Определить степени окисления металла и кислотного остатка (по таблице
- 6. Пример: Fe2(SO4)3 +3 -2 1. Fe2(SO4)3 2. Сульфат - соль H2SO4 (серной кислоты) 3. Сульфат железа
- 7. Упражнение. Назвать: FeSO4 Cr(NO3)3 Cr(NO3)2 Cu2SO3 CuCl2
- 8. Алгоритм (2) построения формул солей по названию. 1. Слева записать металл, указанный в названии, над ним
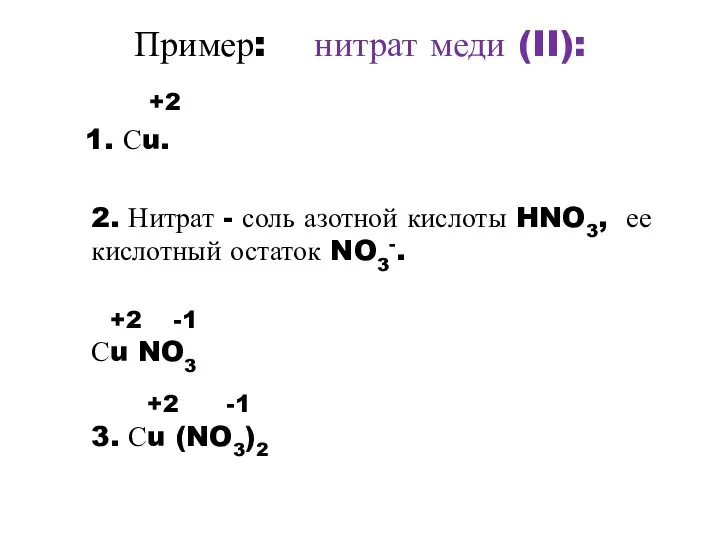
- 9. Пример: нитрат меди (II): +2 1. Сu. 2. Нитрат - соль азотной кислоты HNO3, ее кислотный
- 10. Упражнение. Составьте формулы: сульфит магния бромид хрома (III) ортофосфат бария сульфат алюминия.
- 11. Классификация солей Соли Растворимые КNO3, Na3PO4 Нерастворимые BaCO3, ВаSO4
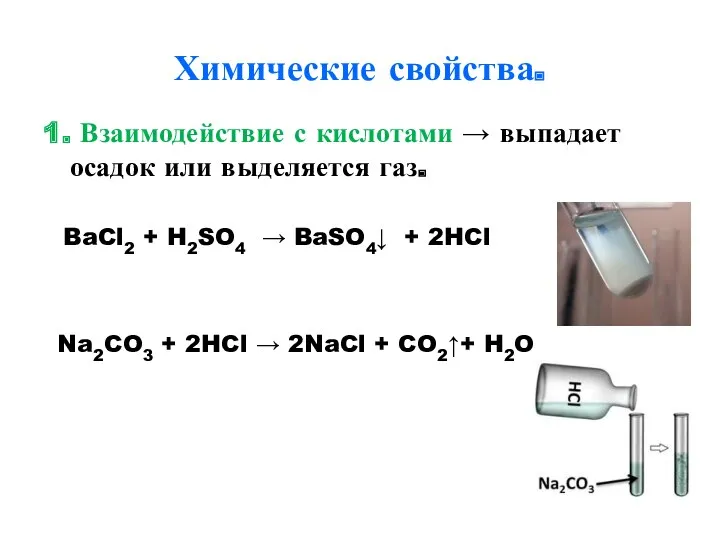
- 12. Химические свойства. 1. Взаимодействие с кислотами → выпадает осадок или выделяется газ. BaCl2 + H2SO4 →
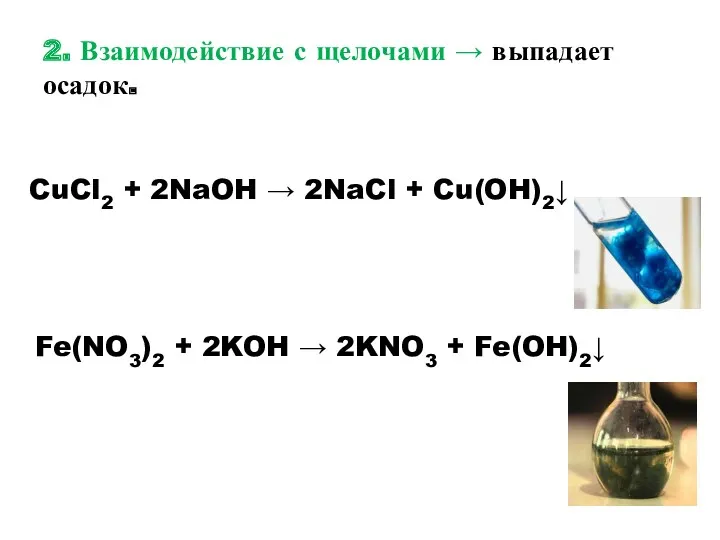
- 13. 2. Взаимодействие с щелочами → выпадает осадок. CuCl2 + 2NaOH → 2NaCl + Cu(OH)2↓ Fe(NO3)2 +
- 15. Скачать презентацию








 Альдегиды и кетоны. Лекция 10
Альдегиды и кетоны. Лекция 10 Выращивание кристаллов медного купороса в домашних условиях
Выращивание кристаллов медного купороса в домашних условиях Химические свойства алканов
Химические свойства алканов Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Электронное строение атома
Электронное строение атома Белки. Строение
Белки. Строение Минеральные вяжущие вещества, материалы и изделия на их основе
Минеральные вяжущие вещества, материалы и изделия на их основе химиияяяяяяяяяяяяяяяяяяяяяяяяяяяяяяяяя
химиияяяяяяяяяяяяяяяяяяяяяяяяяяяяяяяяя Индикаторы кислотно-основного титрования
Индикаторы кислотно-основного титрования Катионы І - ІІІ аналитических групп
Катионы І - ІІІ аналитических групп Резина и её свойства . Полимеры и их использование
Резина и её свойства . Полимеры и их использование Аммиак. № 12 зертханалық тәжірибе Аммиак молекуласының моделі
Аммиак. № 12 зертханалық тәжірибе Аммиак молекуласының моделі Минералы и горные породы
Минералы и горные породы Общая характеристика неметаллов
Общая характеристика неметаллов Методика обучения и воспитания на уроках химии
Методика обучения и воспитания на уроках химии Многоатомные и одноатомные спирты
Многоатомные и одноатомные спирты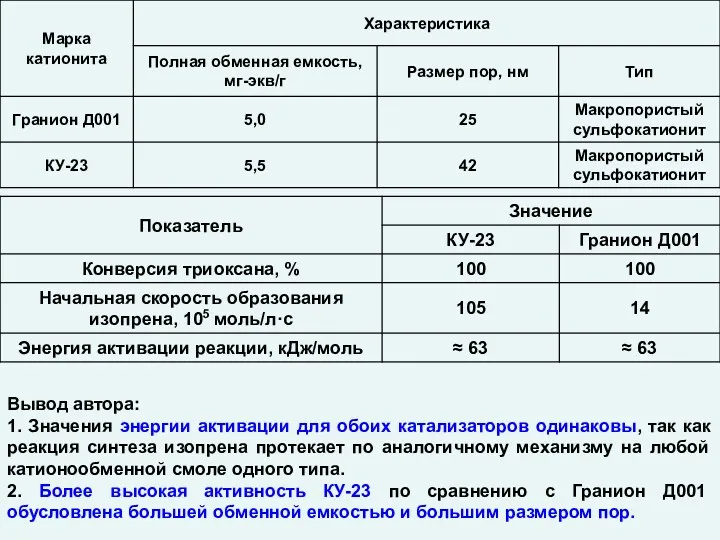 Катализ. Гетерогенные катализаторы
Катализ. Гетерогенные катализаторы Коррозия металлов. Способы защиты металлов от коррозии
Коррозия металлов. Способы защиты металлов от коррозии Основы термодинамики
Основы термодинамики Химическая связь. 8 класс
Химическая связь. 8 класс Электронный помощник по химии (8 класс)
Электронный помощник по химии (8 класс) Важнейшие классы бинарных соединений – оксиды и летучие соединения
Важнейшие классы бинарных соединений – оксиды и летучие соединения Химические формулы. Относительная молекулярная масса вещества
Химические формулы. Относительная молекулярная масса вещества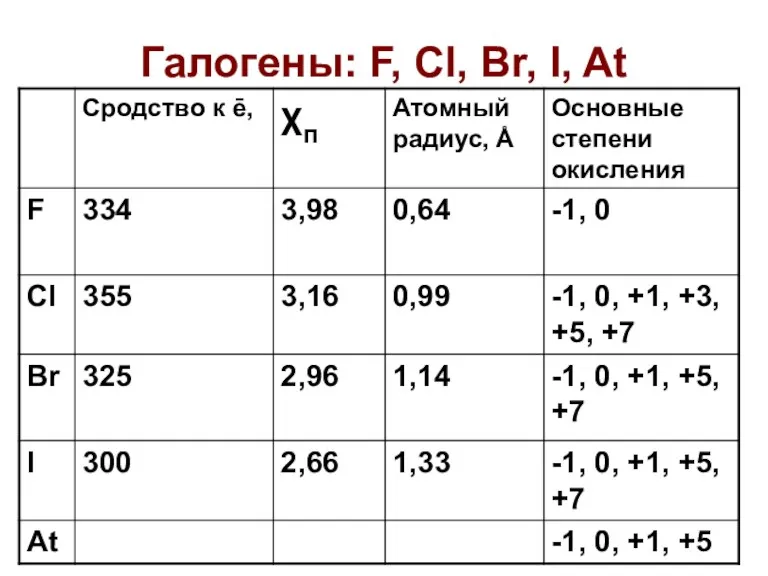 Галогены: F, Cl, Br, I, At
Галогены: F, Cl, Br, I, At Оксиды. Физические свойства
Оксиды. Физические свойства Окисно-відновні реакції у природі і промисловості
Окисно-відновні реакції у природі і промисловості Химические свойства алканов
Химические свойства алканов Гипергенез и почвообразование
Гипергенез и почвообразование