Содержание
- 2. 10.1 Катализ и катализаторы. 10.2 Кинетика ферментативных реакций. План
- 3. 10.1 Катализ – это явление изменения скорости реакции под влиянием веществ, называемых катализаторами.
- 4. Катализаторы – это вещества, изменяющие скорость химической реакции, но не изменяющиеся в ходе процесса ни качественно,
- 5. Небольшие количества катализаторов способны существенно изменить скорость взаимодействия большого количества реагирующих веществ.
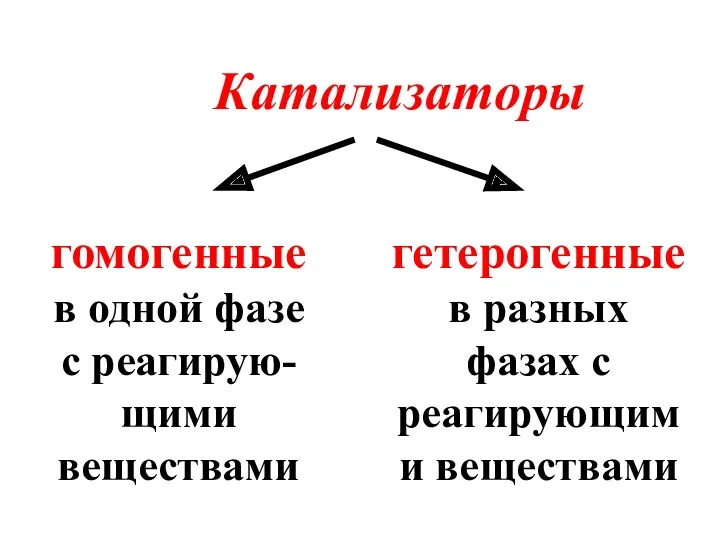
- 6. Катализаторы гомогенные в одной фазе с реагирую-щими веществами гетерогенные в разных фазах с реагирующими веществами
- 7. Пример гетерогенного катализа
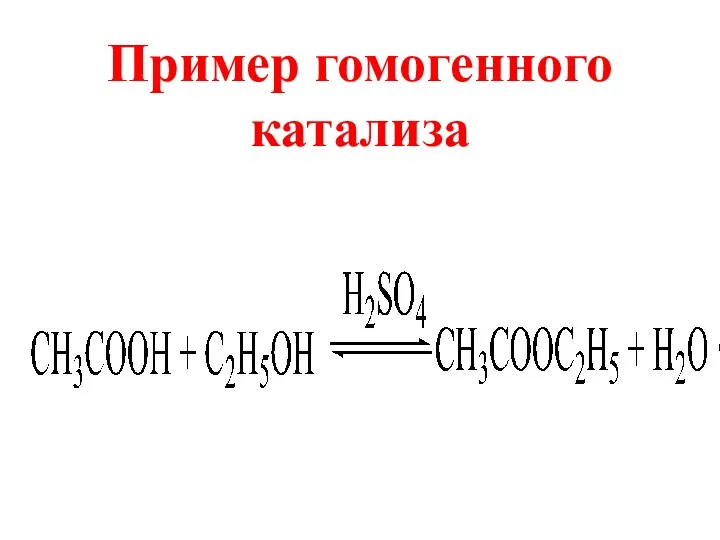
- 8. Пример гомогенного катализа
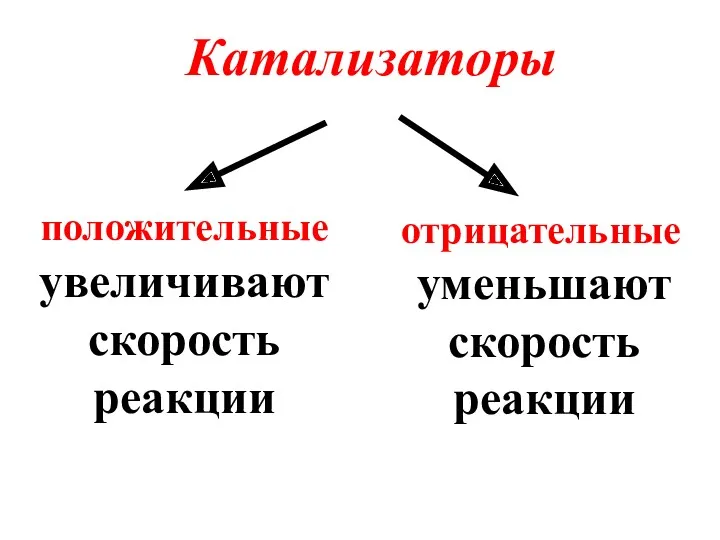
- 9. Катализаторы положительные увеличивают скорость реакции отрицательные уменьшают скорость реакции
- 10. Вещества, усиливающие действие катализаторов, называются промоторами, а ослабляющие - каталитическими ядами.
- 11. Ингибаторы – вещества, уменьшающие скорость реакции, но расходующиеся при этом сами.
- 12. С точки зрения теории активного комплекса механизм действия катализаторов в том, что они изменяют высоту энергетического
- 13. Без катализатора: А + В ↔ А...В → АВ В присутствии катали-затора: А + В +
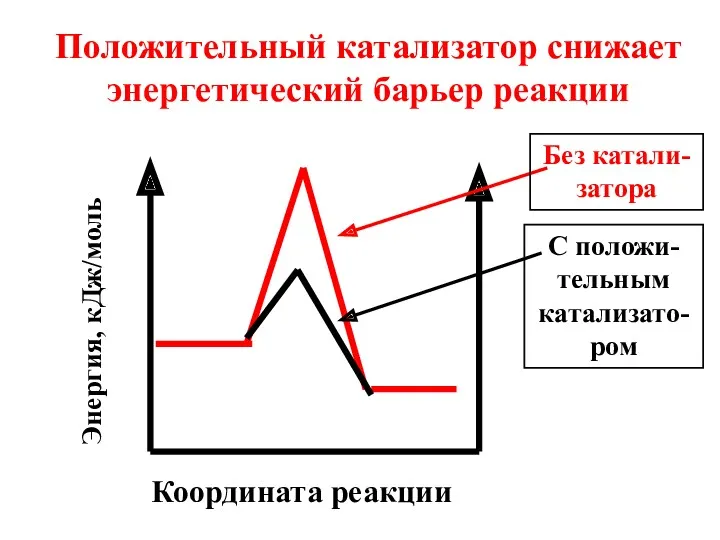
- 14. Координата реакции Положительный катализатор снижает энергетический барьер реакции Энергия, кДж/моль Без катали-затора С положи-тельным катализато-ром
- 15. Под воздействием положительного катализатора в реакционной смеси возрастает доля активных молекул при данной температуре. Скорость реакции
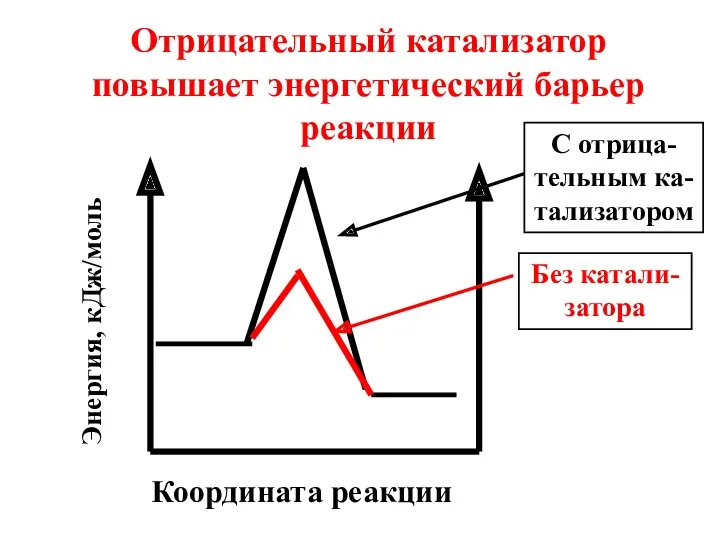
- 16. Координата реакции Отрицательный катализатор повышает энергетический барьер реакции Энергия, кДж/моль Без катали-затора С отрица-тельным ка-тализатором
- 17. Под воздействием отрицательного катализатора в реакционной смеси снижается доля активных молекул при данной температуре. Скорость реакции
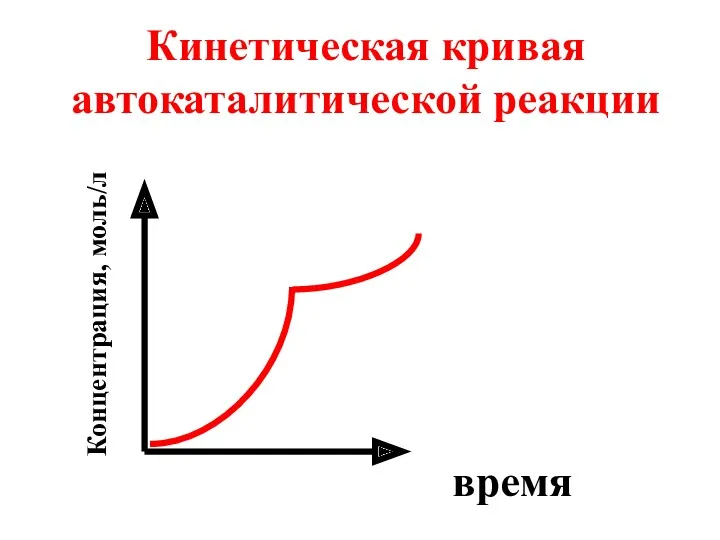
- 19. Частным случаем катализа является автокатализ: катализатором служит один из продуктов реакции.
- 20. Пример автокаталитической реакции: 2 KMnO4 + 5 H2C2O4 + +3 H2SO4 → 2 MnSO4 + +10
- 21. Кинетическая кривая автокаталитической реакции время Концентрация, моль/л
- 22. Катализаторы широко применяются в химической промышленности. В США рынок катализаторов составляет ~2 млрд. $.
- 23. Однако некоторые каталитические процессы в природе оказываются разрушительными для окружающей среды.
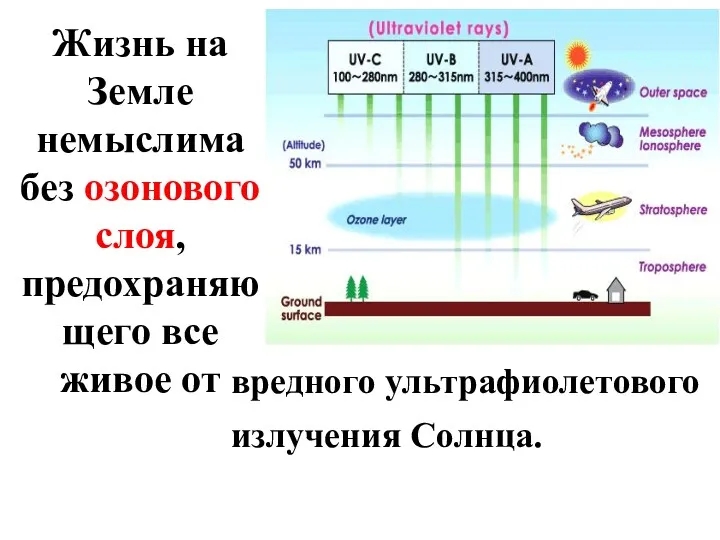
- 24. Разрушение озонового слоя Земли – пример гомогенного катализа, протекающего в атмосфере под воздействием фреонов.
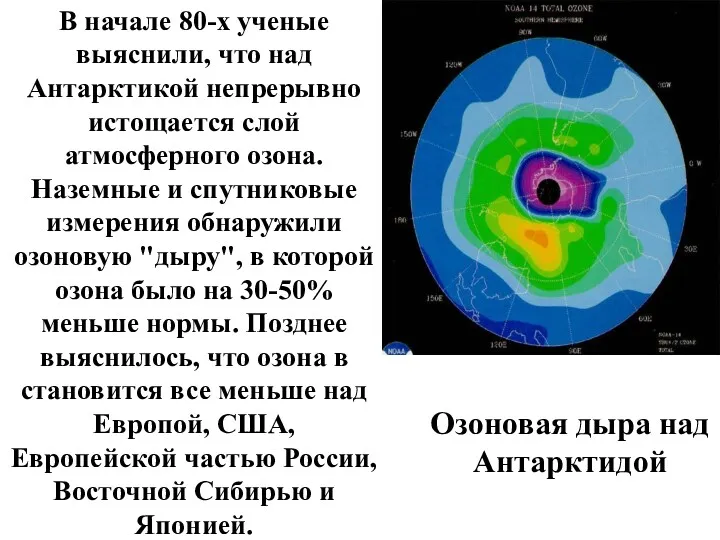
- 25. Жизнь на Земле немыслима без озонового слоя, предохраняющего все живое от вредного ультрафиолетового излучения Солнца.
- 26. Исчезновение озоносферы привело бы к непредсказуемым последствиям - вспышке рака кожи, уничтожению планктона в океане, мутациям
- 27. Озоновая дыра над Антарктидой В начале 80-х ученые выяснили, что над Антарктикой непрерывно истощается слой атмосферного
- 28. Фреоны – это фторо-хлороуглеводороды (СF2Cl2), применяемые как хладагенты. При обычных условиях они отличаются высокой устойчивостью к
- 29. В атмосфере происходит разложение фреонов под воздействием ультрафиолетового излучения солнца: CF2Cl2 → CF2Cl• + Cl• Cl•
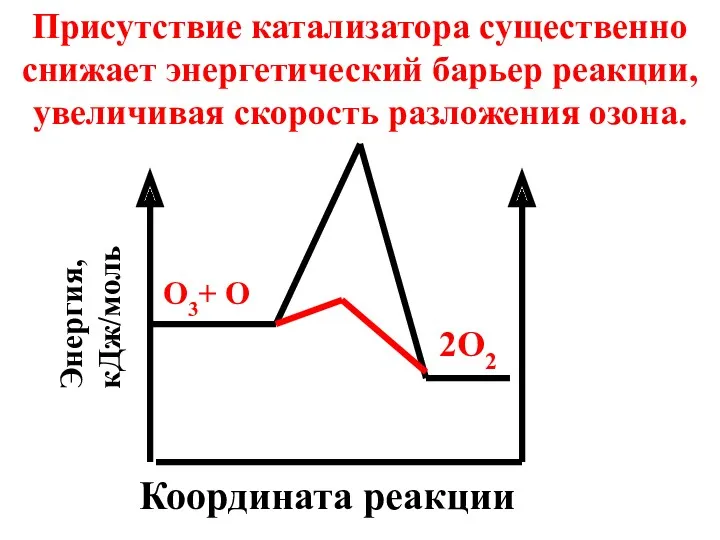
- 30. Без катализатора процесс протекает по схеме: O3 + O → 2 O2 Eак = 17,1 кДж/моль
- 31. В присутствии катализатора: O3 + Cl → ClO + O2 Eак= 2,1 кДж/моль ClO + O
- 32. Координата реакции Энергия, кДж/моль О3+ О 2О2 Присутствие катализатора существенно снижает энергетический барьер реакции, увеличивая скорость
- 33. 1987 году в Монреале состоялась Международная конференция, посвященная угрозе озоновому слою. Промышленно развитые страны договорились о
- 34. К 1992 году замена этих веществ на безопасные проходила так успешно, что было принято решение о
- 35. 10.2 Практически все биохимические реакции являются ферментативными.
- 36. Ферменты (биокатализаторы) – это вещества белковой природы, активированные катионами металлов.
- 37. Известно около 2000 различных ферментов, ~150 из них выделены, причем некоторые используются в качестве лекарственных препаратов.
- 38. Трипсин и химотрипсин – лечение бронхитов и пневмонии; пепсин – лечение гастрита; плазмин – лечение инфаркта;
- 39. Ферменты отличаются от обычных катализаторов: а) более высокой каталитической активностью; б) высокой специфичностью, т.е. избирательностью действия.
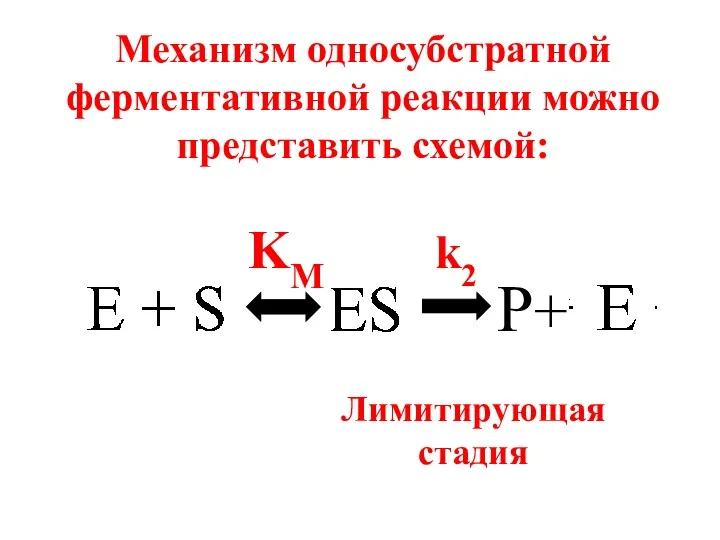
- 40. Механизм односубстратной ферментативной реакции можно представить схемой: P+ KM k2 Лимитирующая стадия
- 41. Е – фермент, S – субстрат, ЕS – фермент- субстратный комплекс, Р – продукт
- 42. Характеристикой первой стадии ферментативной реакции является КМ – константа Михаэлиса. КМ является величиной, обратной константе равновесия.
- 43. KM KM = 10‾5–10‾3 моль/л
- 44. КМ характеризует устойчивость фермент-субстратного комплекса (ES). Чем меньше КМ, тем устойчивее комплекс .
- 45. Кинетическое уравнение: υ = k2 [ES], (1) где k2 – константа скорости, называемая числом оборотов или
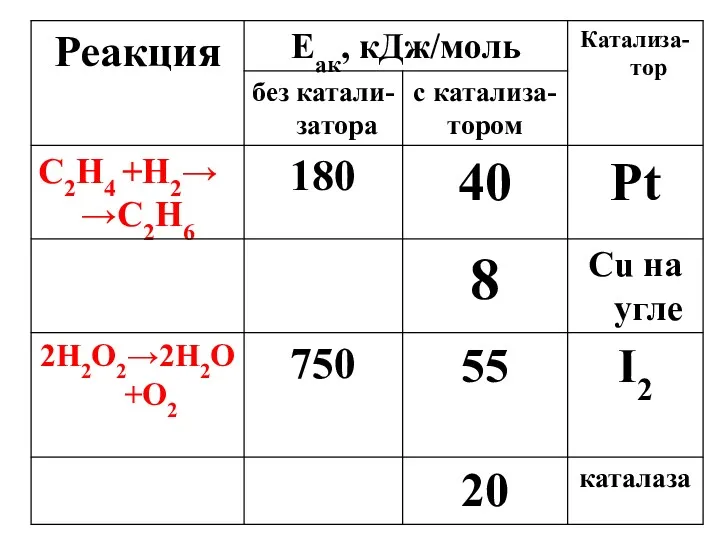
- 46. k2 равна числу молекул субстрата, претерпевающих превращения под воздействием одной молекулы фермента за 1 минуту при
- 47. Для уреазы, ускоряющей гидролиз мочевины: k2 = 1,85∙106 мин‾1 Для аденозинтрифосфатазы, ускоряющей гидролиз АТФ: k2 =
- 48. Существенным недостатком уравнения (1) является невозможность экспериментального определения [ES].
- 49. Выразив [ES] через другие величины, получаем кинетическое уравнение ферментативных реакций, называемое уравнением Михаэлиса-Ментен (1913)
- 50. υ = [E]общ [S] KM + [S] k2 Уравнение Михаэлиса-Ментен
- 51. Произведение k2[E]общ является величиной постоянной, которую обозначают υmax (максимальная скорость).
- 52. Соответственно: υ = υmax [S] KM + [S]
- 53. При низкой концентрации субстрата KM >> [S], поэтому υ = υmax KM [S] Кинетическое уравнение реакции
- 54. 2) При высокой концентрации субстрата Км Кинетическое уравнение реакции 0-го порядка υ = υmax
- 55. Кинетическая кривая ферментативной реакции [S] υ Реакция нулевого порядка Реакция первого порядка
- 56. 3) Если [S] = КМ, то υ = υmax 2 что позволяет графически определять Км ,
- 57. [S] υmax 2 υmax KM Графическое определение константы Михаэлиса(KM)
- 58. Ферменты, как правило, катализируют реакции с участием двух или нескольких субстратов. Для изображения двухсубстратных реакций используют
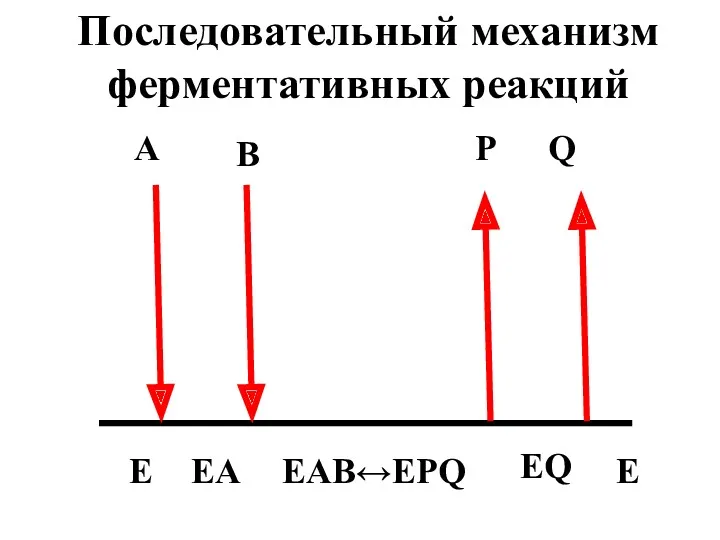
- 59. A B P Q E EA EQ E EAB↔EPQ Последовательный механизм ферментативных реакций
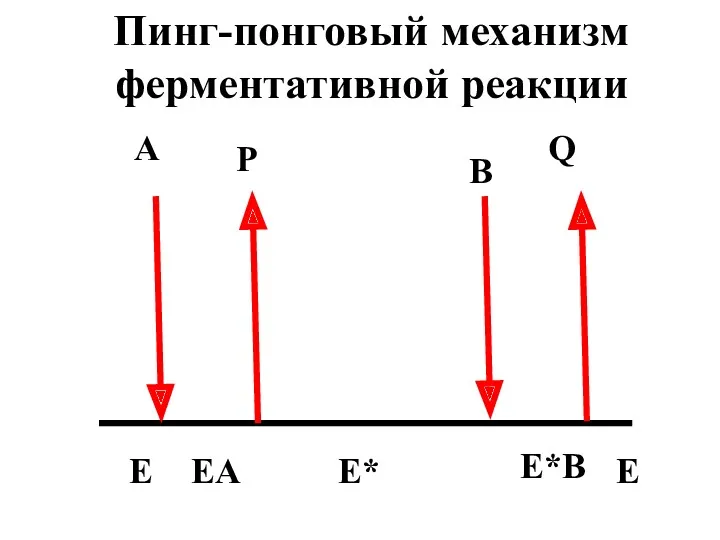
- 60. A B P Q E EA E*B E E* Пинг-понговый механизм ферментативной реакции
- 61. На активность ферментов оказывают влияние: а) температура, б) кислотность среды, в) наличие ингибиторов
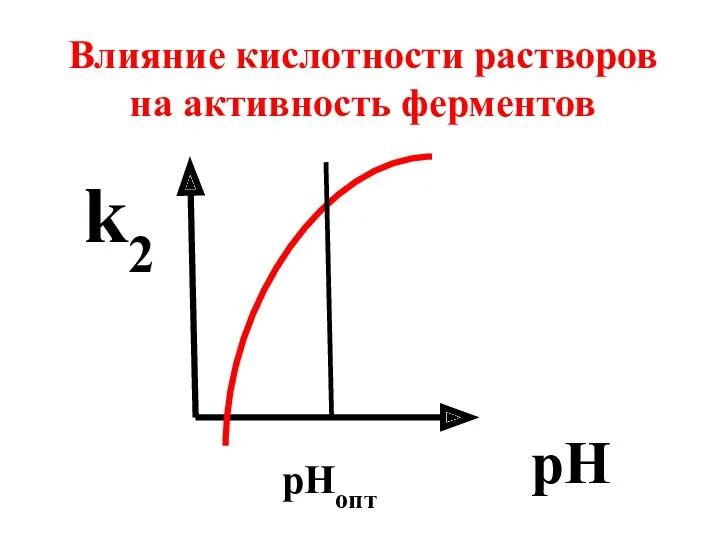
- 62. pH рНопт Влияние кислотности растворов на активность ферментов k2
- 63. Для большинства ферментов оптимальные значения рН совпадают с физиологическими значениями (7,3-7,4).
- 64. Однако существуют ферменты, для нормального функционирования которых нужна сильнокислая (пепсин – 1,5-2,5) или достаточно щелочная среда
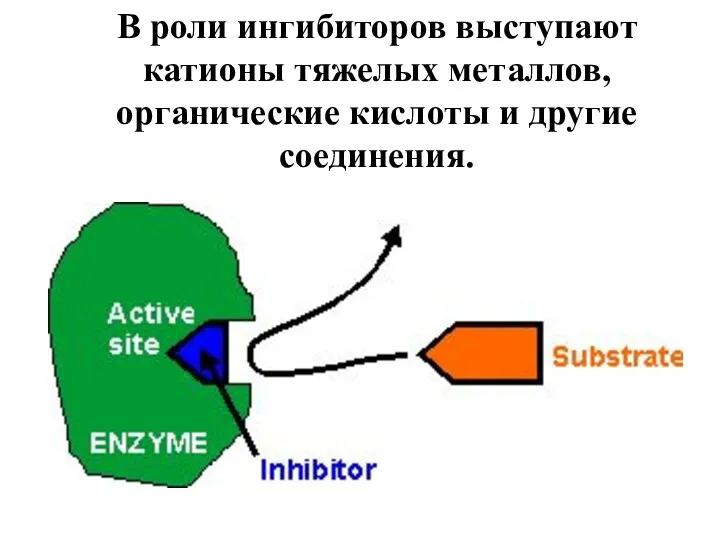
- 65. Ингибиторы ферментов – это вещества, занимающие часть активных центров молекул фермента, в результате чего скорость ферментативной
- 66. В роли ингибиторов выступают катионы тяжелых металлов, органические кислоты и другие соединения.
- 67. "Ключ к познанию ферментов лежит в изучении скоростей реакций". Дж.Холдейн
- 69. Скачать презентацию






























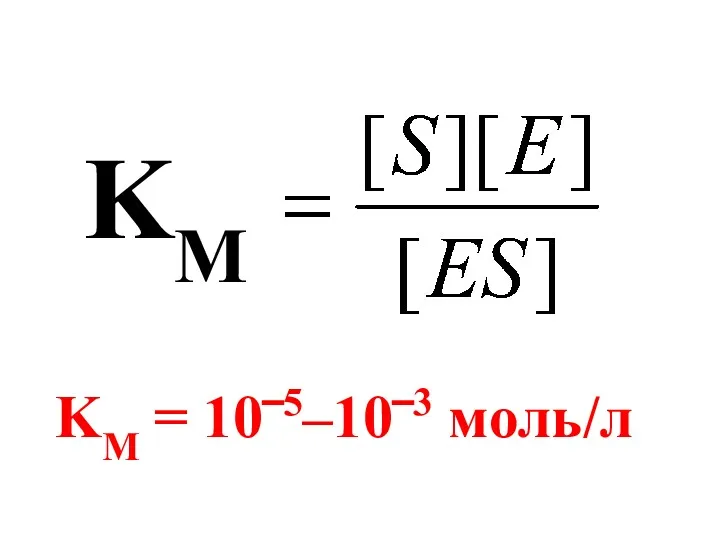

![Кинетическое уравнение: υ = k2 [ES], (1) где k2 –](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/193500/slide-44.jpg)


![Существенным недостатком уравнения (1) является невозможность экспериментального определения [ES].](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/193500/slide-47.jpg)
![Выразив [ES] через другие величины, получаем кинетическое уравнение ферментативных реакций, называемое уравнением Михаэлиса-Ментен (1913)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/193500/slide-48.jpg)
![υ = [E]общ [S] KM + [S] k2 Уравнение Михаэлиса-Ментен](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/193500/slide-49.jpg)
![Произведение k2[E]общ является величиной постоянной, которую обозначают υmax (максимальная скорость).](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/193500/slide-50.jpg)
![Соответственно: υ = υmax [S] KM + [S]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/193500/slide-51.jpg)
![При низкой концентрации субстрата KM >> [S], поэтому υ =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/193500/slide-52.jpg)

![Кинетическая кривая ферментативной реакции [S] υ Реакция нулевого порядка Реакция первого порядка](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/193500/slide-54.jpg)
![3) Если [S] = КМ, то υ = υmax 2 что позволяет графически определять Км ,](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/193500/slide-55.jpg)
![[S] υmax 2 υmax KM Графическое определение константы Михаэлиса(KM)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/193500/slide-56.jpg)






 Цветные металлы и сплавы
Цветные металлы и сплавы Массовая доля вещества в растворе
Массовая доля вещества в растворе Характеристики атома. Электроотрицательность. Шкала Полинга. Изменения химических свойств элементов в ПСЭ. (Лекция 1.2)
Характеристики атома. Электроотрицательность. Шкала Полинга. Изменения химических свойств элементов в ПСЭ. (Лекция 1.2) Анилин. Строение. Физические и химические свойства
Анилин. Строение. Физические и химические свойства Технология промышленных газов
Технология промышленных газов Химия вокруг нас
Химия вокруг нас Непредельные, ненасыщенные, ацетиленовые алкины
Непредельные, ненасыщенные, ацетиленовые алкины Перегонка с водяным паром
Перегонка с водяным паром Липиды. Классификация липидов
Липиды. Классификация липидов Основания. Номенклатура оснований
Основания. Номенклатура оснований Химические свойства металлов
Химические свойства металлов Процесс в химическом реакторе
Процесс в химическом реакторе Скорость химических реакций. Факторы, влияющие на скорость химической реакции
Скорость химических реакций. Факторы, влияющие на скорость химической реакции Щелочные металлы. Периодическая система химических элементов Д.И. Менделеева
Щелочные металлы. Периодическая система химических элементов Д.И. Менделеева Пена и пенообразователи. Назначение, виды, состав и свойства
Пена и пенообразователи. Назначение, виды, состав и свойства Гидроксиды. Основания: способы получения
Гидроксиды. Основания: способы получения Спирты
Спирты Кондуктометрия и кондуктометрическое титрование
Кондуктометрия и кондуктометрическое титрование Тяжелые металлы
Тяжелые металлы Горение жидкостей
Горение жидкостей Определение фосфатов, железа, хлоридов
Определение фосфатов, железа, хлоридов Изменения, происходящие с белками в процессах технологической переработки сырья
Изменения, происходящие с белками в процессах технологической переработки сырья Металлическая связь
Металлическая связь Химический состав воздуха
Химический состав воздуха Сладкая жизнь. Проектно-исследовательская работа
Сладкая жизнь. Проектно-исследовательская работа Хімічні явища в побуті
Хімічні явища в побуті Кристаллы. Кристаллические вещества
Кристаллы. Кристаллические вещества Алканы. (Предельные углеводороды. Парафины. Насыщенные углеводороды.)
Алканы. (Предельные углеводороды. Парафины. Насыщенные углеводороды.)