Содержание
- 3. 49% среди ХЭ
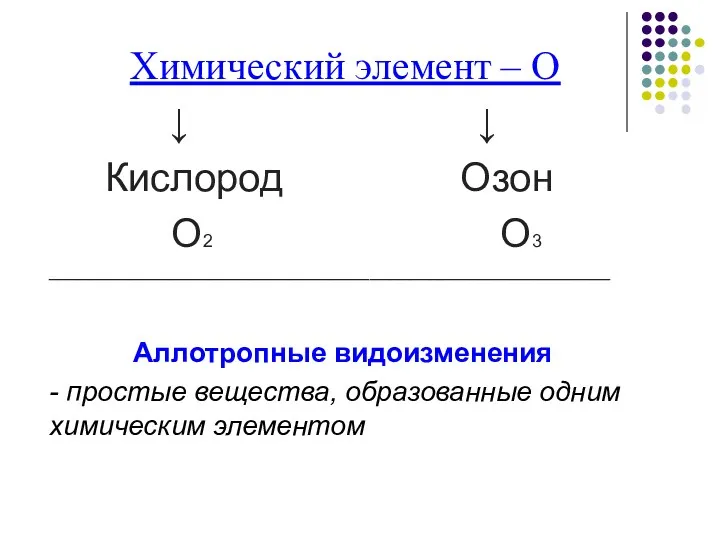
- 4. Химический элемент – О ↓ ↓ Кислород Озон О2 О3 ________________________________________________________ Аллотропные видоизменения - простые вещества,
- 5. Физические свойства кислорода Кислород – бесцветный газ, без вкуса и запаха, мало растворим в воде Кислород
- 6. Получение кислорода 2 HgO = 2Hg + O2 оксид ртуть кислород ртути
- 7. Получение кислорода 2)в промышленности: перегонка жидкого воздуха t(О2)= -1830С t(N2)= -1960С 1) в природе: СО2 +
- 8. Получение кислорода 3) в лаборатории:
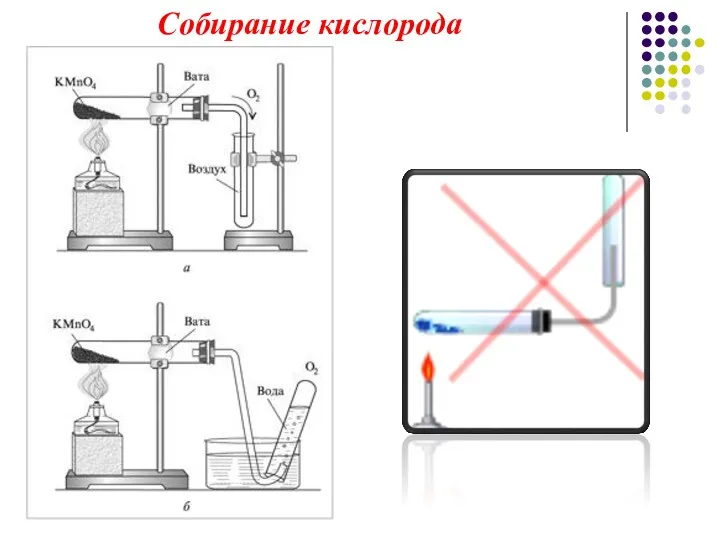
- 9. Собирание кислорода
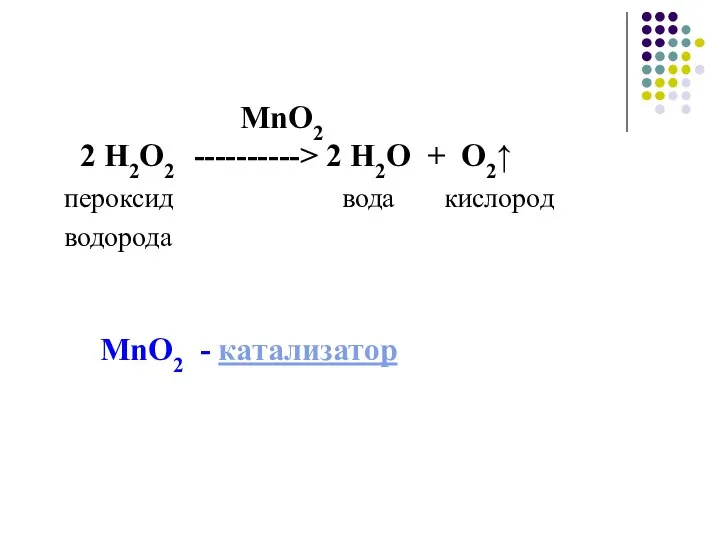
- 10. MnO2 2 Н2О2 ----------> 2 Н2О + О2↑ пероксид вода кислород водорода MnO2 - катализатор
- 11. Химические свойства – способность веществ превращаться в другие вещества
- 12. Химические свойства кислорода S + O2 = S O IV II 2 oксид серы (IV) Взаимодействие
- 13. Взаимодействие с углеродом С + O2 = С O IV II 2
- 14. P + O2 = P O v II Взаимодействие с фосфором 2 5 4 5 2
- 15. 3Fe + 2O2 = Fe3O4 железная окалина 2. Взаимодействие с металлами (кроме золота и платины) 2Mg
- 16. 3. Взаимодействие со сложными веществами СН4 + 2O2 = СO2 + 2Н2О
- 17. SO2 - оксид серы(IV) P2O5 - оксид фосфора(V) Fe O - оксид железа(II) Fe2O3 - оксид
- 18. ВЗАИМОДЕЙСТВИЕ ПРОСТЫХ И СЛОЖНЫХ ВЕЩЕСТВ С КИСЛОРОДОМ НАЗЫВАЕТСЯ ОКИСЛЕНИЕМ. ГОРЕНИЕ —ХИМИЧЕСКАЯ РЕАКЦИЯ,ПРИ КОТОРОЙ ПРОИСХОДИТ ОКИСЛЕНИЕ ВЕЩЕСТВ
- 19. ТЕСТ 1. Самый распространенный х.э.: а) водород в) кремний б) кислород г) алюминий 2. Химический элемент
- 20. 3. Впервые кислород получил: а) А.Лавуазье в)М.Ломоносов б) Д.Пристли г) Р.Бойль 4. Относительная атомная масса кислорода:
- 21. 5. Валентность кислорода в соединениях: а) II в) III б) I г) V 6. Формула простого
- 22. 7. Относительная молекулярная масса кислорода: а) 8 в) 32 б) 16 г) 23 8. Определяют кислород:
- 23. 9. В лаборатории кислород получают: а) р.соединения б) р.разложения в) р.замещения г) р.обмена 10. В промышленности
- 24. кроссворд Свойства кислорода
- 25. О К И С Л Е Н И Е П Р И С Т Л И
- 26. Вопросы к кроссворду: 1. Процесс взаимодействия простых и сложных веществ с кислородом. 2. Английский ученный открывший
- 28. Скачать презентацию






















 Effect of anodizing parameters on growth of selfordering TiO2
Effect of anodizing parameters on growth of selfordering TiO2 5-я группа элементов
5-я группа элементов Химия в повседневной жизни
Химия в повседневной жизни Химическая связь
Химическая связь Окислительно-востановительные реакции в растворах
Окислительно-востановительные реакции в растворах Приемы обращения с лабораторным оборудованием. Строение пламени
Приемы обращения с лабораторным оборудованием. Строение пламени Железо, его характеристики, свойства и соединения
Железо, его характеристики, свойства и соединения Физико-химические методы исследования биологически активных веществ
Физико-химические методы исследования биологически активных веществ Водневий показник ph
Водневий показник ph Plastic varieties and applications in construction
Plastic varieties and applications in construction Узагальнення й систематизація знань з теми Початкові хімічні поняття
Узагальнення й систематизація знань з теми Початкові хімічні поняття Геометрическая кристаллография
Геометрическая кристаллография Химические свойства алкенов. Получение
Химические свойства алкенов. Получение Технология получения многослойного и малослойного графена
Технология получения многослойного и малослойного графена Хімія в побуті
Хімія в побуті Арены. Бензол
Арены. Бензол Тепловий ефект хімічних реакцій. Екзотермічні і ендотермічні реакції. Термохімічні рівняння
Тепловий ефект хімічних реакцій. Екзотермічні і ендотермічні реакції. Термохімічні рівняння Катализ и катализаторы
Катализ и катализаторы Диагностические свойства минералов. Занятие 3-4
Диагностические свойства минералов. Занятие 3-4 Водно-солевой режим оборотной системы. Эффективность использования воды. Коэффициент концентрирования солей
Водно-солевой режим оборотной системы. Эффективность использования воды. Коэффициент концентрирования солей Химический элемент алюминий
Химический элемент алюминий Химическая связь
Химическая связь Химия в решении сырьевой проблемы
Химия в решении сырьевой проблемы Основные понятия и законы химии
Основные понятия и законы химии Закон постоянства состава вещества
Закон постоянства состава вещества Три состояния вещества
Три состояния вещества Tungsten. (Вольфрам)
Tungsten. (Вольфрам) Бериллий, магний и щелочноземельные металлы
Бериллий, магний и щелочноземельные металлы