Содержание
- 2. Что такое ОВР? Окисли́тельно-восстанови́тельные реа́кции (ОВР) — это встречно-параллельные химические реакции, протекающие с изменением степеней окисления
- 3. Виды окислительно-восстановительных реакций Межмолекулярные — реакции, в которых окисляющиеся и восстанавливающиеся атомы находятся в молекулах разных
- 4. Окисление Окисление - это процесс отдачи электронов атомом, молекулой или ионом. Если атом отдает свои электроны,
- 5. Восстановление Восстановление — это процесс присоединения электронов атомом, молекулой или ионом. Если атом присоединяет электроны, то
- 6. Окислителем является атом, молекула или ион, принимающий электроны. Восстановителем является атом, молекула или ион, отдающий электроны.
- 7. Определение стехиометрических коэффициентов в уравнениях ОВР При составлении уравнения окислительно-восстановительной реакции необходимо определить восстановитель, окислитель и
- 8. 1. Применим сначала метод электронно-ионного баланса (полуреакций). В этом методе рассматривают переход электронов от одних атомов
- 9. Рассмотрим для нашего случая полуреакцию окисления. Молекула FeS2превращается в ион Fe3+ (Fе(NО3)3 полностью диссоциирует на ионы,
- 10. Рассмотрим теперь полуреакцию восстановления нитрат-иона: Необходимо отнять у NО3 2 атома О. Для этого к левой
- 11. Добавив в обе части уравнения соответствующее количество ионов NO3- и Н+ находим молекулярное уравнение реакции: Обратите
- 12. 2. Уравняем данную реакцию методом электронного баланса. Процесс восстановления описывается: Сложнее составить схему окисления, поскольку окисляются
- 13. Пять молекул НNО3 идут на окисление FeS2, и еще три молекулы HNO3необходимы для образования Fe(NО3)3: Чтобы
- 14. Рассмотрим, например, процесс окисления этилена, происходящий при пропускании его через водный раствор перманганата калия. В результате
- 15. Стандартные потенциалы окислительно-восстановительных реакций Возможность протекания любой окислительно-восстановительной реакции в реальных условиях обусловлена рядом причин: температурой,
- 16. Химические процессы, сопровождающиеся возникновением электрического тока или вызываемые им, называются электрохимическими Чтобы понять природу электрохимических процессов,
- 17. При погружении металла не в воду, а в раствор соли этого металла равновесие в соответствии с
- 18. Ряд стандартных электродных потенциалов Если пластинку металла, погруженную в раствор его соли с концентрацией ионов металла,
- 19. Ряд напряжений характеризует химические свойства металлов: 1. Чем более отрицателен электродный потенциал металла, тем больше его
- 20. Электролиз растворов Совокупность окислительно-восстановительных реакций, которые протекают на электродах в растворах или расплавах электролитов при пропускании
- 21. При выборе наиболее вероятного процесса на аноде и катоде следует исходить из положения, что будет протекать
- 22. 3. При электролизе растворов солей, содержащих ионы, расположенные в ряду напряжений между Al+ и Н+, на
- 23. Электролиз расплавов Для получения высокоактивных металлов (натрия, алюминия, магния, кальция и др.), легко вступающих во взаимодействие
- 25. Скачать презентацию






















 Техники ювелирного дела. Введение в предмет. Общие сведения
Техники ювелирного дела. Введение в предмет. Общие сведения Современные проблемы молекулярной биологии
Современные проблемы молекулярной биологии Цикл трикарбоновых кислот (Ц.Кребса). Подсчёт суммарного энергетического эффекта аэробного окисления глюкозы
Цикл трикарбоновых кислот (Ц.Кребса). Подсчёт суммарного энергетического эффекта аэробного окисления глюкозы Речовини. Молекули. Атоми
Речовини. Молекули. Атоми Процесс в химическом реакторе
Процесс в химическом реакторе 20231104_prezentatsiya_teoriya_elektroliticheskoy_dissotsiatsii
20231104_prezentatsiya_teoriya_elektroliticheskoy_dissotsiatsii Каталитический риформинг
Каталитический риформинг Купрум. Знаходження в періодичній системі
Купрум. Знаходження в періодичній системі Непредельные углеводороды. Алкены
Непредельные углеводороды. Алкены Массовая доля вещества в растворе
Массовая доля вещества в растворе Анионы. Группы анионов
Анионы. Группы анионов Углерод и его свойства. 9 класс
Углерод и его свойства. 9 класс Физико-химия полимеров и их растворов
Физико-химия полимеров и их растворов Химический состав клетки
Химический состав клетки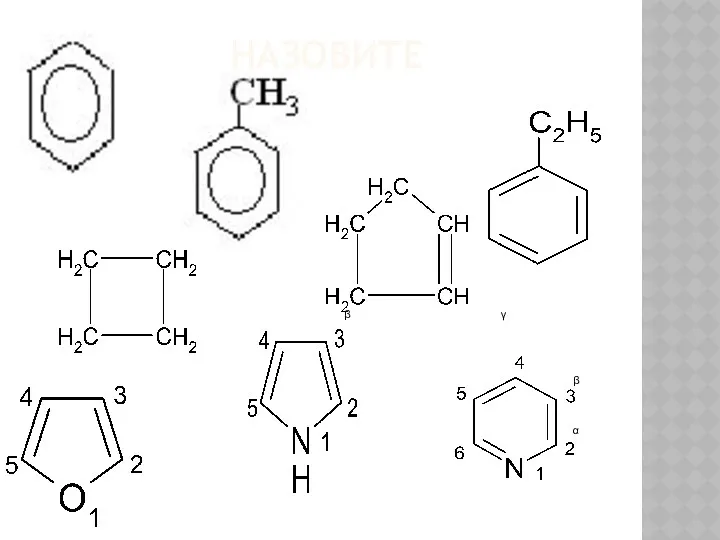 Общие сведения о гетероциклах
Общие сведения о гетероциклах Побочная подгруппа. 8 группы
Побочная подгруппа. 8 группы Проект узла регенерации растворителя уксусной кислоты производства терефталевой кислоты
Проект узла регенерации растворителя уксусной кислоты производства терефталевой кислоты Лекция 5. Нуклеофильное замещение при насыщенном атоме углерода
Лекция 5. Нуклеофильное замещение при насыщенном атоме углерода Пниктогены - элеметны VA группы
Пниктогены - элеметны VA группы Неметаллы: общая характеристика. 9 класс
Неметаллы: общая характеристика. 9 класс Полиэтилен
Полиэтилен Химическая посуда и лабораторное оборудование
Химическая посуда и лабораторное оборудование Кислоты. Состав кислот
Кислоты. Состав кислот Спектрофометрия
Спектрофометрия Углерод и его свойства
Углерод и его свойства d997-13229e5e
d997-13229e5e Теория электролитической диссоциации
Теория электролитической диссоциации Реакции ионного обмена
Реакции ионного обмена