Содержание
- 2. Какие из этих соединений могут встречаться в природной воде? Mg, CaO, Ca(OH)2 , MgCO3 , CaCl2,
- 3. Какие из этих соединений могут встречаться в природной воде? CaCl2, Ca (HCO3)2, Mg(HCO3)2 , MgSO4 ,
- 4. Помочь чайнику! Составить уравнения реакций процессов образования накипи, ее устранения и предотвращения
- 5. Жесткость воды и способы ее устранения
- 6. Алгоритм действий Определить цель – изучить природу жесткости воды и методы ее устранения 2. Выдвинуть гипотезу
- 7. План работы Уточнить значение термина «жесткость воды». Проанализировать информацию о причинах образования жесткой воды, ее влиянии
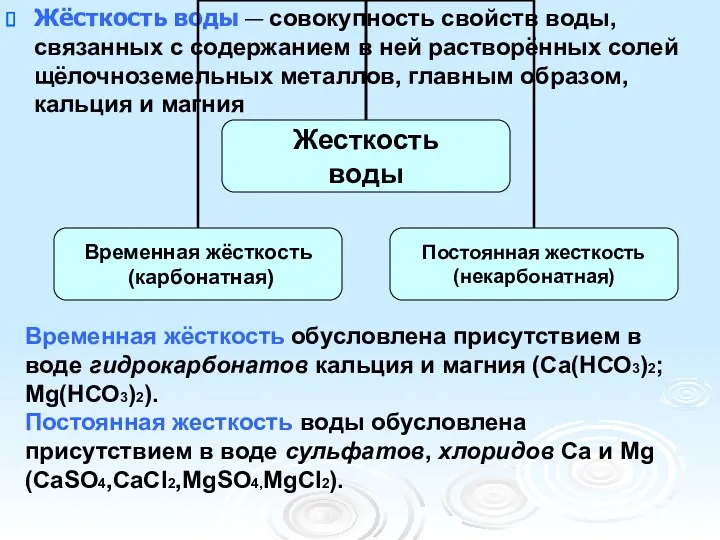
- 9. Жёсткость воды — совокупность свойств воды, связанных с содержанием в ней растворённых солей щёлочноземельных металлов, главным
- 10. Карбонатная жесткость (временная) обусловлена присутствием в воде гидрокарбонатов кальция и магния: Устраняется кипячением, действием известкового «молока»
- 11. Некарбонатная жесткость (постоянная) обусловлена присутствием в воде сульфатов и хлоридов кальция и магния. Устраняют некарбонатную жесткость
- 12. Влияние жесткости на качество воды Высокая жесткость ухудшает свойства воды, придавая ей горьковатый вкус и оказывая
- 13. При взаимодействии солей жесткости с моющими веществами происходит образование "мыльных шлаков" в виде пены. Это приводит
- 14. Образующийся карбонатный продукт реакции оседает на стенках сосуда, возникает накипь: Ca2+ + 2HCO3- =CaCO3 + H2O
- 15. Лейка душа забита накипью Накипь на смесителе Накипь в быту
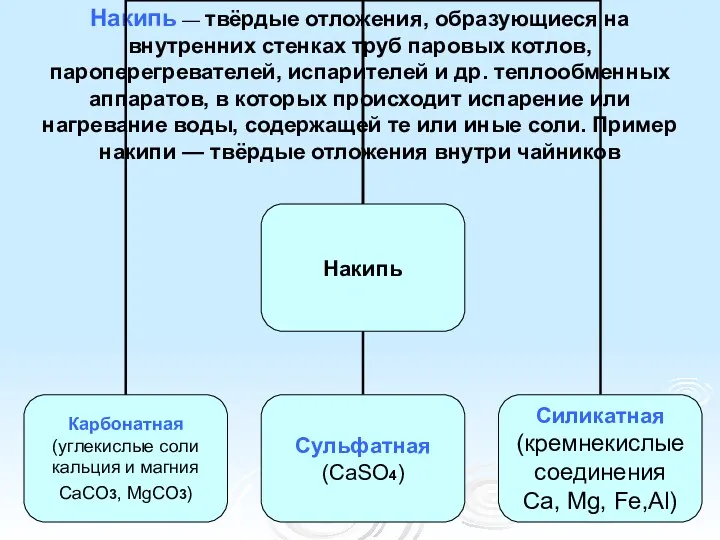
- 16. Накипь — твёрдые отложения, образующиеся на внутренних стенках труб паровых котлов, пароперегревателей, испарителей и др. теплообменных
- 17. Состояние воды в Липецке Городская водопроводная сеть на 100 % питается из подземных источников, качество воды
- 18. Помочь чайнику! Составить уравнения реакций процессов образования накипи, ее устранения и предотвращения
- 19. Тесты по теме «Жесткость воды» Чем обусловлена жесткость воды: А. количеством растворимых солей кальция Б. количеством
- 20. Тесты по теме «Жесткость воды» 2. Как называется временная жесткость воды: А. карбонатная Б. фосфатная В.
- 21. Тесты по теме «Жесткость воды» 3. Постоянную жесткость воды можно удалить: А. отстаиванием Б. кипячением В.
- 22. Тесты по теме «Жесткость воды» 4. Временную жесткость воды можно удалить: А. отстаиванием Б. кипячением В.
- 23. Тесты по теме «Жесткость воды» 5. Умеренная жесткость - __________ качество для питьевой воды, поскольку из
- 24. Рекламная пауза!
- 25. Виват, Калгон! Виват?
- 26. Фосфаты натрия Сода Поликарбоксилаты Кристаллическая целлюлоза Полиэтиленгликоль Фосфаты Поликарбоксилаты Силикаты Энзимы Отдушки и отбеливатель
- 27. Помочь чайнику ! Запишите уравнения реакций, лежащих в основе процессов образования накипи и ее устранения
- 28. Дело – труба! Тише воды, ниже травы Вывести на чистую воду Чувствую себя, как рыба в
- 30. Скачать презентацию

























 Фенолы. Классификация и номенклатура фенолов
Фенолы. Классификация и номенклатура фенолов 20231113_tipy_him._reaktsiy_prezentatsiya
20231113_tipy_him._reaktsiy_prezentatsiya Физико-химические свойства поливинилового спирта и поливинилформаля
Физико-химические свойства поливинилового спирта и поливинилформаля Введение в общеобразовательную научную дисциплину Химия
Введение в общеобразовательную научную дисциплину Химия Наглядное пособие Динамические модели. Химическое равновесие в растворах
Наглядное пособие Динамические модели. Химическое равновесие в растворах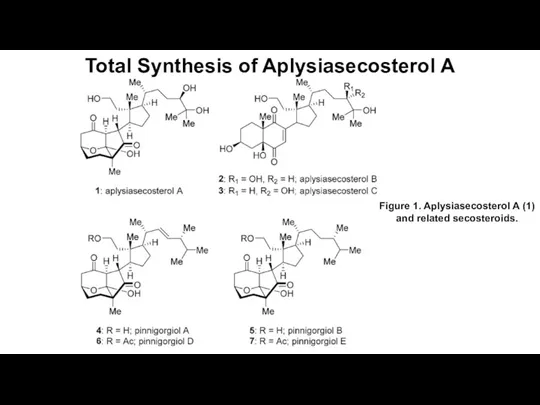 Total Synthesis of Aplysiasecosterol A
Total Synthesis of Aplysiasecosterol A Химико-лесной комплекс
Химико-лесной комплекс Металлы в организме человека
Металлы в организме человека Тепловой эффект химических реакций
Тепловой эффект химических реакций Полімери. Будова і властивості полімерів
Полімери. Будова і властивості полімерів Көпатомды спирттер. Химиялық қасиеттері
Көпатомды спирттер. Химиялық қасиеттері Занимательные опыты в качественном анализе
Занимательные опыты в качественном анализе Атомы и молекулы. Простые и сложные вещества. 6 класс
Атомы и молекулы. Простые и сложные вещества. 6 класс Пниктогены - элеметны VA группы
Пниктогены - элеметны VA группы Соли. Классификация. Физические и химические свойства солей
Соли. Классификация. Физические и химические свойства солей Теория электролитической диссоциации
Теория электролитической диссоциации Производство чугуна и стали
Производство чугуна и стали Основания. 8 класс
Основания. 8 класс Каталитические процессы нефтепереработки
Каталитические процессы нефтепереработки Строение атома. Лекция №2
Строение атома. Лекция №2 Карбоновые кислоты. Тест
Карбоновые кислоты. Тест Сплавы, растворы и смеси. Задачи на концентрвцию
Сплавы, растворы и смеси. Задачи на концентрвцию АТФ молекуласының құрылысы мен қызметтері
АТФ молекуласының құрылысы мен қызметтері Периодический закон и периодическая система химических элементов Д.И. Менделеева (8 класс)
Периодический закон и периодическая система химических элементов Д.И. Менделеева (8 класс) Спирты. Действие этанола на организм человека (10 класс)
Спирты. Действие этанола на организм человека (10 класс) Генетическая связь между классами неорганических соединений
Генетическая связь между классами неорганических соединений Електроліти в сучасних акумуляторах
Електроліти в сучасних акумуляторах Химия воды
Химия воды