Содержание
- 2. Цели урока: изучить классификацию химических реакций по тепловому эффекту; Научиться решать задачи на тепловой эффект. повторить
- 3. Тепловой эффект химических реакций
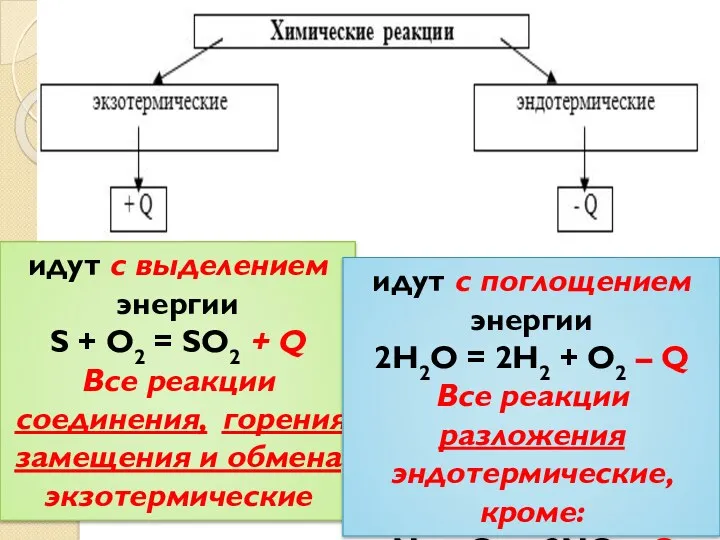
- 4. Идут с выделение теплоты S + O2 = SO2 + Q идут с выделением энергии S
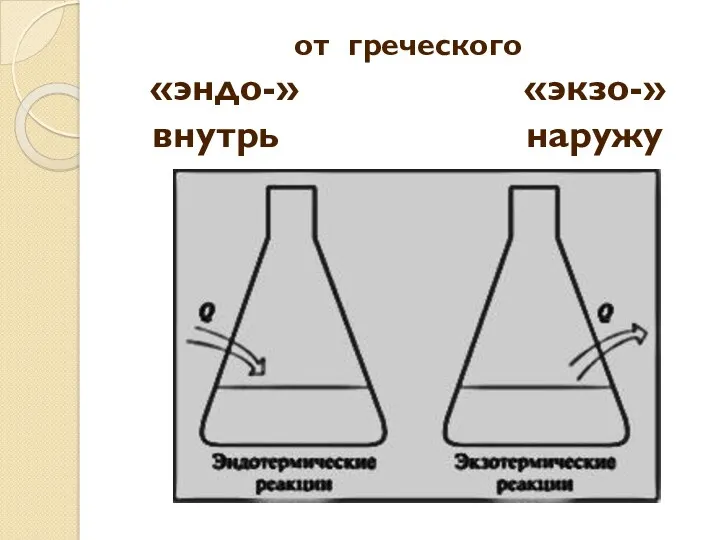
- 5. от греческого «эндо-» «экзо-» внутрь наружу
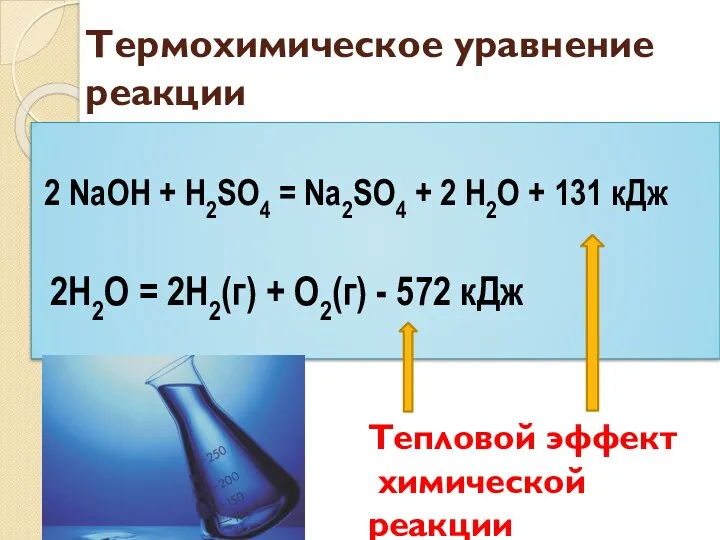
- 6. Tермохимическое уравнение реакции 2 NaOH + H2SO4 = Na2SO4 + 2 H2O + 131 кДж 2H2О
- 7. Применение знаний о тепловом эффекте химических реакций Самая мощная в мире российская ракета "Энергия" Двигатели одной
- 8. Горение газа метана в бытовых плитах: СH4+ 2O2 = СO2+ 2 H2О + 890 кДж Горение
- 9. Световых частиц поток Падает на зеленый листок, Листок кислород выделяет, энергию запасает.
- 10. Д/з: 1) Попробуйте объяснить изображения. 1 2 3 4
- 11. Решение задач При взаимодействии 7г железа с серой выделилось 12,15 кДж энергии. Составьте термохимическое уравнение реакции.
- 13. Решение задач Вычислить массу углерода, которая потребуется для получения 1608,96кДж энергии, если термохимическое уравнение: C +
- 15. Скачать презентацию









 Бытовая химия. Правила безопасного обращения со средствами бытовой химии
Бытовая химия. Правила безопасного обращения со средствами бытовой химии Висбрекинг (перспективный процесс ТК)
Висбрекинг (перспективный процесс ТК) Камни и Лев
Камни и Лев Алканы (предельные углеводороды)
Алканы (предельные углеводороды) Кристаллическое состояние вещества в природе
Кристаллическое состояние вещества в природе Серная кислота. Свойства разбавленной серной кислоты, соли серной кислоты
Серная кислота. Свойства разбавленной серной кислоты, соли серной кислоты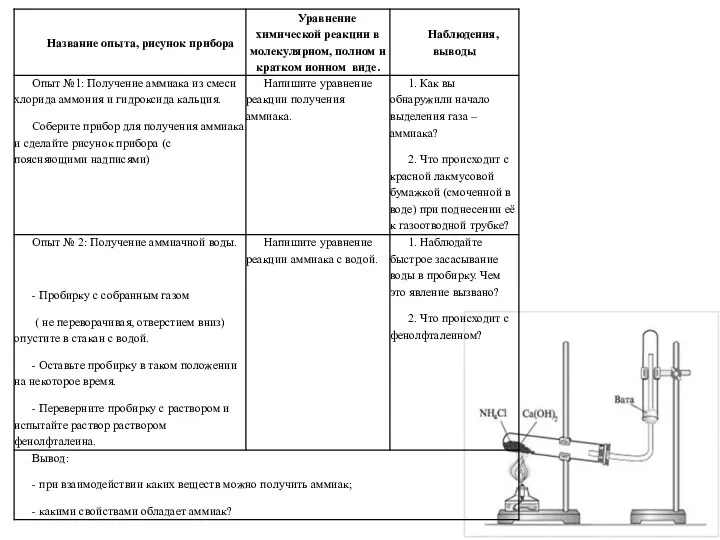 Получение аммиака и изучение его свойств
Получение аммиака и изучение его свойств Электролит және бейэлектролит ерітінділердің коллигативті қасие
Электролит және бейэлектролит ерітінділердің коллигативті қасие Химический турнир
Химический турнир Окислительно-восстановительные реакции. Основные положения электронной теории ОВР
Окислительно-восстановительные реакции. Основные положения электронной теории ОВР Фосфор и его соединения
Фосфор и его соединения Неорганические полимеры
Неорганические полимеры Спирты. Определение. Классификация
Спирты. Определение. Классификация Синтетический каучук и его применение
Синтетический каучук и его применение Вещества. Чистые вещества. Смеси
Вещества. Чистые вещества. Смеси Теория сильных и слабых электролитов
Теория сильных и слабых электролитов Вычисление массовой доли растворенного вещества. 8 класс
Вычисление массовой доли растворенного вещества. 8 класс Электрофизические свойства GaAs, зонная структура, полупроводящий и полуизолирующий GaAs, способы создания p-n перехода
Электрофизические свойства GaAs, зонная структура, полупроводящий и полуизолирующий GaAs, способы создания p-n перехода Электролиз
Электролиз Изучение свойств тиосульфата натрия
Изучение свойств тиосульфата натрия Кислород и озон
Кислород и озон Цветные маталлы и сплавы
Цветные маталлы и сплавы Химическая промышленность Донецкой области
Химическая промышленность Донецкой области Распространенность химических элементов на земле и в космосе
Распространенность химических элементов на земле и в космосе Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР) Тепловий ефект хімічних реакцій. Екзотермічні і ендотермічні реакції. Термохімічні рівняння
Тепловий ефект хімічних реакцій. Екзотермічні і ендотермічні реакції. Термохімічні рівняння Актуальные вопросы содержания контрольных измерительных материалов ЕГЭ в 2019 г
Актуальные вопросы содержания контрольных измерительных материалов ЕГЭ в 2019 г Выращивание кристаллов в домашних условиях
Выращивание кристаллов в домашних условиях