Содержание
- 2. Девиз. «Периодическому закону будущее не грозит разрушением, а только надстройка и развитие обещаются» Д.И. Менделеев
- 3. План: Открытие периодического закона Периодический закон и строение атома Периодическая система и строение атома Значение закона
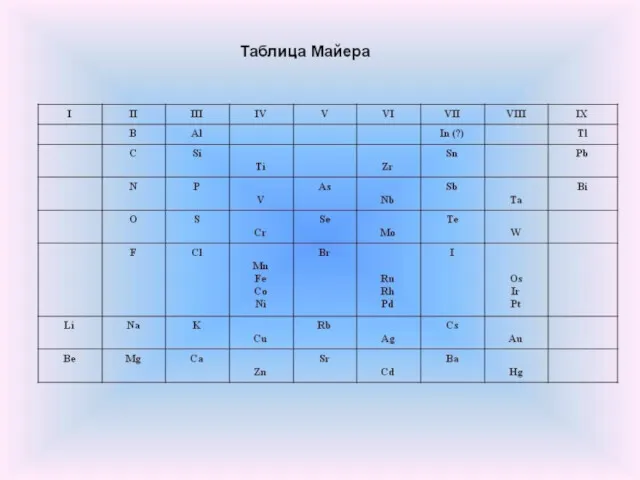
- 4. Открытие периодического закона Опубликовал таблицу из 27 элементов
- 5. Дмитрий Иванович Менделеев (1834 – 1907 г.г.)
- 6. Расположение карточек по возрастанию атомного веса химического элемента
- 7. Расположение карточек по возрастанию атомного веса химического элемента Н 1 Li 7 Be 9
- 8. 1 марта 1869 года Менделеев сформулировал Периодический закон “Свойства элементов, а также образуемых ими простых и
- 9. Д.И. Менделеев «Периодическому закону будущее не грозит разрушением, а только надстройка и развитие обещаются»
- 10. Современная формулировка периодического закона “Свойства элементов, а также образуемых ими простых и сложных веществ находятся в
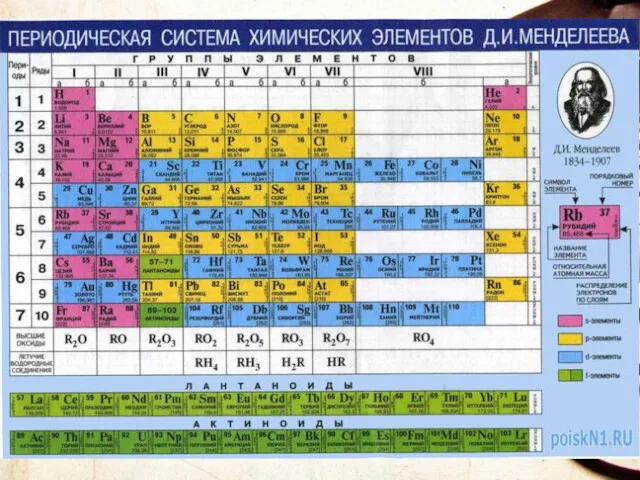
- 11. Периодическая система химических элементов (ПСХЭ) - это графическое изображение закона, каждое обозначение отражает какую либо особенность
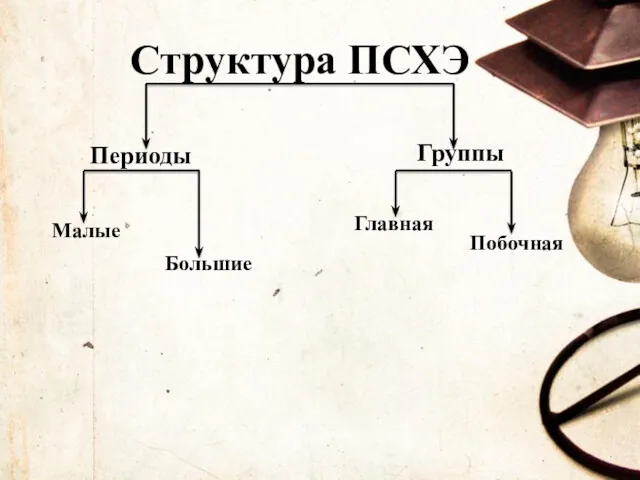
- 13. Структура ПСХЭ Периоды Группы Малые Большие Главная Побочная
- 14. Периоды - горизонтальные ряды элементов, в пределах которых свойства элементов изменяются последовательно. Группы- это вертикальные столбцы
- 15. В периодах СЛЕВА НАПРАВО металлические свойства ослабевают, а неметаллические усиливаются. а) увеличиваются заряды атомных ядер; б)
- 16. В группах главных подгруппах СВЕРХУ ВНИЗ металлические свойства элементов усиливаются, а неметаллические ослабевают. а) увеличиваются заряды
- 17. S – это символ элемента СЕРА – это название элемента 32,064 – это атомная масса 16
- 18. 1. В главных подгруппах периодической системы химических элементов Д.И.Менделеева с увеличением заряда ядра радиус атомов, как
- 19. 3. В периодах периодической системы химических элементов Д.И.Менделеева с увеличением заряда ядер атомов не изменяется: 1)
- 20. ПРОВЕРЬ СЕБЯ - 1) - 4) - 2) - 4)
- 22. Скачать презентацию
















 Степень окисления
Степень окисления Гидролиз солей
Гидролиз солей Основные понятия органической химии. Лекция № 1
Основные понятия органической химии. Лекция № 1 Обмен жиров
Обмен жиров Структура и функции биомакромолекул. Лекция 1
Структура и функции биомакромолекул. Лекция 1 Коррозия каменных и бетонных строительных конструкций
Коррозия каменных и бетонных строительных конструкций Основания. Классификация оснований
Основания. Классификация оснований Номенклатура оснований. Классификация и примеры. Получение оснований. Химические свойства
Номенклатура оснований. Классификация и примеры. Получение оснований. Химические свойства Топливо. Виды топлива. Химический состав топлива. Основные характеристики топлива. Марки топлива
Топливо. Виды топлива. Химический состав топлива. Основные характеристики топлива. Марки топлива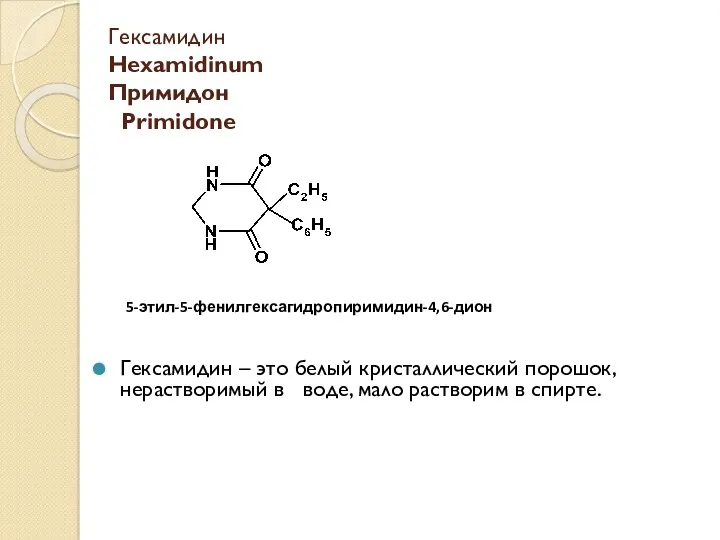 Гексамидин Hexamidinum. Примидон Primidone
Гексамидин Hexamidinum. Примидон Primidone Кислородные соединения азота
Кислородные соединения азота Реакции деструкции макромолекул
Реакции деструкции макромолекул Тепловой эффект химической реакции. 11 класс
Тепловой эффект химической реакции. 11 класс Отрицательное влияние азотных минеральных удобрений на почву
Отрицательное влияние азотных минеральных удобрений на почву Хімічна рівновага. Принцип зміщення хімічної рівноваги
Хімічна рівновага. Принцип зміщення хімічної рівноваги Хром. Химиялық қасиеттері
Хром. Химиялық қасиеттері Ферроқорытпа. Кремний және Хром
Ферроқорытпа. Кремний және Хром Дисперсные системы. (Лекция 6)
Дисперсные системы. (Лекция 6) Определение критических точек двойного сплава
Определение критических точек двойного сплава Природный газ
Природный газ Растворы. Приготовление растворов
Растворы. Приготовление растворов Атом құрылысы
Атом құрылысы Циклоалканы
Циклоалканы Органическая химия: Жиры
Органическая химия: Жиры Кремний и его соединения
Кремний и его соединения Chemical kinetics
Chemical kinetics Сопряжение электронной плотности, как фактор обеспечения стабильности молекул
Сопряжение электронной плотности, как фактор обеспечения стабильности молекул Научные основы и технологии зеленой химии
Научные основы и технологии зеленой химии