Слайд 2

Открытие алюминия
Впервые был получен датским физиком Эрстедем в 1925 году.
Название было
дано от латинского «alume»,так в древности назывались квасцы для крашения тканей.
Слайд 3

Применение
Применяется в одной из отраслей металлургии – алюмотермии
Алюминаты используются во многих
отраслях промышленности
В авиапромышленности
В фармацевтики
Для дубления кож
Для крашения тканей
Слайд 4

Электронное строение
Алюминий, как и все элементы, находящиеся в III группе, главной
подгруппе, имеет на последнем энергетическом уровне 3 электрона, что объясняет его амфотерные свойства.
Алюминий имеет радиус атома равный 0,125 нм.
Его восстановительные свойства хотя и велики, но значительно меньше, чем у элементов, стоящих в первой и второй группах, из-за уменьшения радиуса атома.
Слайд 5

Физические свойства
Самый распространенный металл в природе.
Легкий
Серебристо-белый
Пластичный
Не имеет характерного металлического блеска (покрыт
тонкой белой пленкой из оксида алюминия)
По электропроводности превосходит другие металлы, кроме серебра и меди
Температура плавления – 6600С
Образует с другими металлами легкие, но прочные сплавы
Слайд 6

Химические свойства
Алюминий активен, но при нормальных условиях активность снижена наличием прочной
оксидной пленки, которая защищает металл от атмосферных воздействий.
Обладает амфотерными свойствами
Слайд 7

Взаимодействует с…
Неметаллами
Кислородом
Щелочами
Водой
Кислотами
Оксидами металлов
Слайд 8

Соли алюминия (алюминаты)
Алюминат натрия используют для получения оксида алюминия в текстильной
промышленности, как протраву для тканей, в бумажной промышленности, для ионно-обменной очистки воды
Алюминат кальция – для приготовления быстротвердеющего цемента.
Алюминат бария – для очистки воды от сульфат-, карбонатионов и ионов кальция
Слайд 9

Взаимодействие с неметаллами
Способен к взаимодействию под действием температуры с серой, азотом
и углеродом.
С галогенами реагирует при нормальных условиях.
Слайд 10
![Взаимодействие со щелочами 2Al + 2NaOH + 6H2O=2Na[Al(OH)4] + 3H2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/291410/slide-9.jpg)
Взаимодействие со щелочами
2Al + 2NaOH + 6H2O=2Na[Al(OH)4] + 3H2
2NaOH + Al2O3
+ 3H2O=2Na[Al(OH)4]
2Al + 6H2O=3H2 +2Al(OH)3
NaOH + Al(OH)3=Na[Al(OH)4]
Слайд 11

Взаимодействие с водой
Если в отсутствии воздуха удалить с поверхности алюминия оксидную
пленку, то он активно реагирует с водой.
2Al + 6H2O=2H2 + 2Al(OH)3
Слайд 12

Взаимодействие с кислотами
Концентрированные серная и азотная кислоты пассивируют алюминий (образуется плотная
оксидная пленка).
При взаимодействии с разбавленными кислотами алюминий образует соли.
Слайд 13

Взаимодействие с кислородом
Алюминий взаимодействует с кислородом воздуха, образуя при этом оксид
алюминия, покрывающий металл тонкой плотной белой пленкой.
При сильном нагревании порошок алюминия воспламеняется и сгорает ослепительным белым пламенем.








![Взаимодействие со щелочами 2Al + 2NaOH + 6H2O=2Na[Al(OH)4] + 3H2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/291410/slide-9.jpg)



 Общая характеристика халькогенов. Кислород
Общая характеристика халькогенов. Кислород Нанохимия
Нанохимия Фосфор и его соединения. Электронные формулы атома фосфора
Фосфор и его соединения. Электронные формулы атома фосфора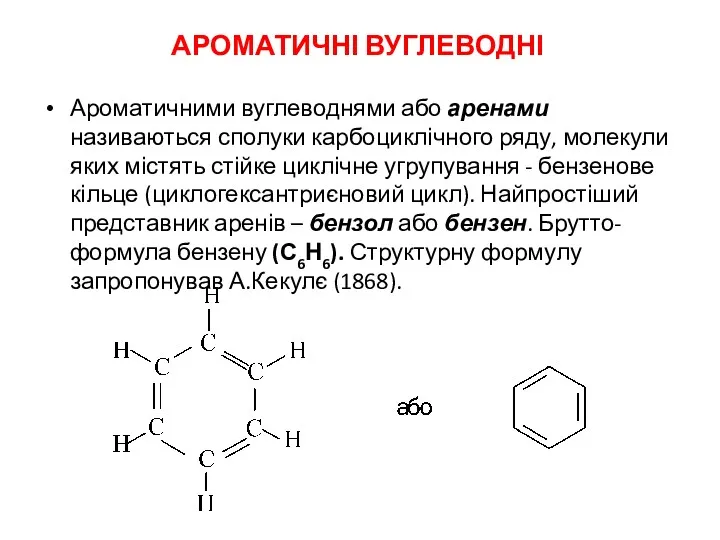 Ароматичні вуглеводні
Ароматичні вуглеводні Гидродинамические свойства полимеров. Полиэлектролиты
Гидродинамические свойства полимеров. Полиэлектролиты Біріншілік алкилсульфаттар және алкилэтоксисульфаттарды алу
Біріншілік алкилсульфаттар және алкилэтоксисульфаттарды алу Озон. Значение Озона
Озон. Значение Озона Обзор электродных процессов
Обзор электродных процессов Особенности химического состава клетки
Особенности химического состава клетки Хром. Элемент под № 24
Хром. Элемент под № 24 Полисахариды. Крахмал и целлюлоза
Полисахариды. Крахмал и целлюлоза Аминокислоты. Белки
Аминокислоты. Белки Металлические стёкла
Металлические стёкла Бета-лактамиды (природные и полусинтетические пенициллины и цефалоспорины)
Бета-лактамиды (природные и полусинтетические пенициллины и цефалоспорины) Кислоты, основания, соли в свете ТЭД
Кислоты, основания, соли в свете ТЭД Практическая работа по разделению смесей
Практическая работа по разделению смесей Свинец
Свинец Кислородные соединения азота
Кислородные соединения азота Буферные растворы
Буферные растворы Основные классы неорганических веществ. Соединения химических элементов
Основные классы неорганических веществ. Соединения химических элементов Резина. Состав и применение резины
Резина. Состав и применение резины Аминокислоты. Понятие аминокислот
Аминокислоты. Понятие аминокислот АЛКАНЫ Строение молекулы метана.
АЛКАНЫ Строение молекулы метана. Растворы. Классификация, способы выражения концентрации, свойства растворов
Растворы. Классификация, способы выражения концентрации, свойства растворов 20230205_okislitelno-vosstanovitelnye_reaktsii
20230205_okislitelno-vosstanovitelnye_reaktsii Хімічні властивості оксидів
Хімічні властивості оксидів Электролиз. Электролизеры
Электролиз. Электролизеры Моделирование структуры биомакромолекул
Моделирование структуры биомакромолекул