Содержание
- 2. Элемент VI группы побочной подгруппы Элемент 4-ого периода Массовая доля хрома в земной коре – 0,02%
- 3. Хромистый железняк FeO* Cr2O3 Хромит FeCr2O4 Крокоит PbCrO4 Нахождение в природе
- 4. Металл серебристо-белого цвета Хрупкий, с плотностью 7,2 г/см3 Физические свойства Температура плавления 18900C Самый твердый металл
- 5. 1.Реагирует с неметаллами(при нагревании) А)4Cr + 3O2 =2Cr2O3 Б)2Cr +3S = Cr2S3 2.Реагирует с парами воды(в
- 6. Применение хрома В производстве стали В нагревательных элементах электрических печей(сплав железа ,никеля и хрома) Хромирование (создание
- 7. Соединения хрома Соединения хрома(II) CrO –основный оксид Cr(OH)2- основание Соединения хрома(III) Cr2O3-амфотерный оксид Cr(OH)3-амфотерное соединение Соединения
- 8. Соли Хроматы(хромовой кислоты) Дихроматы(дихромовой кислоты) Дихроматы термически неустойчивые соединения. Реакция разложения дихромата аммония(опыт » Вулканчик») (NH4)2Cr2O7=Cr2O3+N2+4H2O
- 9. Применение соединений хрома Соединения хрома применяют в качестве минеральных красок Хромовую смесь используют для мытья химической
- 11. Скачать презентацию
 Имидазол. Получение, свойства, анализ, применение, условия хранения лекарственных препаратов производных имидазола
Имидазол. Получение, свойства, анализ, применение, условия хранения лекарственных препаратов производных имидазола Спирти. 3агальна характеристика спиртів
Спирти. 3агальна характеристика спиртів Алюминий. Характеристика алюминия по положению в ПСХЭ. Строение атома
Алюминий. Характеристика алюминия по положению в ПСХЭ. Строение атома Бром. Общие сведения
Бром. Общие сведения Композиты как материалы конструкционного назначения
Композиты как материалы конструкционного назначения Железо и его свойства
Железо и его свойства Витамины молока и молочных продуктов. Жирорастворимые витамины
Витамины молока и молочных продуктов. Жирорастворимые витамины Стратегії дослідження хімічних сполук з використанням сучасних фізичних методів (частина перша)
Стратегії дослідження хімічних сполук з використанням сучасних фізичних методів (частина перша)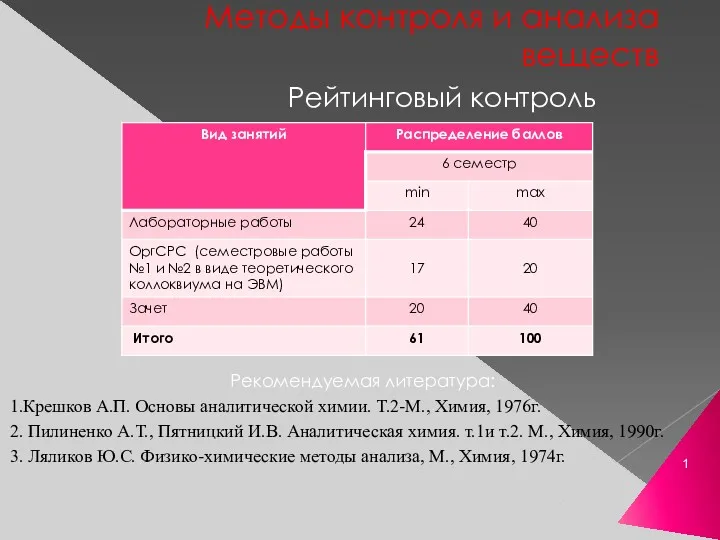 Методы контроля и анализа веществ
Методы контроля и анализа веществ Азотсодержащие органические соединения. Амины
Азотсодержащие органические соединения. Амины Азот – простое вещество. Неметаллы
Азот – простое вещество. Неметаллы Типы химических реакций
Типы химических реакций Химическая связь. Электроотрицательность и полярность связи
Химическая связь. Электроотрицательность и полярность связи Нефть и способы её переработки
Нефть и способы её переработки Калийные удобрения
Калийные удобрения Поняття про полімери на прикладі поліетилену. Використання поліетилену
Поняття про полімери на прикладі поліетилену. Використання поліетилену Внутренняя энергия и энтальпия. Классификация химических реакций по тепловому эффекту
Внутренняя энергия и энтальпия. Классификация химических реакций по тепловому эффекту Превращение веществ
Превращение веществ Взрывчатые вещества, их история и применение
Взрывчатые вещества, их история и применение Цинк. Месторождения. Применение
Цинк. Месторождения. Применение Растворы. Типы растворов
Растворы. Типы растворов Жёсткость воды
Жёсткость воды Роль хімії у житті суспільства
Роль хімії у житті суспільства Строение и свойства комплексных соединений
Строение и свойства комплексных соединений Проблема содержания нитратов в пищевых продуктах
Проблема содержания нитратов в пищевых продуктах Мини-тақталарда немесе дәптерде қатты, сұйық және газтектес заттардың құрылысын сал
Мини-тақталарда немесе дәптерде қатты, сұйық және газтектес заттардың құрылысын сал Общая электронная теория восстановления и окисления металлов
Общая электронная теория восстановления и окисления металлов Высокомолекулярные соединения и супрамолекулярные структуры. Синтез полимеров (Лекция 1)
Высокомолекулярные соединения и супрамолекулярные структуры. Синтез полимеров (Лекция 1)