Слайд 2

ПЛАН
Получение, свойства, анализ, применение, условия хранения лекарственных препаратов производных имидазола.
Получение, свойства,
анализ, применение, условия хранения лекарственных препаратов производных имидазолина.
Слайд 3

Имидазол — органическоесоединение класса гетероциклов,пятичленный цикл с двумя атомамиазота и тремя атомами углерода вцикле, изомерен пиразолу.
Слайд 4
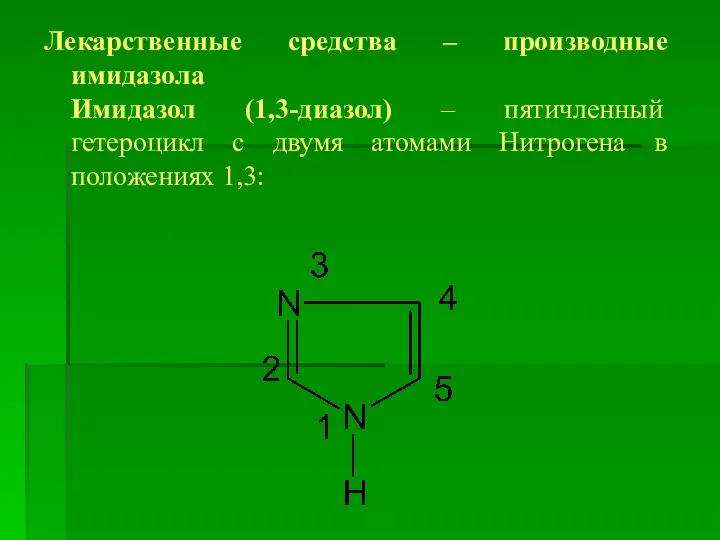
Лекарственные средства – производные имидазола
Имидазол (1,3-диазол) – пятичленный гетероцикл с двумя
атомами Нитрогена в положениях 1,3:
Слайд 5

Имидазол (температура плавления 90 °С, температура кипения 256 °С) – амфотерное
соединение, образующее соли и с сильными кислотами и с щелочными металлами.
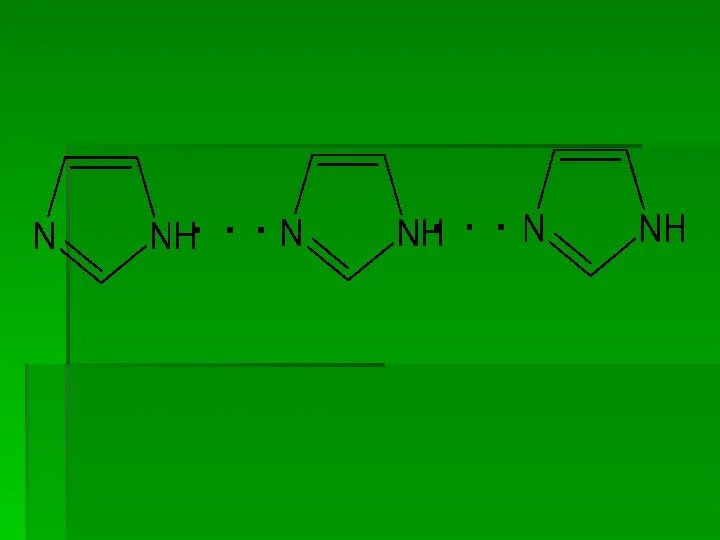
Наличие в молекуле имидазола кислотной иминогруппы* –NH (*имины – насыщенные гетероциклы с группой –NH в кольце) и основного атома Нитрогена –N= является причиной образования междумолекулярных ассоциатов за счет водородных связей:
Слайд 6

Свойства
В незамещенном имидазоле положения 4 и 5 (атомы углерода) равноценны, вследствие таутомерии.
Ароматичен,
реагирует с солями диазония (сочетание).
Нитруется и сульфируется только в кислой среде в положение 4, галогены в щелочной среде вступают по положению 2, в кислой - по положению 4.
Легко алкилируется и ацилируется по иминному N, раскрывает цикл при взаимодействии с растворами сильных кислот и пероксидов.
Катализирует гидролиз трудноомыляемых сложных эфиров и амидов карбоновых кислот.
На основе имидазола производят большое количество различных ионных жидкостей.
Слайд 7

Свойства имидазола
Имидазол проявляет ароматические свойства. Вступает в реакции с солями диазония,
нитруется, сульфируется только в кислой среде в положении 4(5); галогенирование происходит в щелочной среде в положении 2, в кислой среде – в положении 4(5). Легко алкируется и ацилируется по иминному (пиррольному) атому Нитрогена; при взаимодействии с растворами сильных щелочей и пероксидами происходит раскрытие цикла. Катализирует гидролиз трудно омыляющихся эстеров и амидов карбоновых кислот.
Слайд 8
Слайд 9
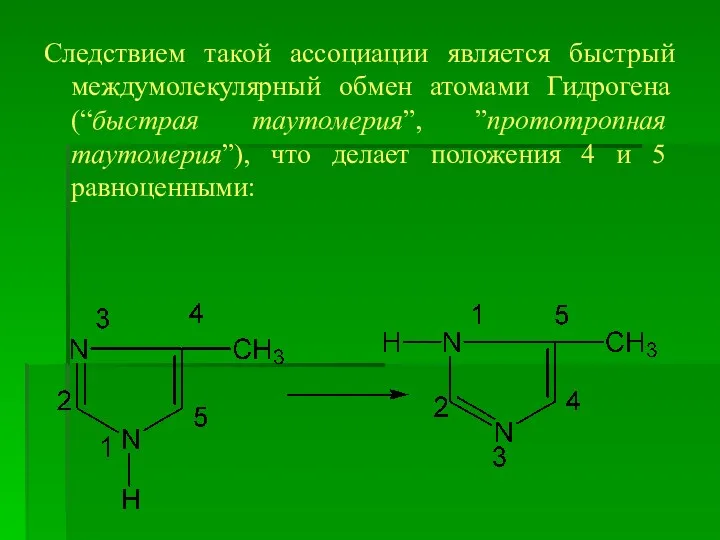
Следствием такой ассоциации является быстрый междумолекулярный обмен атомами Гидрогена (“быстрая таутомерия”,
”прототропная таутомерия”), что делает положения 4 и 5 равноценными:
Слайд 10

Получают имидазол взаимодействием глиоксаля (оксалатного альдегида ) с аммиаком NH3 и
формальдегидом НСНО.
К производным имидазола относятся такие лекарственные препараты: мерказолил, метронидазол.
Частично гидрированный имидазол в положениях 4,5 (4,5-дигидроимидазол) называют имидазолин.
Слайд 11
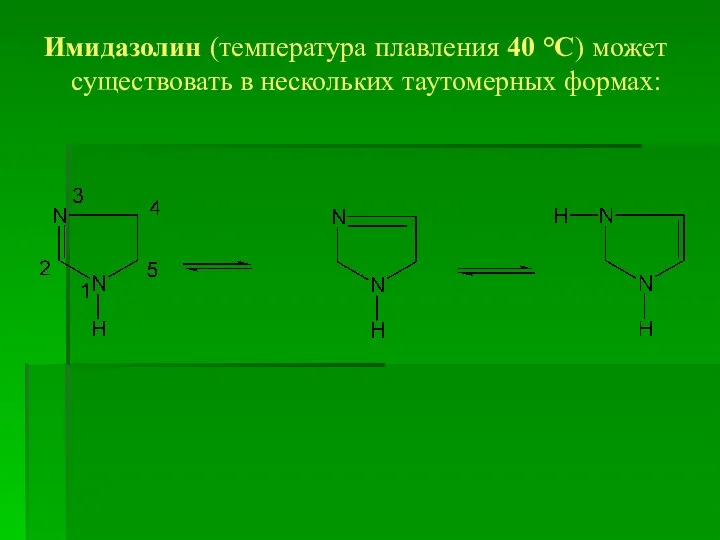
Имидазолин (температура плавления 40 °С) может существовать в нескольких таутомерных формах:
Слайд 12

Имидазолин (температура плавления 40 °С) может существовать в нескольких таутомерных формах:
Это сильное основание, с растворами щелочей реагирует с раскрытием цикла; при дегидрировании в присутствии Ni-катализатора при 350–400 °С образует имидазол. Получают пропусканием N,N’-диформилэтилендиамина над силикагелем при 400–600 °С.
Имидазолин – это структурный элемент молекул таких препаратов, как: нафтизин (син. санорин), ксилометазолин (син. галазолин), клонидина гидрохлорид (клофелин).
Слайд 13

Имидазол инструкция по применению
К клотримазолу чувствительны дерматофиты, дрожжеподобные грибы рода Candida,
Torulopsis glabrata, Rhodotorula, плесневые грибы, а также возбудитель разноцветного лишая Pityriasis versicolor и возбудитель эритразмы.
Даже однократное применение этого лекарственного средства может привести к серьезным нарушениям в процессе внутриутробного формирования плода в первом триместре беременности.
В состав входит гормональные компонент, что с одной стороны помогает быстро устранить воспалительные проявления, а с другой стороны может негативно воздействовать на состояние стероидного баланса организма женщины.
Имидазол инструкция по применению скачать
В отличие от других противогрибковых препаратов является комплексным средством, в составе которого уникальным образом сочетаются нистатин и тернидазол, неомицин в форме сульфата и преднизолон.
Это значительно расширяет спектр патогенного воздействия в отношении большого количества микроорганизмов.
Слайд 14

Методы получения
Впервые имидазол был получен Генрихом Дебюсом в 1858 г. конденсацией глиоксаляВпервые
имидазол был получен Генрихом Дебюсом в 1858 г. конденсацией глиоксаля с аммиакомВпервые имидазол был получен Генрихом Дебюсом в 1858 г. конденсацией глиоксаля с аммиаком и формальдегидом[1], этот метод может использоваться и в синтезе замещенных имидазолов:
В лабораторной практике имидазол синтезируют декарбоксилированием 4,5-имидазолдикарбоновой кислоты, получаемой окислениембензимидазола.
Слайд 15
![Биологическая роль[правитьБиологическая роль[править | править вики-текст] Имидазольный цикл входит в](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/336904/slide-14.jpg)
Биологическая роль[правитьБиологическая роль[править | править вики-текст]
Имидазольный цикл входит в состав незаменимой аминокислотыИмидазольный цикл входит
в состав незаменимой аминокислоты гистидина.
Структурный фрагмент гистамина, пуриновых оснований, ряда лекарственных средств (дибазолСтруктурный фрагмент гистамина, пуриновых оснований, ряда лекарственных средств (дибазол, метапрот и др.).













![Биологическая роль[правитьБиологическая роль[править | править вики-текст] Имидазольный цикл входит в](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/336904/slide-14.jpg)
 Теории кислот и оснований
Теории кислот и оснований Брейн – ринг. Мини – ЕГЭ по химии
Брейн – ринг. Мини – ЕГЭ по химии Физическая химия. Химическая термодинамика
Физическая химия. Химическая термодинамика Ненасыщенные (непредельные) алифатические углеводороды. Алкены
Ненасыщенные (непредельные) алифатические углеводороды. Алкены Кислоты. Классификация кислот по строению кислотного остатка
Кислоты. Классификация кислот по строению кислотного остатка Неметаллы: общая характеристика. 9 класс
Неметаллы: общая характеристика. 9 класс Комплексонометрлік титрлеу
Комплексонометрлік титрлеу Нітроген
Нітроген Простые вещества — металлы и неметаллы
Простые вещества — металлы и неметаллы Сандық есептер (металдар мен оның қосылыстарындағы генетикалық байланысты көрсететін)
Сандық есептер (металдар мен оның қосылыстарындағы генетикалық байланысты көрсететін) Спекание порошковых систем
Спекание порошковых систем Органическая химия. Ацетилен
Органическая химия. Ацетилен Изучение раздела Углеводороды в курсе органической химии в старшей школе
Изучение раздела Углеводороды в курсе органической химии в старшей школе Электроизоляционные лаки, эмали, компаунды
Электроизоляционные лаки, эмали, компаунды Определение качественного состава минеральных вод
Определение качественного состава минеральных вод Использование методов проблемного обучения на уроках химии
Использование методов проблемного обучения на уроках химии Кислородные соединения серы. 2 часть
Кислородные соединения серы. 2 часть Алюминий AL- химический элемент
Алюминий AL- химический элемент Трансмиссионные масла
Трансмиссионные масла Профілактика захворювань незбалансованого харчування. Харчові добавки
Профілактика захворювань незбалансованого харчування. Харчові добавки Соли как производные кислот и оснований
Соли как производные кислот и оснований Органикалық химияға кіріспе. Органикалық заттардың ерекшеліктері
Органикалық химияға кіріспе. Органикалық заттардың ерекшеліктері IVA группа С, Si, Ge, Sn, Pb (подгруппа титана)
IVA группа С, Si, Ge, Sn, Pb (подгруппа титана) Бериллий. Строение элемента. Физические и химические свойства. Способы получения. Применение. Интересные факты. Опыты
Бериллий. Строение элемента. Физические и химические свойства. Способы получения. Применение. Интересные факты. Опыты Мыльное чудо своими руками. История мыловарения. Изготовление мыла в домашних условиях
Мыльное чудо своими руками. История мыловарения. Изготовление мыла в домашних условиях Физико-химические и пожароопасные свойства углеводородов. (Тема 3.1)
Физико-химические и пожароопасные свойства углеводородов. (Тема 3.1) Техника безопасности в кабинете химии
Техника безопасности в кабинете химии Мультимедийная презентация Углерод. Характеристика химического элемента
Мультимедийная презентация Углерод. Характеристика химического элемента