Содержание
- 2. Литература 1. Глинка Н.Л. Общая химия. М.; Интеграл – Пресс. 2009г. 728 с. 2. Коробейникова Е.Г.
- 3. Ознакомиться с физико-химическими и пожароопасными свойствами алифатических углеводородов, способами получения, областью применения в профессии. Цели занятия:
- 4. 1. Алифатические углеводороды, их физико-химические и пожароопасные свойства. 2. Сравнительная характеристика пожарной опасности углеводородов. 3. Галогенпроизводные
- 5. Многие органические соединения являются пожаро-взрывоопасными: - Природные газы: метан этан, пропан, бутан – горючие вещества. -
- 6. Углеводороды – органические вещества, состоящие из углерода и водорода. Алканы (предельные) – СnH2n+2 Алкены (непредельные) –
- 7. Алканы (предельные, насыщенные, парафиновые углеводороды) - соединения углерода с водородом, в которых атомы углерода связаны между
- 8. Гомологический ряд алканов
- 9. 1. Выделяют из природных источников (газ, нефть, каменный уголь, горючие сланцы) – ректификация. 2. Газификация угля:
- 10. Все алканы нерастворимы в воде. Плотность d С1 – С4 – газы; С5 – С15 –
- 11. Алканы малоактивны, не обесцвечивают бромную воду и KMnO4. Вступают в реакции: - замещения – галогенирования; -
- 12. Общее уравнение реакции горения углеводорода СmHn + (m+n/4)O2 = mCO2 + n/2H2O + Q, где m
- 13. Водород у алканов замещается на галогены по свободно-радикальному механизму: CH4 + CI2 → CH3CI + HCI
- 14. Горение: С5Н12 + 8(О2 + 3,76N2) + 5CO2 + 6H2O + 8 * 3,76 N2 Каталитическое
- 15. Метан СН4 – болотный, рудниковый газ. Взрывается с воздухом в пределах 4 – 16%об.при температуре 600
- 16. Алкены (непредельные, ненасыщенные, олефины) – соединения углерода с водородом, в которых атомы углерода связаны между собой
- 17. Гомологический ряд алкенов
- 18. Алкены обладают четырьмя видами изомерии: - углеродного скелета; - кратной (двойной) связи; - пространственной; - межклассовой.
- 19. С2 – С4 – газы; С5 – С17 – жидкости; С19 > твердые вещества. Нерастворимы в
- 20. Этилен и его гомологи химически активны. Вступают в реакции присоединения, окисления и полимеризации. Этилен горит коптящим
- 21. 1. Крекингом алканов: С8Н18 → С4Н8 + С4Н10 2. Дегалогенирование галогеналканов: СН2Br = CH2Br + Zn
- 22. Алкины – представитель ацетилен – С2Н2 Ацетилен С2Н2 – бесцв. газ, немного растворим в воде. Горючий
- 23. Вступают в реакции присоединения (ступенчато), разложения, полимеризации (тримеризация ацетилена: 3С2Н2 → С6Н6) Алкины горят ярким пламенем,
- 24. Бутадиен – 1,3. СН2=СН-СН=СН2 С4Н6 С4Н6 – газ, остальные диеновые – жидкости. Характерны реакции присоединения: СН2=СН-СН=СН2
- 25. 1. Из этилового спирта (реакция Лебедева): 2С2Н5ОН → СН2=СН-СН=СН2 + 2Н2О +Н2 бутадиен – 1,3 2.
- 26. Этан Этилен Этин Составить самостоятельно таблицу характеристики для трех газов, используя учебник Глинка Н.Л. по вопросам:
- 27. CH3CI CHCI3 CHI3 хлорметан хлороформ иодоформ Имеют характерный запах, многие обладают наркотическими свойствами. Температура кипения и
- 28. Реакцией замещения: С2Н6 + Br2 → C2H5Br + HBr Гидрогалогенирование: СН3 – СН = СН2 +
- 29. Хлороформ СНCl3 впервые был синтезирован в 1831 году одновременно Либихом и Субейраном. В 1848 году хлороформ
- 30. Хлористый этил (хлорэтан) С2Н5Сl при обычных условиях газ с температурой кипения +120С. При сравнительно небольшом охлаждении
- 31. Все углеводороды являются горючими. Некоторые окислители вызывают самовозгорание органических веществ при смешивании или соприкосновении. 3. Взрыво-пожароопасные
- 32. Ацетилен, метан и этилен в смеси с хлором самовозгорается: С2Н2 + Cl2 = 2HCI + 2C
- 33. Четыреххлористый углерод и четырехбромистый углерод дают со щелочными металлами взрыв при нагревании смеси до 65 –
- 34. Дополнить лекцию учебник Глинка Н.Л. С.561 -565. Построить 5 изомеров для С8Н14 указать класс вещества, назвать
- 36. Скачать презентацию

































 Карбоновые кислоты и их гетерофункциональные производные
Карбоновые кислоты и их гетерофункциональные производные Химические превращения веществ
Химические превращения веществ Химический элемент. Неон
Химический элемент. Неон Вода — это уникальное вещество
Вода — это уникальное вещество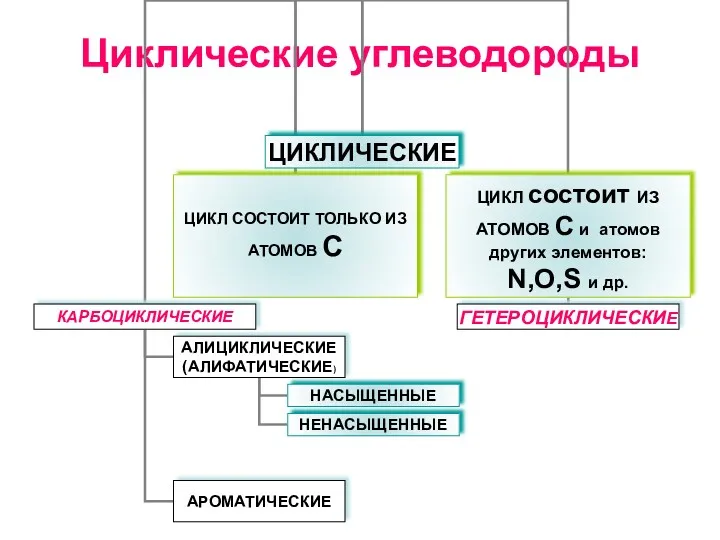 Циклические углеводороды
Циклические углеводороды Мембранный транспорт ионов: электродиффузионная теория
Мембранный транспорт ионов: электродиффузионная теория Углерод и кремний
Углерод и кремний Изменения, происходящие с белками в процессах технологической переработки сырья
Изменения, происходящие с белками в процессах технологической переработки сырья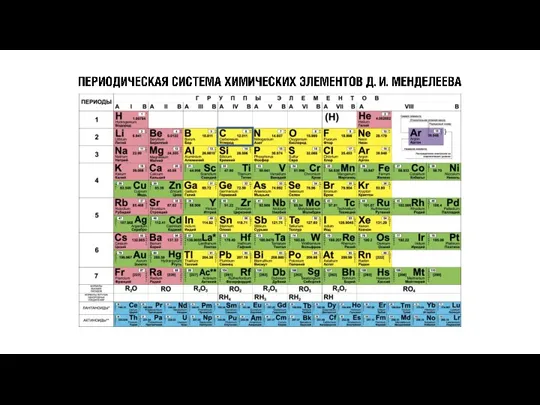 Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Все о чае
Все о чае Массовая доля элемента в сложном веществе
Массовая доля элемента в сложном веществе Химическая кинетика
Химическая кинетика La notion de catabolisme et d’anabolisme. La bioenergetique. La chaine mitochondriale de transfert d’electrons
La notion de catabolisme et d’anabolisme. La bioenergetique. La chaine mitochondriale de transfert d’electrons Сера и её соединения
Сера и её соединения osobennosti_i_klassifikatsiya_khimicheskikh_reaktsiy_v_organicheskoy_khimii
osobennosti_i_klassifikatsiya_khimicheskikh_reaktsiy_v_organicheskoy_khimii Кислотно-основное равновесие в процессах жизнедеятельности. Ионное произведение воды. Водородный показатель
Кислотно-основное равновесие в процессах жизнедеятельности. Ионное произведение воды. Водородный показатель Растворимость. Равновесие системы осадок-раствор
Растворимость. Равновесие системы осадок-раствор Производные бис-(β-хлорэтил)-амина, препараты для лечения онкозаболеваний
Производные бис-(β-хлорэтил)-амина, препараты для лечения онкозаболеваний Фотохимические превращения ДНК. Люминесцентные метки и зонды и их применение в биологии и медицине
Фотохимические превращения ДНК. Люминесцентные метки и зонды и их применение в биологии и медицине Хімічні властивості кислот
Хімічні властивості кислот Химические реакции. (8 класс)
Химические реакции. (8 класс) Способы раскисления и модифицирования стали
Способы раскисления и модифицирования стали Оксиды углерода
Оксиды углерода Основные классы неорганических соединений
Основные классы неорганических соединений Фенолы. Классификация фенолов
Фенолы. Классификация фенолов Пурин нуклеозидтері (аденозии 3-фосфор қышқылы, рибоксии). Сапасына Қойылантын талаптар, талдау әдістері
Пурин нуклеозидтері (аденозии 3-фосфор қышқылы, рибоксии). Сапасына Қойылантын талаптар, талдау әдістері Ендотермічні реакції на службі людини
Ендотермічні реакції на службі людини Обмен жиров в организме
Обмен жиров в организме