Содержание
- 2. Разминка НСl Н2SО4 НNО3 Н3РО4 СаСl2 Н2SiО3 Мg(NO3)2 НI К3РО4 НNO2 Cu(OH)2 Серная кислота Соляная кислота
- 3. Актуализация знаний -Какие явления происходят в природе? -Что такое химическое явление? -Каковы признаки химических реакций? -Что
- 4. Эпиграф «Вопросов полон мир, - кто даст на них ответ?» О.Хайам.
- 5. Урок химии с элементами поиска в 8 классе «Основные типы химических реакций»
- 6. Цели урока: повторить сущность химических реакций; познакомиться с типами химических реакций: соединения и разложения; закрепить навыки
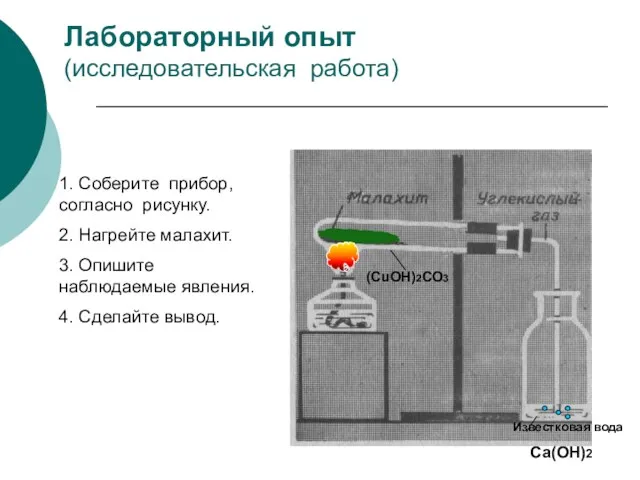
- 7. Лабораторный опыт (исследовательская работа) 1. Соберите прибор, согласно рисунку. 2. Нагрейте малахит. 3. Опишите наблюдаемые явления.
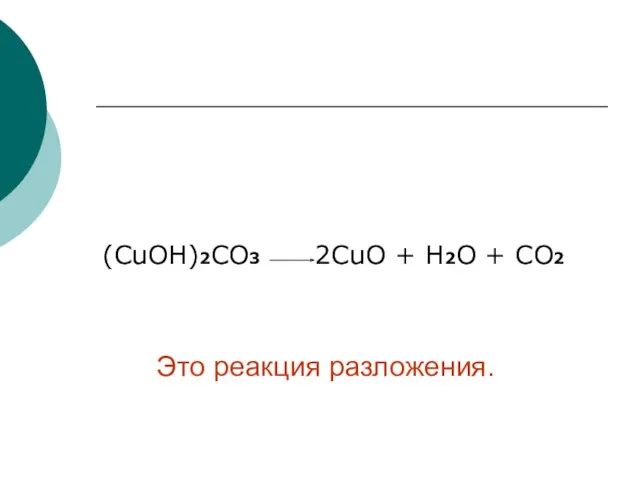
- 8. (СuОН)2СО3 2СuО + Н2О + СО2 Это реакция разложения.
- 9. Значение реакций соединения и разложения в природе и жизни человека Разрушение меловых гор, образование сталактитов СаСО3
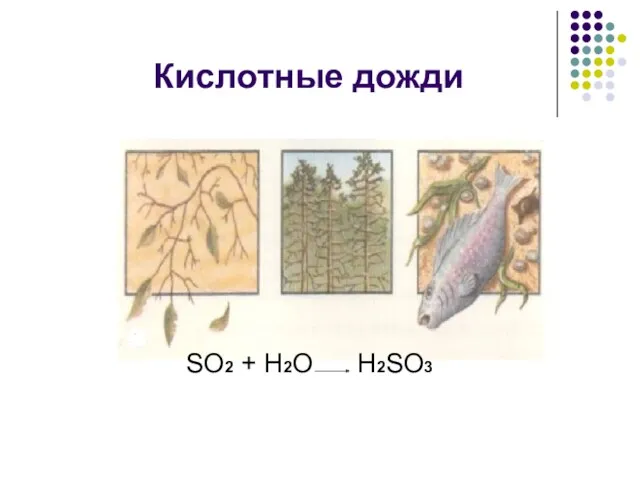
- 10. Кислотные дожди SО2 + Н2О Н2SО3
- 11. Кипячение воды в чайнике Мg(НСО3)2 МgСО3 + СО2 + Н2О
- 12. Брожение глюкозы в дрожжевом тесте дрожжи С6Н12О6 2 С2Н5ОН + 2 СО2 глюкоза этанол углекислый газ
- 13. Самостоятельная работа. Расставьте коэффициенты и отметьте известный вам тип реакции Уровень А а) Сг2О3 + Аl
- 14. Уровень А а) Сг2О3 + 2Аl → Аl2О3 + 2Сг; б) 2HI → Н2 + I2;
- 16. Скачать презентацию










 Щелочные металлы IА группы. Литий
Щелочные металлы IА группы. Литий Натуральный каучук
Натуральный каучук Получение и применение спиртов
Получение и применение спиртов Сложные эфиры. Жиры
Сложные эфиры. Жиры Розрахунки за хімічними рівняннями
Розрахунки за хімічними рівняннями Свойства кислот
Свойства кислот Методы разделения и концентрирования. Хроматографические методы
Методы разделения и концентрирования. Хроматографические методы Теория электролитической диссоциации (ТЭД)
Теория электролитической диссоциации (ТЭД) Электронное строение атома. Периодический закон
Электронное строение атома. Периодический закон Азотная кислота и ее свойства
Азотная кислота и ее свойства Історія відкриття періодичної системи хімічних елементів
Історія відкриття періодичної системи хімічних елементів Химия p-элементов. VI и VII группы главные подгруппы
Химия p-элементов. VI и VII группы главные подгруппы Общая характеристика и классификация топлива
Общая характеристика и классификация топлива Подготовка к ГИА. А9. Химические свойства простых веществ: металлов и неметаллов
Подготовка к ГИА. А9. Химические свойства простых веществ: металлов и неметаллов Минералы. Свойства минералов
Минералы. Свойства минералов Глицерин. Свойства и применение
Глицерин. Свойства и применение топ през
топ през Алканы. Состав, строение, свойства и химические превращения. Экологические последствия. Синтезы генетическая связь
Алканы. Состав, строение, свойства и химические превращения. Экологические последствия. Синтезы генетическая связь Алгоритм определения вида связи по формуле вещества
Алгоритм определения вида связи по формуле вещества III А – топтың элементтері
III А – топтың элементтері Алюминий и его соединения. Строение атома
Алюминий и его соединения. Строение атома Молекулярные и немолекулярные вещества
Молекулярные и немолекулярные вещества Обезвреживающая функция печени
Обезвреживающая функция печени Химическая связь
Химическая связь Происхождение нефти
Происхождение нефти Генетическая связь между классами неорганических веществ
Генетическая связь между классами неорганических веществ Контрольная работа по дисциплине: химия
Контрольная работа по дисциплине: химия Почва. Интегрированный урок по химии и географии
Почва. Интегрированный урок по химии и географии