Содержание
- 2. Назначение презентации Презентация предназначена для использования в качестве наглядного материала при изучении темы «Кислоты» на уроках
- 3. Преимущества презентации Содержит опорные схемы, способствующие быстрому запоминанию учащимися учебного материала; Содержит анимацию «Изменение окраски индикаторов»,
- 4. Na2CO3 Cu(OH)2 FeO AlCl3 MgBr2 NaOH CO2 NiO Ca(OH)2 HCl H2SO4 H2SiO3
- 5. КИСЛОТЫ Тема урока
- 6. Цель урока: познакомиться с классификациями и общими химическими свойствами кислот.
- 7. План урока Классификации кислот Физические свойства кислот Химические свойства кислот
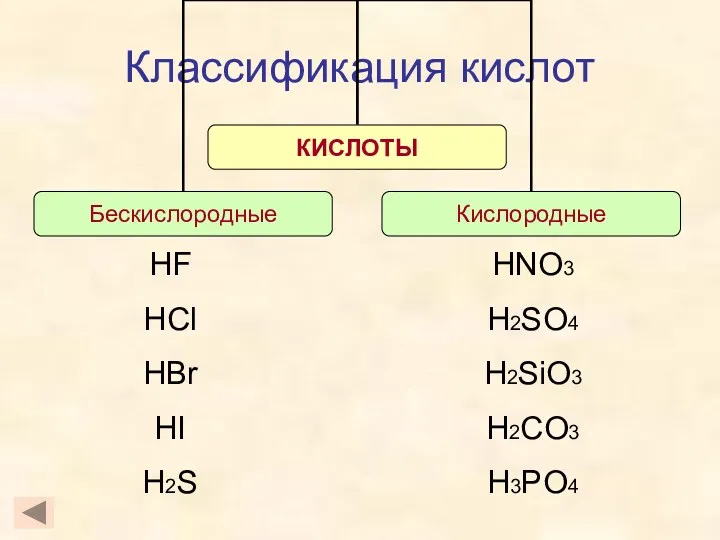
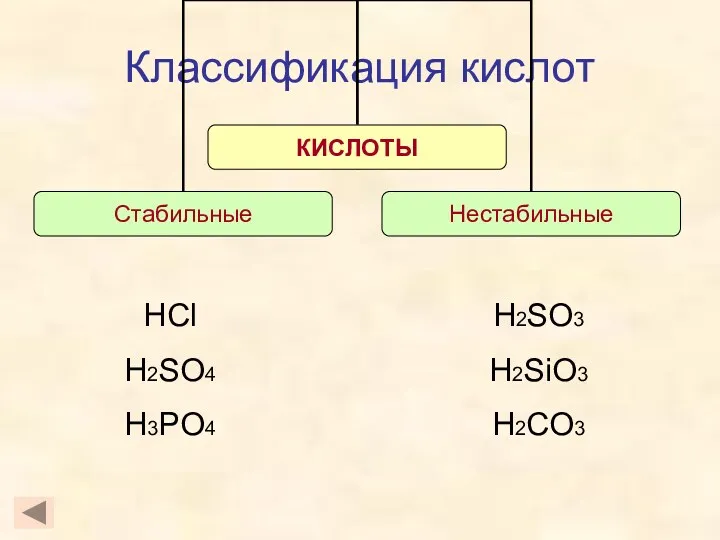
- 8. Классификация кислот HF HCl HBr HI H2S HNO3 H2SO4 H2SiO3 H2CO3 H3PO4
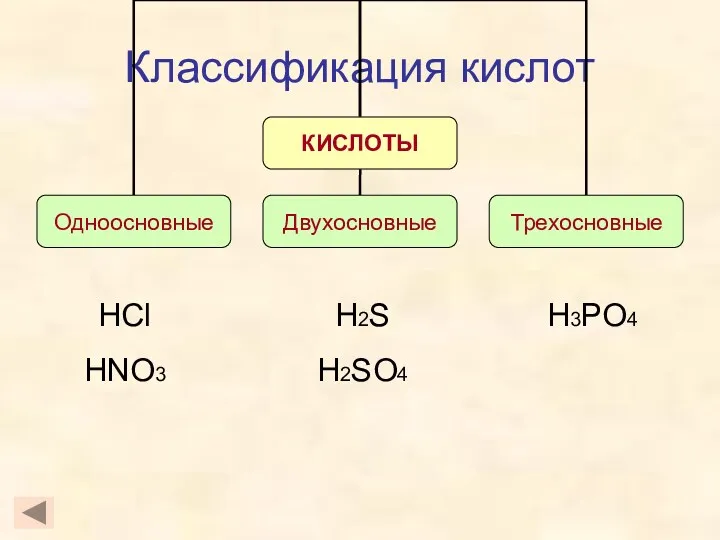
- 9. Классификация кислот HCl HNO3 H3PO4 H2S H2SO4
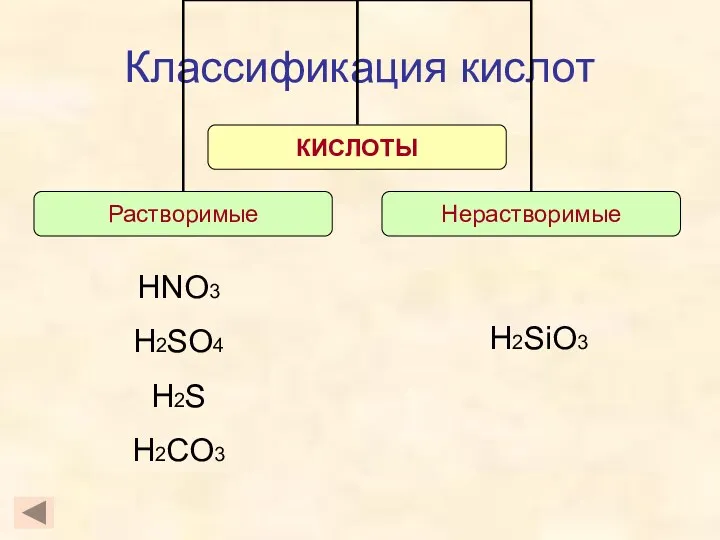
- 10. Классификация кислот H2SiO3 HNO3 H2SO4 H2S H2CO3
- 11. Классификация кислот HCl H2SO4 H3PO4 H2SO3 H2SiO3 H2CO3
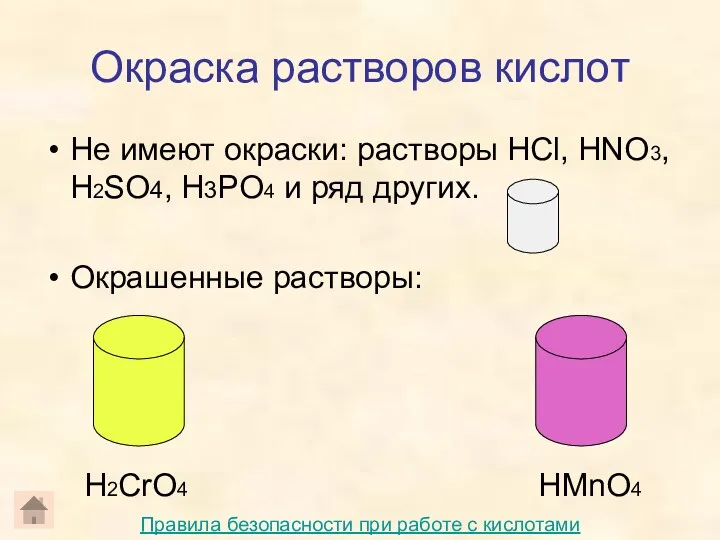
- 12. Окраска растворов кислот Не имеют окраски: растворы HCl, HNO3, H2SO4, H3PO4 и ряд других. Окрашенные растворы:
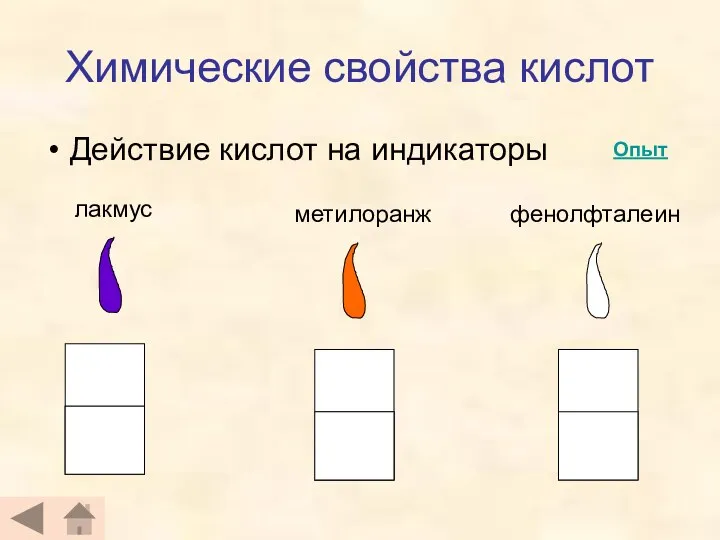
- 13. Химические свойства кислот Действие кислот на индикаторы лакмус метилоранж фенолфталеин Опыт
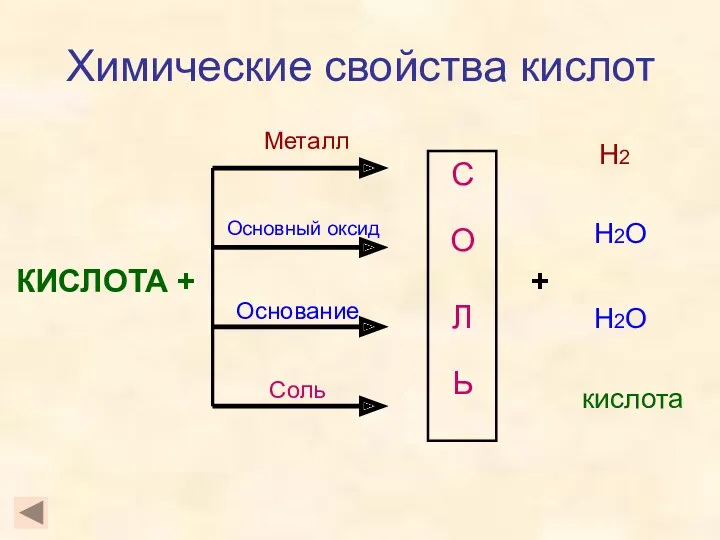
- 14. Химические свойства кислот КИСЛОТА + С О Л Ь Металл Основный оксид Основание Соль + Н2
- 15. Химические свойства кислот Кислота + металл = соль + водород Ряд активности металлов: Li K Ba
- 16. Химические свойства кислот Кислота + основный оксид = соль + вода Опыт. Взаимодействие оксида меди (Опыт.
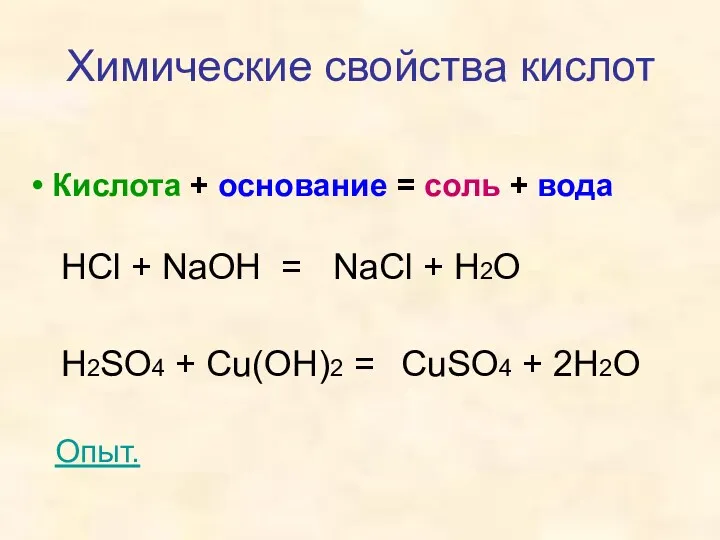
- 17. Кислота + основание = соль + вода Химические свойства кислот HCl + NaOH = H2SO4 +
- 18. Химические свойства кислот Кислота 1 + соль 1 = соль 2 + Кислота 2 Условия реакции:
- 19. Составьте возможные уравнения реакций взаимодействия перечисленных веществ с раствором серной кислоты.
- 20. Спасибо за внимание!
- 22. Скачать презентацию










 Решение задач в химии (ОГЭ, ЕГЭ, Олимпиады)
Решение задач в химии (ОГЭ, ЕГЭ, Олимпиады) Катализаторы. Ферменты
Катализаторы. Ферменты Электролитическая диссоциация веществ
Электролитическая диссоциация веществ Элементный, фракционный и химический состав нефти. Классификация нефтей
Элементный, фракционный и химический состав нефти. Классификация нефтей Галогены. Расположите галогены в порядке их открытия
Галогены. Расположите галогены в порядке их открытия Атомно-кристаллическое строение материалов
Атомно-кристаллическое строение материалов Сероводород, Сульфиды. Оксид серы (IV). Сернистая кислота
Сероводород, Сульфиды. Оксид серы (IV). Сернистая кислота Реакции при нагревании
Реакции при нагревании Природные источники углеводородов
Природные источники углеводородов Суды тазарту әдістері
Суды тазарту әдістері Алюминий. Сплавы алюминия
Алюминий. Сплавы алюминия Молярный объем. Закон Авогадро
Молярный объем. Закон Авогадро Силикаты (класс). Подкласс филлосиликаты (слоистые/листовые силикаты). Семейство слюды
Силикаты (класс). Подкласс филлосиликаты (слоистые/листовые силикаты). Семейство слюды Вода и здоровье
Вода и здоровье Атмосфера. Химия стратосферы
Атмосфера. Химия стратосферы Углерод. Аллотропные модификации
Углерод. Аллотропные модификации Сплав золота и серебра - электрум
Сплав золота и серебра - электрум Алкени та алкіни
Алкени та алкіни Комплексні сполуки
Комплексні сполуки Марганец и его соединения
Марганец и его соединения Методы определения механических свойств полимерных композиционных материалов
Методы определения механических свойств полимерных композиционных материалов Свойства простых веществ в свете ОВР
Свойства простых веществ в свете ОВР Углеводы (сахариды)
Углеводы (сахариды) Простые и сложные вещества. Химический элемент
Простые и сложные вещества. Химический элемент Химическая посуда и лабораторное оборудование
Химическая посуда и лабораторное оборудование Кислородные соединения азота
Кислородные соединения азота Химические свойста воды
Химические свойста воды Химическое равновесие
Химическое равновесие