Содержание
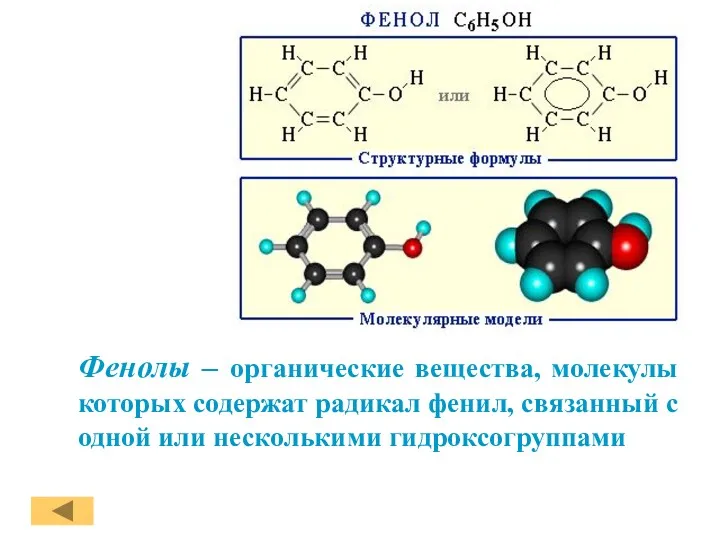
- 2. Фенолы – органические вещества, молекулы которых содержат радикал фенил, связанный с одной или несколькими гидроксогруппами
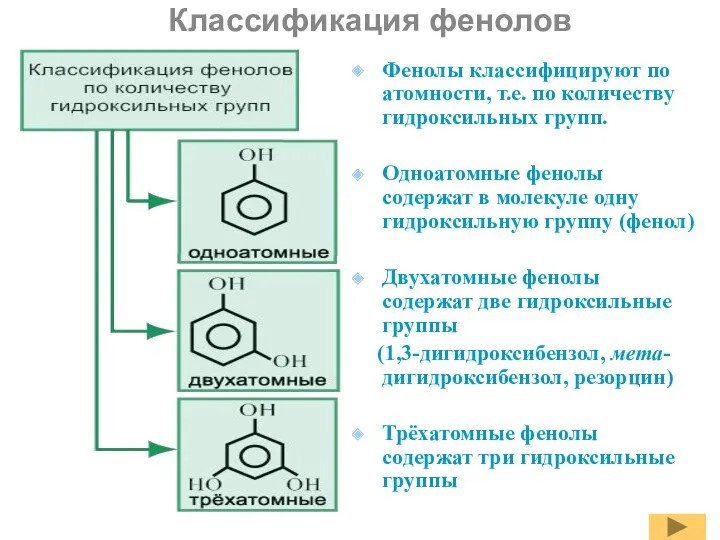
- 3. Фенолы классифицируют по атомности, т.е. по количеству гидроксильных групп. Одноатомные фенолы содержат в молекуле одну гидроксильную
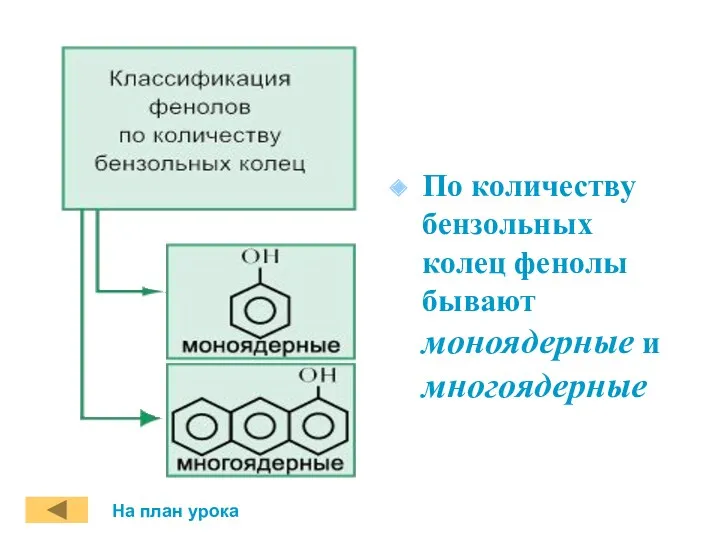
- 4. По количеству бензольных колец фенолы бывают моноядерные и многоядерные На план урока
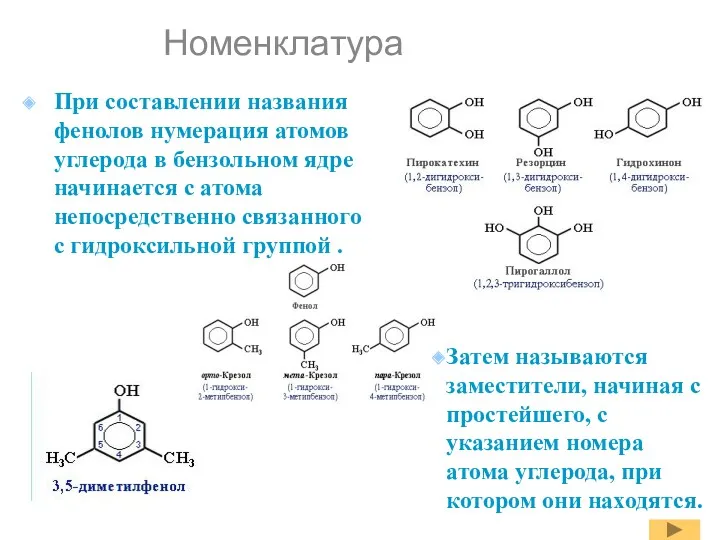
- 5. Номенклатура При составлении названия фенолов нумерация атомов углерода в бензольном ядре начинается с атома непосредственно связанного
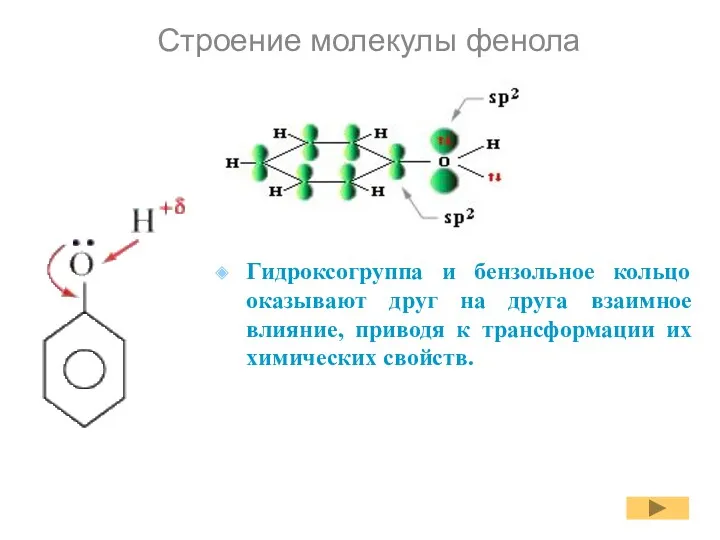
- 6. Строение молекулы фенола Гидроксогруппа и бензольное кольцо оказывают друг на друга взаимное влияние, приводя к трансформации
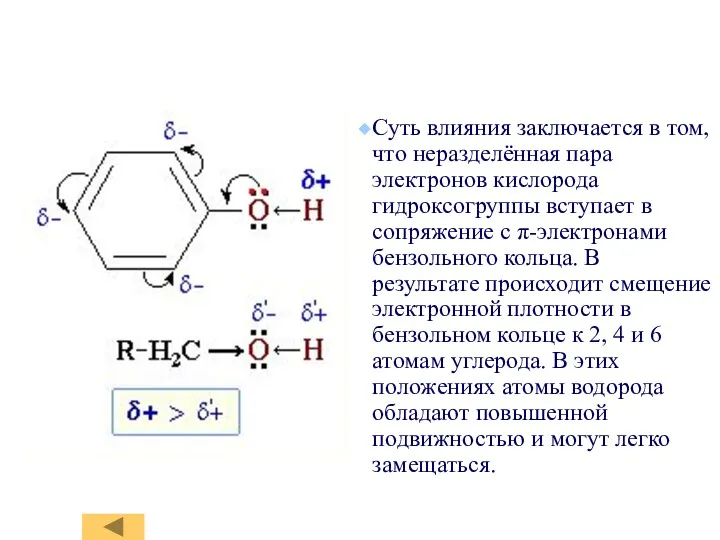
- 7. Суть влияния заключается в том, что неразделённая пара электронов кислорода гидроксогруппы вступает в сопряжение с π-электронами
- 8. Физические свойства фенола Фенол - твёрдое бесцветное кристаллическое вещество. Вследствие частичного окисления на воздухе он бывает
- 9. Химические свойства фенола Химические свойства фенола обусловлены наличием в его молекуле гидроксильной группы бензольного ядра
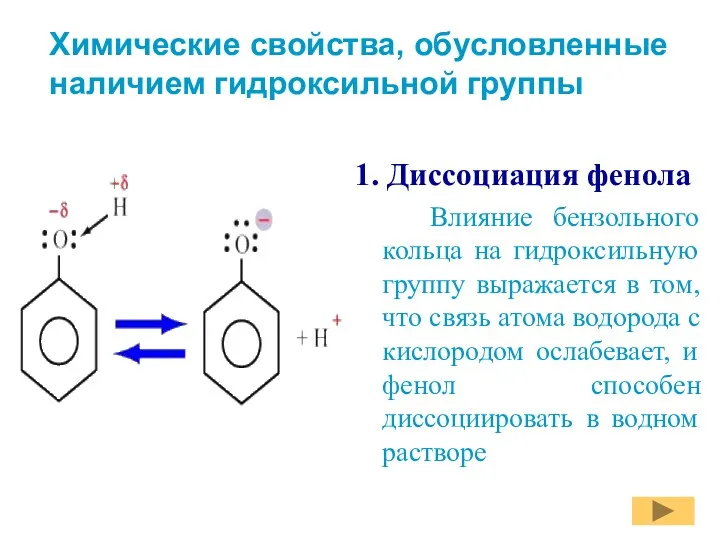
- 10. Химические свойства, обусловленные наличием гидроксильной группы 1. Диссоциация фенола Влияние бензольного кольца на гидроксильную группу выражается
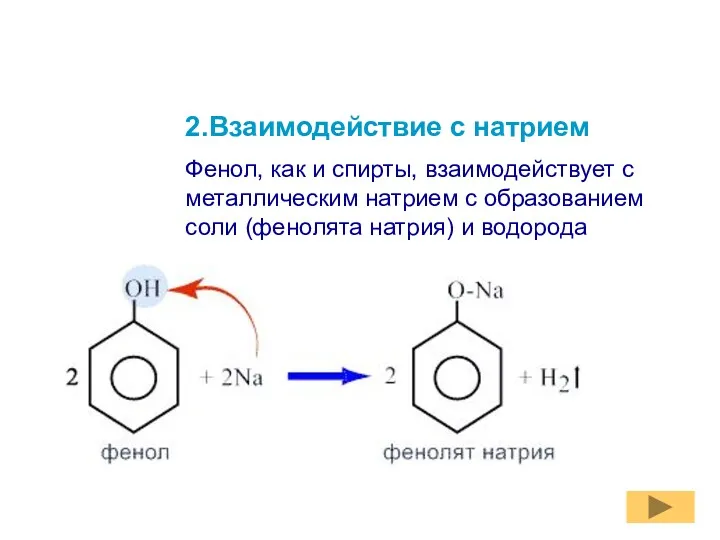
- 11. 2.Взаимодействие с натрием Фенол, как и спирты, взаимодействует с металлическим натрием с образованием соли (фенолята натрия)
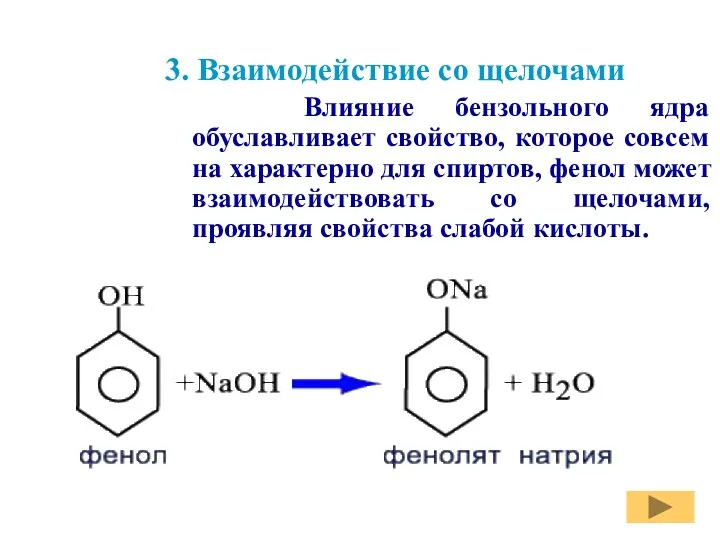
- 12. 3. Взаимодействие со щелочами Влияние бензольного ядра обуславливает свойство, которое совсем на характерно для спиртов, фенол
- 13. Химические свойства, обусловленные наличием бензольного ядра
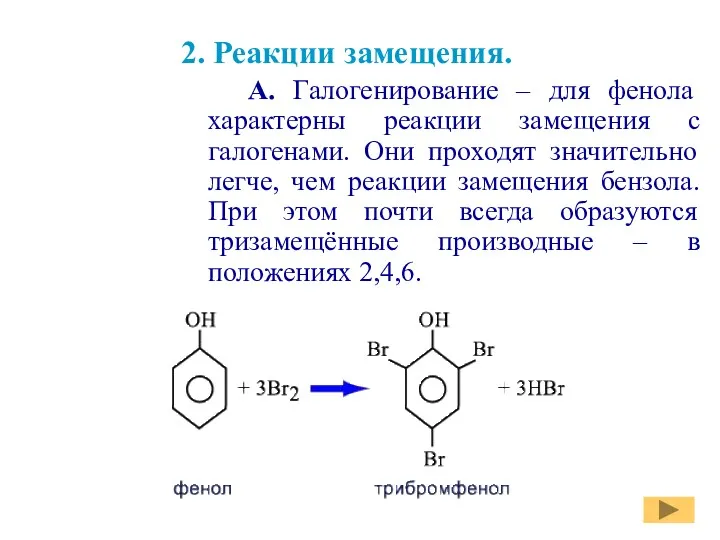
- 14. 2. Реакции замещения. А. Галогенирование – для фенола характерны реакции замещения с галогенами. Они проходят значительно
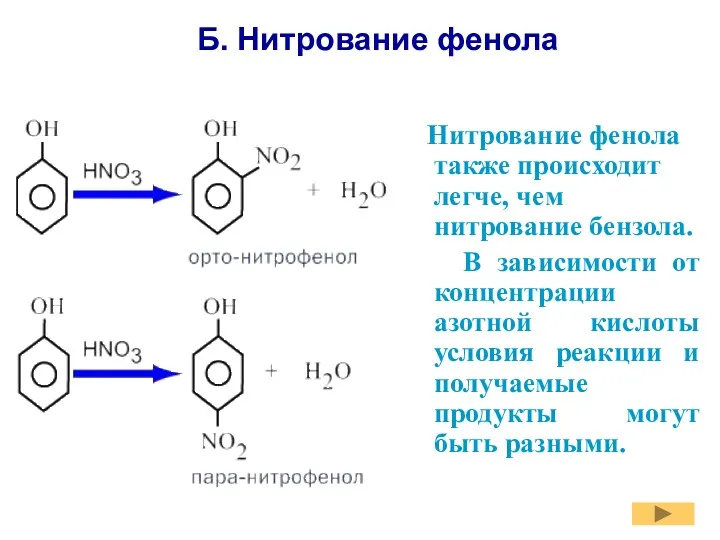
- 15. Б. Нитрование фенола Нитрование фенола также происходит легче, чем нитрование бензола. В зависимости от концентрации азотной
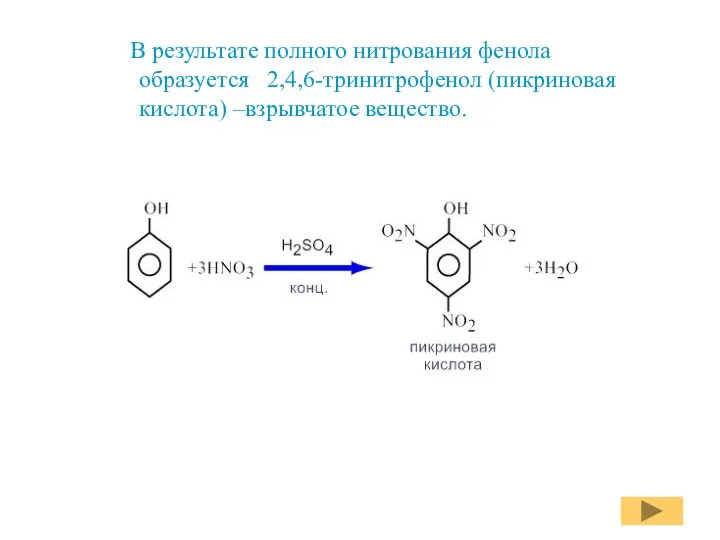
- 16. В результате полного нитрования фенола образуется 2,4,6-тринитрофенол (пикриновая кислота) –взрывчатое вещество.
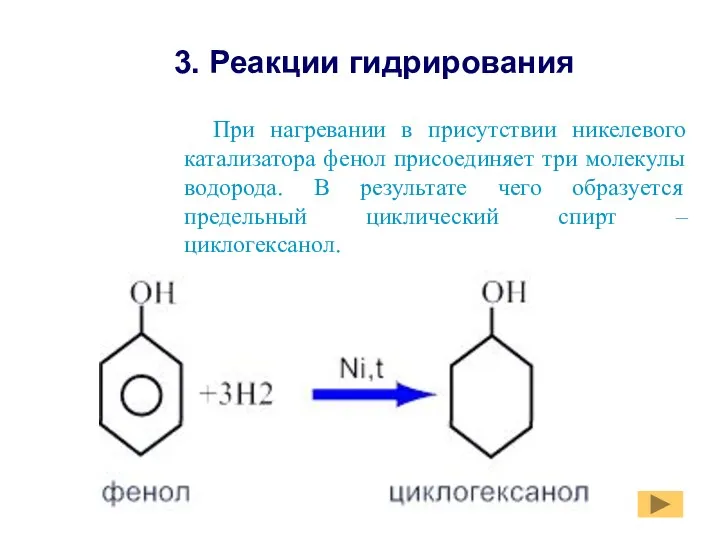
- 17. При нагревании в присутствии никелевого катализатора фенол присоединяет три молекулы водорода. В результате чего образуется предельный
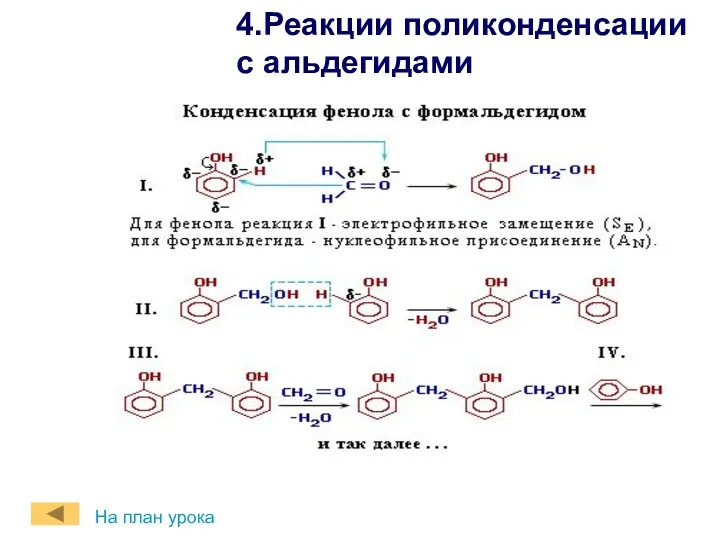
- 18. 4.Реакции поликонденсации с альдегидами На план урока
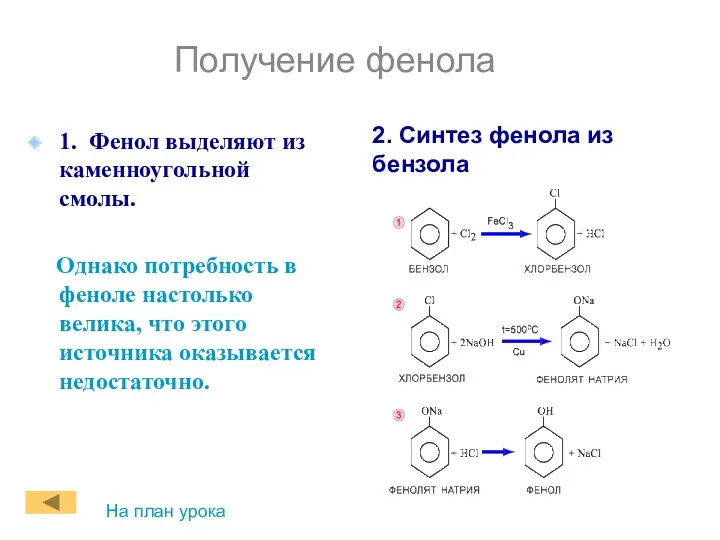
- 19. Получение фенола 1. Фенол выделяют из каменноугольной смолы. Однако потребность в феноле настолько велика, что этого
- 21. Скачать презентацию



 Минерал турмалин
Минерал турмалин Пластмассы: свойства, требования, перспективы развития. Виды конструкций из пластмасс
Пластмассы: свойства, требования, перспективы развития. Виды конструкций из пластмасс Лекарственные средства, относящиеся к производным пиридина : производные никотиновой и изоникотиновой кислоты
Лекарственные средства, относящиеся к производным пиридина : производные никотиновой и изоникотиновой кислоты Искусственные полимеры. 10 класс
Искусственные полимеры. 10 класс Теория химического строения органических соединений
Теория химического строения органических соединений Роль побутової хімії у житті
Роль побутової хімії у житті Методы чтения последовательностей нуклеиновых кислот. Секвенирование геномов древних людей
Методы чтения последовательностей нуклеиновых кислот. Секвенирование геномов древних людей альдегиды, свойства, получение
альдегиды, свойства, получение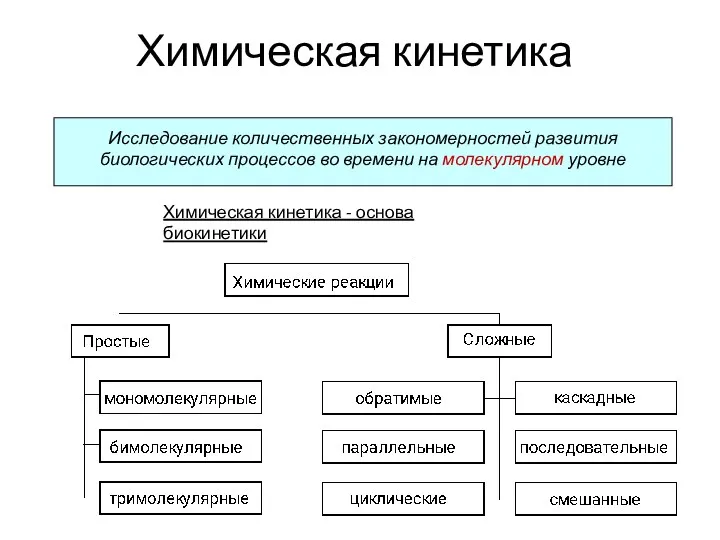 Химическая кинетика
Химическая кинетика Техника безопасности для учащихся в кабинете химии
Техника безопасности для учащихся в кабинете химии Theories of acids and bases. Ionic equilibria in electrolyte solutions. Buffer solutions (topic 3.4)
Theories of acids and bases. Ionic equilibria in electrolyte solutions. Buffer solutions (topic 3.4) Химические и физические свойства воды
Химические и физические свойства воды Окислительно-восстановительные реакции. Готовимся к ЕГЭ
Окислительно-восстановительные реакции. Готовимся к ЕГЭ Ферменты в биотехнологии
Ферменты в биотехнологии Губна помада та ії призначення
Губна помада та ії призначення Анализ двойных диаграмм. Лабораторная работа
Анализ двойных диаграмм. Лабораторная работа Общая характеристика металлов
Общая характеристика металлов Азот и его соединения
Азот и его соединения Обобщение по типам химических реакций
Обобщение по типам химических реакций The production of stable isotopes
The production of stable isotopes Хімічні властивості насичених одноатомних спиртів. Одержання етанолу
Хімічні властивості насичених одноатомних спиртів. Одержання етанолу Protein Chemistry
Protein Chemistry Силикаты. Слюды. Тальк. Фосфаты. Апатит. Крокоит
Силикаты. Слюды. Тальк. Фосфаты. Апатит. Крокоит Хинолин және хинуклидин, 4- жағдайда алмасқан хинолин туындыларының дәрілік заттарын талдау
Хинолин және хинуклидин, 4- жағдайда алмасқан хинолин туындыларының дәрілік заттарын талдау Выращивание кристаллов в домашних условиях
Выращивание кристаллов в домашних условиях Лекция 1 эквивалент 2
Лекция 1 эквивалент 2 Теплові прояви механічної, електричної та хімічної енергії
Теплові прояви механічної, електричної та хімічної енергії Элементы V группы главной подгруппы. Азот. Фосфор. (Лекция 13)
Элементы V группы главной подгруппы. Азот. Фосфор. (Лекция 13)