Содержание
- 2. Составьте электронные формулы атома фосфора. Определите возможные степени окисления химического элемента.
- 3. Возможные степени окисления фосфора
- 5. Физические свойства фосфора АЛЛОТРОПНЫЕ МОДИФИКАЦИИ ФОСФОРА: Белый фосфор Р4 -молекулярная решетка ЯД !!! 2.Красный фосфор Рп
- 6. Аллотропные модификации фосфора БЕЛЫЙ ФОСФОР КРАСНЫЙ ФОСФОР ЧЕРНЫЙ ФОСФОР
- 7. Получение фосфора Метод Веллера: Ca3(PO4)2 + 5C + 3SiO2 → 2P↑ + 5CO ↑ + 3CaSiO3.
- 8. Химические свойства фосфора 1) Фосфор легко окисляется кислородом: 4P + 5O2 → 2P2O5, 4P + 3O2
- 9. Химические свойства фосфора Взаимодействует со многими простыми веществами — галогенами, серой, некоторыми металлами, проявляя окислительные и
- 10. Химические свойства фосфора 4) Взаимодействует с водой, при этом диспропорционирует ( 700-800°C, кат.Pt? Cu): 4Р +
- 11. Соединения фосфора Фосфиды- соединения фосфора с металлами ( Ca3P2) Фосфин -соединение с водородом( РН3). Ядовитый бесцветный
- 12. Р2О5- кислотный оксид Взаимодействует: 1) с водой, образуя при этом различные кислоты Р2О5 + Н2О =
- 13. Р2О5- водоотнимающий реагент Фосфорный ангидрид отнимает у других веществ не только гигроскопическую влагу, но и химически
- 14. Р2О5- кислотный оксид Р2О5 H₃PO₄ HPO3 H4P2O7 Пирофосфорная кислота Метафосфорная кислота Ортофосфорная кислота +5 +5 +5
- 15. Физические свойства ортофосфорной кислоты При обычной температуре безводная Н3РO4 представляет собой прозрачное кристаллическое вещество, очень гигроскопичное
- 16. Исходным сырьем для промышленного получения Н3РO4 служит природный фосфат Са3(РO4)2: I. Са3(РO4)2 → Р → Р2O5
- 17. Химические свойства ортофосфорной кислоты Н3РО4 Металлы до Н Основные и амфотерные оксиды Основания Соли Изменяет окраску
- 18. Ортофосфорная кислота и её свойства 1. 2. 3. дигидрофосфат -ион гидрофосфат -ион фосфат -ион Диссоциация ортофосфорной
- 19. Качественная реакция на фосфат - ионы K3PO4+3AgNO3=Ag3PO4↓+3KNO3 при этом выпадает жёлтый осадок нитрата серебра
- 20. Соли ортофосфорной кислоты Н3РO4 как 3-основная кислота образует 3 типа солей, которые имеют большое практическое значение.
- 21. Р Фосфорная кислота Моющие средства Производство спичек Удобрения Ядохимикаты Взрывчатые вещества Пищевые добавки Медицина
- 22. Домашнее задание Н3РО4+Са= Н3РО4+СаО= Н3РО4+Са(ОН)2= Н3РО4+СаСО3= Допишите уравнения реакций
- 24. Скачать презентацию
 Алкины. Ацетиленовые углеводороды
Алкины. Ацетиленовые углеводороды Нефть и газ
Нефть и газ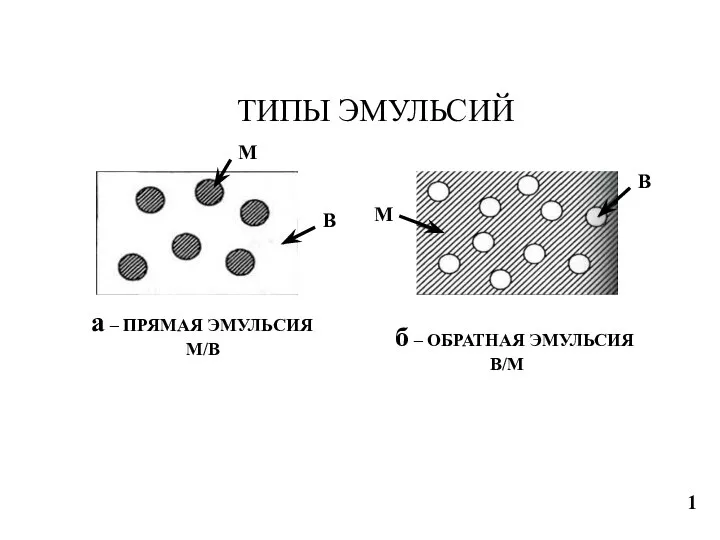 Типы эмульсий. Фракционный состав нефти. Типы нефти
Типы эмульсий. Фракционный состав нефти. Типы нефти Обмен нуклеопротеинов
Обмен нуклеопротеинов Инструментальный метод анализа
Инструментальный метод анализа Полиамиды. Классификация по методу получения
Полиамиды. Классификация по методу получения Хромотография, явления, атомы и молекулы. 8 класс
Хромотография, явления, атомы и молекулы. 8 класс Химическое производство
Химическое производство Водородные соединения неметаллов. Выходное тестирование
Водородные соединения неметаллов. Выходное тестирование Нефть - “Кормилица”. 10 класс
Нефть - “Кормилица”. 10 класс Характеристика щелочных металлов
Характеристика щелочных металлов Ароматические углеводороды (Арены)
Ароматические углеводороды (Арены) Растворы ВМС и их свойства
Растворы ВМС и их свойства Штучні і синтетичні волокна
Штучні і синтетичні волокна Кристаллическое строение металлов и сплавов
Кристаллическое строение металлов и сплавов Лекция 15. Аминокислоты
Лекция 15. Аминокислоты Органическая химия. Этапы развития органической химии
Органическая химия. Этапы развития органической химии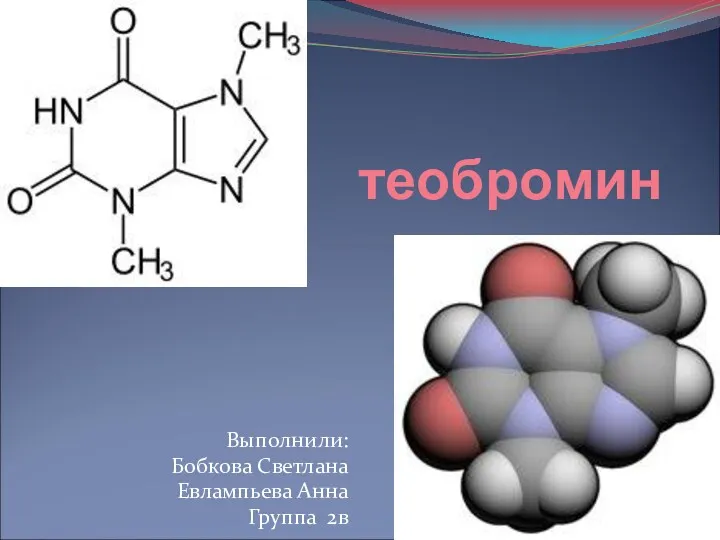 Теобромин
Теобромин Коррозия металлов. Часть 2. Лекция №11
Коррозия металлов. Часть 2. Лекция №11 Биохимия. Критерии оценки косметических средств. Лекция 4. Индустрия красоты
Биохимия. Критерии оценки косметических средств. Лекция 4. Индустрия красоты Хімічні формули речовин
Хімічні формули речовин Изотопный обмен
Изотопный обмен Основания, их классификация и свойства
Основания, их классификация и свойства Физико-химические основы дезодорации растительных масел
Физико-химические основы дезодорации растительных масел Количественный учет влияния заместителя на реакционную способность и его использование для интерпретации механизмов реакций
Количественный учет влияния заместителя на реакционную способность и его использование для интерпретации механизмов реакций Круговорот воды в природе
Круговорот воды в природе Коллигативные свойства растворов неэлектролитов
Коллигативные свойства растворов неэлектролитов Химическая связь
Химическая связь