Заключение
Свойства растворов, которые зависят от концентрации и практически не зависят от
природы растворенных веществ, называют коллигативными
Давление насыщенного пара любого чистого вещества при данной температуре постоянно и определяется природой этого вещества. Относительное понижение давления насыщенного пара растворителя над раствором равно молярной доле растворенного нелетучего вещества
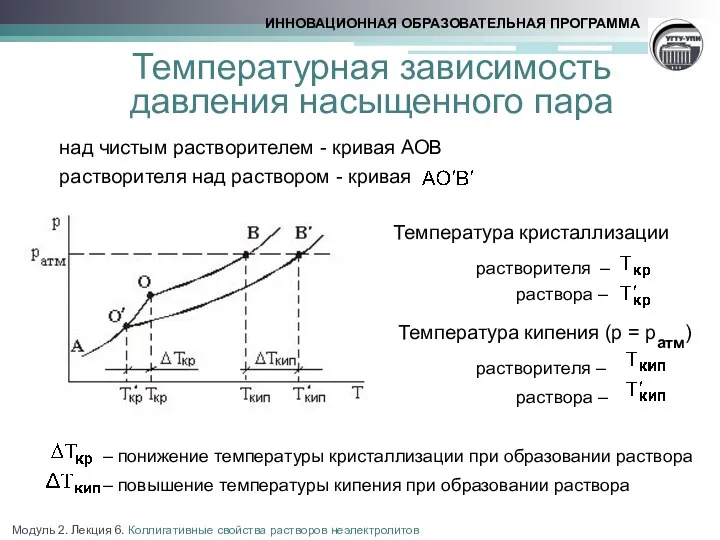
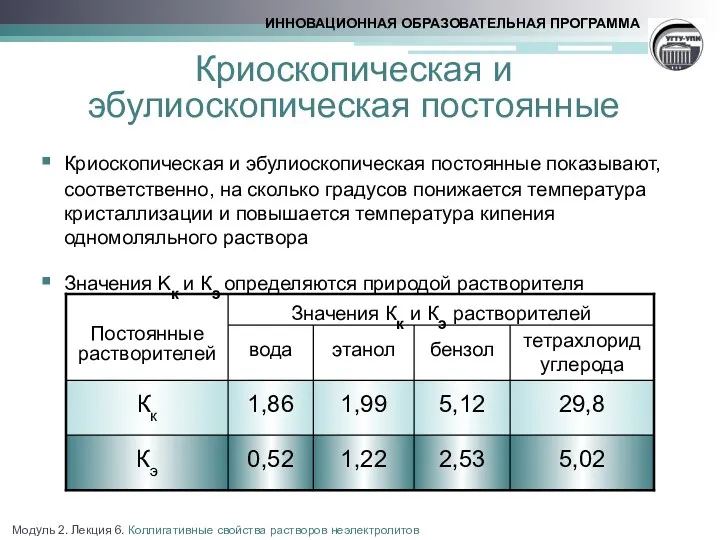
Температура кристаллизации раствора ниже температуры кристаллизации растворителя, а температура кипения раствора при ратм=const выше температуры кипения растворителя. Изменение температуры кристаллизации и кипения при образовании раствора пропорционально моляльной концентрации раствора
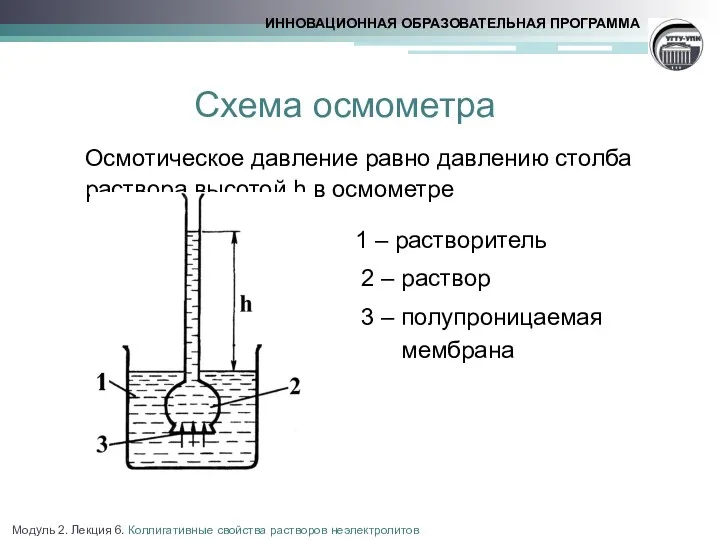
Самопроизвольный процесс перехода растворителя через полупроницаемую мембрану, разделяющую растворитель и раствор или два раствора, называют осмосом. Равновесное давление раствора, препятствующее диффузии растворителя - осмотическое давление
Осмотическое давление в растворе пропорционально молярной концентрации растворенного вещества
Модуль 2. Лекция 6. Коллигативные свойства растворов неэлектролитов











 Химический элемент радий
Химический элемент радий Основания. Классификация оснований
Основания. Классификация оснований Реакции электрофильного замещения в ароматическом ряду Se
Реакции электрофильного замещения в ароматическом ряду Se Главная подгруппа IV группы
Главная подгруппа IV группы Алкадиены (диеновые углеводороды)
Алкадиены (диеновые углеводороды) Свойства моторных топлив
Свойства моторных топлив Соли. Классификация. Физические и химические свойства. Получение и применение солей
Соли. Классификация. Физические и химические свойства. Получение и применение солей Химия и обмен углеводов. Функции углеводов
Химия и обмен углеводов. Функции углеводов Азотовмисні та елементоорганічні сполуки
Азотовмисні та елементоорганічні сполуки Физико-химия полимеров и их растворов
Физико-химия полимеров и их растворов Азотная кислота. К уроку химии для 9 класса
Азотная кислота. К уроку химии для 9 класса Тірі ағзада жүретін процесстер – физика-химиялық интерпретация
Тірі ағзада жүретін процесстер – физика-химиялық интерпретация Колоїдний захист
Колоїдний захист Алюминий и его соединения
Алюминий и его соединения Матеріальний баланс процесу горіння. Основні поняття матеріального балансу горіння
Матеріальний баланс процесу горіння. Основні поняття матеріального балансу горіння Содержание кислорода и углекислого газа в помещениях школы
Содержание кислорода и углекислого газа в помещениях школы Конструкционные функциональные волокнистые композиты. Углеродные волокна
Конструкционные функциональные волокнистые композиты. Углеродные волокна Основания. Состав, классификация, свойства, получение
Основания. Состав, классификация, свойства, получение Основные химические понятия
Основные химические понятия Интоксикации сельскохозяйственными ядохимикатами (пестицидами)
Интоксикации сельскохозяйственными ядохимикатами (пестицидами) Химическая кинетика
Химическая кинетика Классификация органических реакций
Классификация органических реакций Строение электронных оболочек атомов
Строение электронных оболочек атомов Алкены
Алкены Основные понятия и законы химии. Тема1
Основные понятия и законы химии. Тема1 Карбон қышқылдар, түрлері қасиеттері, түындылары. Лекция № 8. Гетерофункционалды қосылыстар. Лекция № 9
Карбон қышқылдар, түрлері қасиеттері, түындылары. Лекция № 8. Гетерофункционалды қосылыстар. Лекция № 9 Осадительное титрование. Меркуриметрия
Осадительное титрование. Меркуриметрия Общая характеристика неметаллов
Общая характеристика неметаллов