Содержание
- 2. Этапы развития органической химии: Стихийный – период развития до XIV века Алхимия – XVI – XVII
- 3. Середина XVIII в. – выделение органической химии в отдельную отрасль Вещества растительного и животного происхождения –
- 4. Органическая химия – раздел химии, изучающий соединения углерода, их структуру, свойства, методы синтеза. Органическими называют соединения
- 5. Ряд открытий, сокрушивших витализм: В 1822 г. Веллер показал, что неорганическое вещество – циановокислый аммоний при
- 6. Английский химик Э. Франкланд ввел в науку понятие о валентности Валентность – это способность атома присоединять
- 7. Классификация органических соединений по происхождению Органические соединения: а) Природные – это продукты жизнедеятельности живых организмов. б)
- 8. Органическая химия – раздел химии, изучающий структуру, свойства и методы синтеза углеводородов и их производных. Углеводороды
- 9. Выпишите формулы органических соединений: BaCO3 ; CH4 ; CO2 ; CH3OH ; H2CO3 ; HCl ;
- 10. Домашнее задание: 1. Опишите свойства и применение одного органического соединения: а) природного б) искусственного в)синтетического 2.
- 11. Теория строения органических Соединений А.М. Бутлерова
- 12. Основные положения теории строения химических соединений Атомы в молекулах соединяются в определенном порядке в соответствии с
- 13. б) Порядок соединения атомов углерода в молекулах может быть различным и зависит от вида ковалентной химической
- 14. 2. Свойства веществ зависят не только от их качественного и количественного состава, но и от строения
- 15. Виды изомерии: Структурная: изомерия углеродного скелета, изомерия положения, изомерия межклассовая Пространственная : цис- изомерия транс- изомерия
- 16. Структурная изомерия Структурная изомерия, при которой вещества различаются порядком связи атомов в молекулах: 1) Изомерия углеродного
- 17. 3) Межклассовая изомерия CH3-CH=CH-CH3 Бутен-2 в) изомерия положения функциональных групп
- 18. Пространственная изомерия Пространственная изомерия, при которой молекулы веществ отличаются не порядком связи атомов, а положением их
- 19. 3. Свойства веществ зависят от взаимного влияния атомов в молекулах. В уксусной кислоте в реакцию со
- 21. Скачать презентацию


















 Свойства топлив. Марки бензинов и их характеристики
Свойства топлив. Марки бензинов и их характеристики Определение окисляемости воды
Определение окисляемости воды Основные задачи и понятия химической метрологии
Основные задачи и понятия химической метрологии Удивительные свойства воды
Удивительные свойства воды Классификация химических элементов
Классификация химических элементов Классификация и свойства кислот
Классификация и свойства кислот Контроль качества пищевых товаров
Контроль качества пищевых товаров Кислород и оксиген
Кислород и оксиген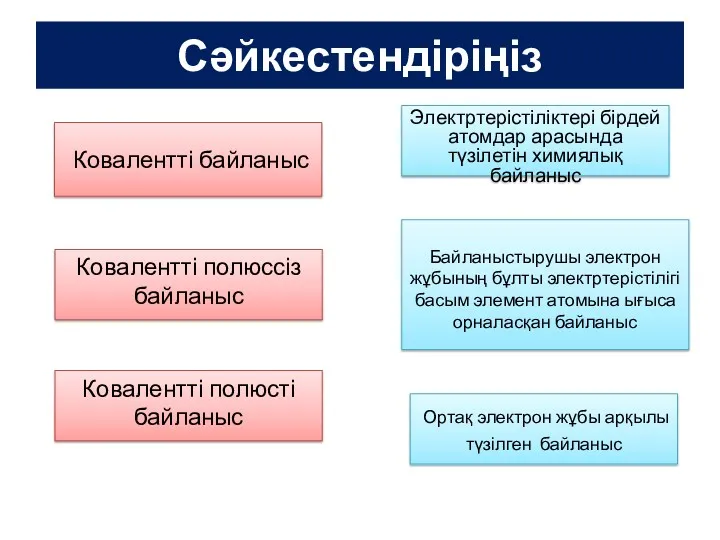 Иондық байланыс
Иондық байланыс Газовые смеси
Газовые смеси Алюминий и его соединения
Алюминий и его соединения Кислород. Химия – 8 класс
Кислород. Химия – 8 класс Углекислый газ СО2
Углекислый газ СО2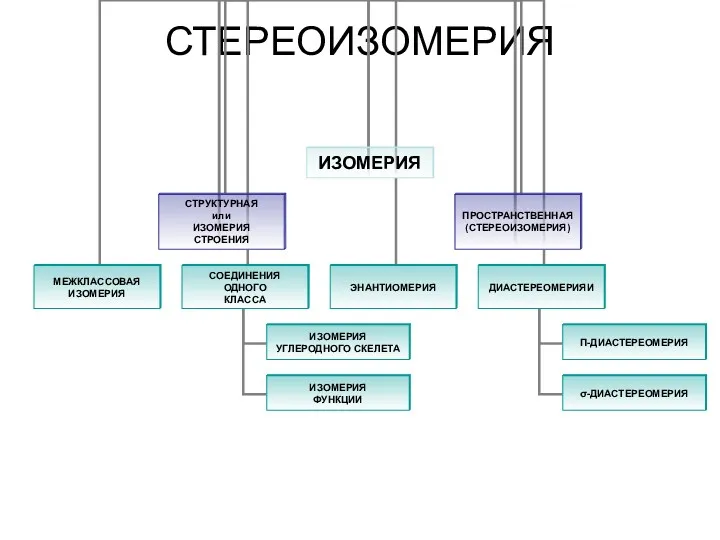 Стереоизомерия. Изомерия. Пространственная (стереоизомерия) углеродного скелета
Стереоизомерия. Изомерия. Пространственная (стереоизомерия) углеродного скелета 20230212_urok_ionnye_uravneniya
20230212_urok_ionnye_uravneniya Ароматические углеводороды (Арены)
Ароматические углеводороды (Арены) Спирти. 3агальна характеристика спиртів
Спирти. 3агальна характеристика спиртів Тотығу-тотықсыздану реакциялары
Тотығу-тотықсыздану реакциялары Растворы. Свойства растворов. (Тема 3)
Растворы. Свойства растворов. (Тема 3) Кондуктометрия и кондуктометрическое титрование
Кондуктометрия и кондуктометрическое титрование Гидролиз неорганических веществ (теоретический материал для подготовки к ЕГЭ)
Гидролиз неорганических веществ (теоретический материал для подготовки к ЕГЭ) Качественный анализ (часть 1)
Качественный анализ (часть 1) Нанопористые материалы
Нанопористые материалы Понятие о спиртах. 9 класс
Понятие о спиртах. 9 класс Щелочные металлы. Положение в ПСХЭ
Щелочные металлы. Положение в ПСХЭ Тайна великого открытия периодической таблицы
Тайна великого открытия периодической таблицы Разработка проектных решений по переводу паровых котлов электростанций в конденсационный режим с целью увеличения кпд котла
Разработка проектных решений по переводу паровых котлов электростанций в конденсационный режим с целью увеличения кпд котла Понятие биогенности химических элементов
Понятие биогенности химических элементов