Содержание
- 2. образовательные: – проверить глубину и прочность усвоения учащимися знаний по теме “Соединения химических элементов” – выявить
- 3. “Единственный путь, ведущий к знанию, - это деятельность” (Б. Шоу. ) Девиз урока:
- 4. Цель для обучающихся: -упражнения в составлении формул по названиям и названий веществ по формулам. -классификация сложных
- 5. Классификация веществ вещества простые сложные металлы неметаллы кислоты оксиды соли основания
- 6. Распределение веществ по классам Металл Li Неметалл P Оксид P2O5; CaO; Li2O Основание LiOH Кислота H3PO4;
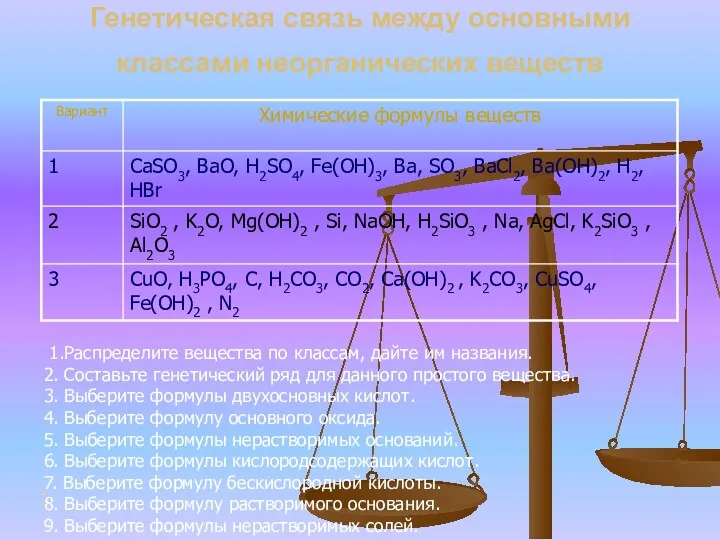
- 7. Генетическая связь между основными классами неорганических веществ 1.Распределите вещества по классам, дайте им названия. 2. Составьте
- 8. Распределение веществ по классам Оксиды BaO –оксид бария SO3 – оксид серы (VI) SiO2- оксид кремния
- 9. Генетический ряд данного простого вещества Ba BaO Ba(OH)2 BaCl2 Si SiO2 H2SiO3 K2SiO3 C CO2 H2CO3
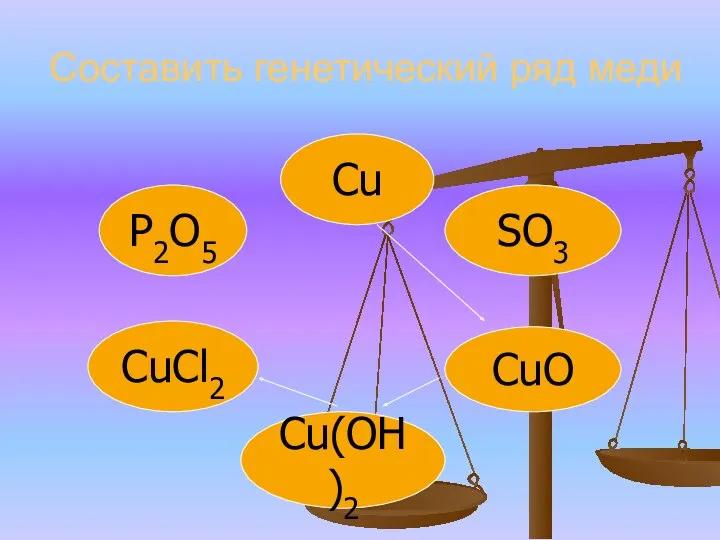
- 10. Составить генетический ряд меди CuCl2 Сu CuO Cu(OH)2 SO3 P2O5
- 11. Выделяем признаки, которые характеризуют генетический ряд: Вещества разных классов; Разные вещества образованы одним химическим элементом, т.е.
- 12. Вещества 1)H2SO4 2) MgCl2 3)Ca(OH)2 4) CuSO4 5) H2O 6) HCl 7)Fe2O3 8) NaOH 9) Al(NO3)3
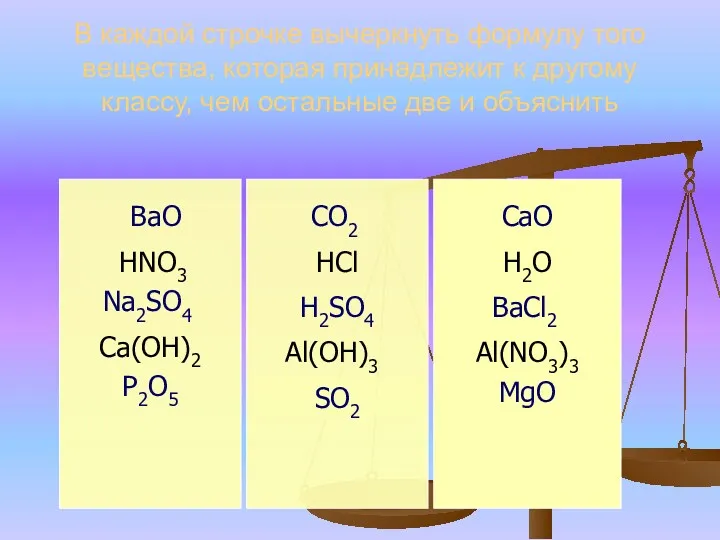
- 13. В каждой строчке вычеркнуть формулу того вещества, которая принадлежит к другому классу, чем остальные две и
- 15. Скачать презентацию









 Вещества и их свойства
Вещества и их свойства Элементтер-органогендер. Көміртек – органикалық қосылыстардың негізін құраушы. Тірі және өлі табиғат арасындағы шекара
Элементтер-органогендер. Көміртек – органикалық қосылыстардың негізін құраушы. Тірі және өлі табиғат арасындағы шекара Типы химических реакций в органической химии
Типы химических реакций в органической химии Хімічні явища в побуті
Хімічні явища в побуті Обзор электродных процессов
Обзор электродных процессов Аммиак
Аммиак Распределение электронов в атомах. 8 класс
Распределение электронов в атомах. 8 класс Синтетичні високомолекулярні речовини і полімерні матеріали на їх основі. Лекція №27
Синтетичні високомолекулярні речовини і полімерні матеріали на їх основі. Лекція №27 Агрегатные состояния вещества с точки зрения атомно-молекулярных представлений
Агрегатные состояния вещества с точки зрения атомно-молекулярных представлений Металдар
Металдар Карбоновые кислоты
Карбоновые кислоты Химическая кинетика
Химическая кинетика Гидрирование альдегидов и кетонов
Гидрирование альдегидов и кетонов Mechanistic insights into the aminolysis of 3,4-epoxysulfolane
Mechanistic insights into the aminolysis of 3,4-epoxysulfolane Йони. Йонний зв’язок, його утворення
Йони. Йонний зв’язок, його утворення 6-я группа элементов. 9 класс
6-я группа элементов. 9 класс Оксиды. Классификация. Химические и физические свойства (8 класс)
Оксиды. Классификация. Химические и физические свойства (8 класс) Кислородосодержащие соединения - спирты
Кислородосодержащие соединения - спирты Классификация химических реакций. 8 класс
Классификация химических реакций. 8 класс Водород и его свойства
Водород и его свойства Аминокислоты. Белки
Аминокислоты. Белки Основания
Основания Фазовые превращения в стали при охлаждении
Фазовые превращения в стали при охлаждении Химическая связь. Взаимное влияние атомов в молекуле. Классификация реакций и реагентов. Структура и функции биолекул
Химическая связь. Взаимное влияние атомов в молекуле. Классификация реакций и реагентов. Структура и функции биолекул Приготування розчинів
Приготування розчинів Электролитическая диссоциация. 9 класс
Электролитическая диссоциация. 9 класс Полимеры и их использование
Полимеры и их использование Алкадиены: гомологический ряд, общая формула, номенклатура. Сопряжённые, изолированные, кумулированные
Алкадиены: гомологический ряд, общая формула, номенклатура. Сопряжённые, изолированные, кумулированные