Слайд 2
Тема урока
Кислородосодержащие соединения- спирты.
R−O−H.
Слайд 3

Слайд 4

Слайд 5
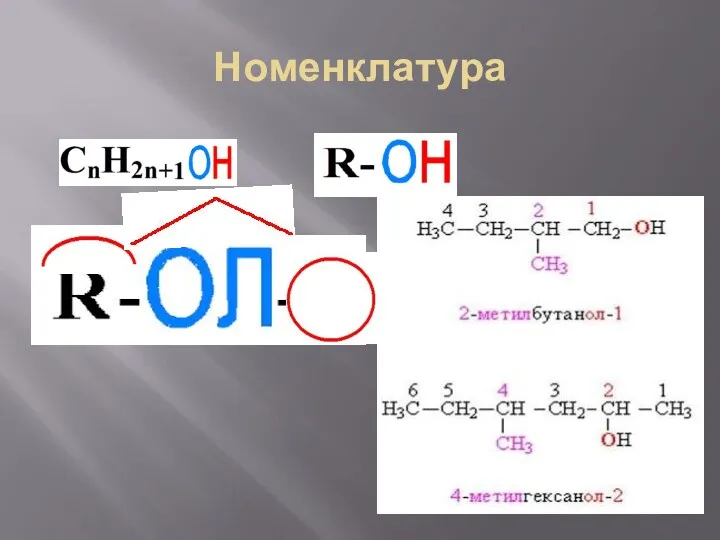
Слайд 6

Физические свойства
Температура кипения спиртов выше температуры кипения соответствующих углеводородов.
Среди спиртов
нет газов.
С увеличением относительной молекулярной массы спиртов повышаются их температуры кипения, уменьшается растворимость в воде.
Слайд 7
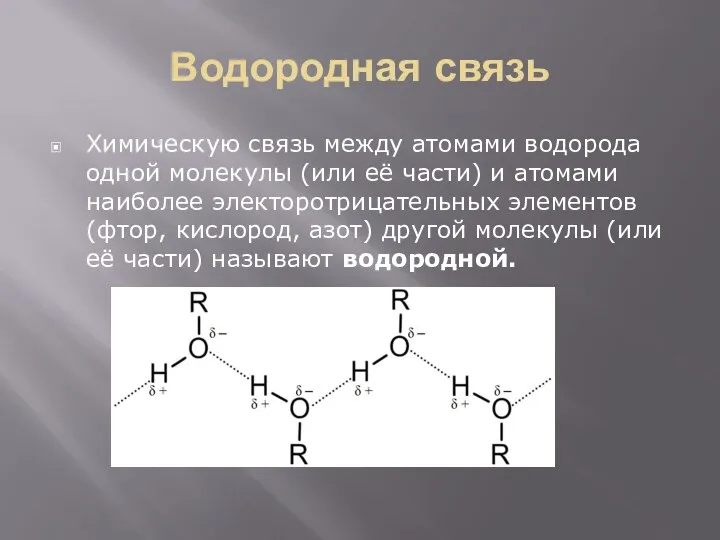
Водородная связь
Химическую связь между атомами водорода одной молекулы (или её части)
и атомами наиболее электоротрицательных элементов (фтор, кислород, азот) другой молекулы (или её части) называют водородной.
Слайд 8

Получение спиртов
В промышленности
1.Гидратация
СН2= СН2 + Н2О= 2С2Н5ОН
2.Брожение
С6Н12О6 =2С2Н5ОН + 2СО2
В лаборатории
С2Н5Br + NaOH=
С2Н5ОH +NaBr
Слайд 9

Химические свойства
Взаимодействие со щелочными и щелочно-земельными металлами
2 R – OH +
2 Na 2 R – O-Na + H2
алкоголятNa
Реакция межмолекулярной дегидратации:
H2SO4 (к), t<140
R-OH + HO-R H2O + R- O- R
Простой эфир
Реакция внутримолекулярной дегидратации:
H2SO4 (к), t<140
R - CH - CH - R′ R - CH = CH - R′
OH H -H2O Алкен
Слайд 10

Реакция этерификации(от лат. ester – эфир) – образование сложных эфиров
Слайд 11
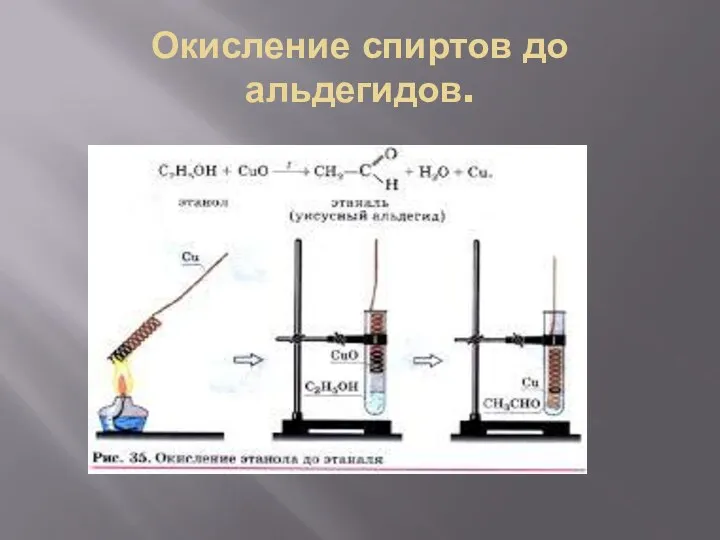
Окисление спиртов до альдегидов.
Слайд 12

Качественная реакция на многоатомные спирты
Реакцией на многоатомные спирты является их
взаимодействие со свежеполученным осадком гидроксида меди (II), который растворяется с образованием яркого сине-фиолетового раствора
Слайд 13

Закрепление
Дать название следующему веществу:
CH2—CH—CH2—CH2—OH
I
CH3
Назовите функциональную группу спиртов.
Перечислите
продукты реакции горения спиртов.
Укажите конечный продукт
2C2H5OH+ Na → ……. + H2↑
При помощи какой реакции можно определить наличие многоатомного спирта в пробирке.
Слайд 14

Проверь себя.
3-метилбутанол-1
Гидроксильная (-ОН)
Углекислый газ и вода
Этилат натрия C2H5ONa
Реакция со свежим гидроксидом
меди,
появится ярко-синее окрашивание.
МОЛОДЦЫ!













 Амины. Анилин
Амины. Анилин Полимеры (10 класс)
Полимеры (10 класс) Химический элемент цинк
Химический элемент цинк Кислород
Кислород Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Кислородсодержащие органические соединения. 9 класс
Кислородсодержащие органические соединения. 9 класс Основания. Состав, классификация, свойства, получение
Основания. Состав, классификация, свойства, получение Теория электролитической диссоциации
Теория электролитической диссоциации Азот. Строение атома и молекулы
Азот. Строение атома и молекулы Алкены. Непредельные углеводороды ряда этилена
Алкены. Непредельные углеводороды ряда этилена Електролітична дисоціація. Електроліти та неелектроліти. Урок хімії в 9 класі
Електролітична дисоціація. Електроліти та неелектроліти. Урок хімії в 9 класі Карбоновые кислоты и их функциональные производные
Карбоновые кислоты и их функциональные производные Study of the properties of halogens and the determination of halide ions in aqueous solution
Study of the properties of halogens and the determination of halide ions in aqueous solution Полимеры
Полимеры Кислотно-основное титрование. Алкалиметрия
Кислотно-основное титрование. Алкалиметрия Алюминий и его соединения
Алюминий и его соединения Сера и ее важнейшие соединения
Сера и ее важнейшие соединения Установка производства олефинов для синтеза линейных алкилбензолов
Установка производства олефинов для синтеза линейных алкилбензолов Алюминий и его соединения
Алюминий и его соединения Свойства неорганических веществ. (Задание 37. ЕГЭ по химии)
Свойства неорганических веществ. (Задание 37. ЕГЭ по химии) Основи. Загальна формула основ
Основи. Загальна формула основ Природный и попутный нефтяной газы
Природный и попутный нефтяной газы Гидрокси және оксоқышқылдар биологиялық рөлі
Гидрокси және оксоқышқылдар биологиялық рөлі Искусственные полимеры
Искусственные полимеры Протекание ОВР зависит от рН среды
Протекание ОВР зависит от рН среды Природный и попутный нефтяные газы
Природный и попутный нефтяные газы 20230330_metodicheskaya_razrabotka_ovr_v_organicheskoy_himii
20230330_metodicheskaya_razrabotka_ovr_v_organicheskoy_himii Галогены. Положение галогенов в ПСХЭ
Галогены. Положение галогенов в ПСХЭ