Химическая связь. Взаимное влияние атомов в молекуле. Классификация реакций и реагентов. Структура и функции биолекул презентация
Содержание
- 2. План 1. Типы химических связей 2. Сопряжение. Сопряженные системы. Ароматичность 3. Взаимное влияние атомов в молекуле.
- 3. 1. Типы химических связей
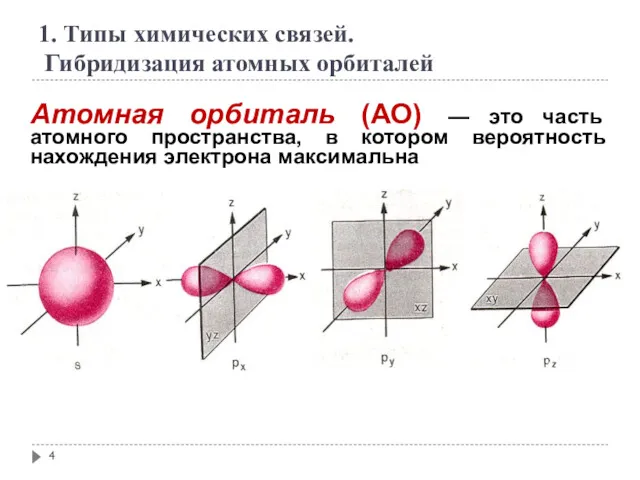
- 4. Атомная орбиталь (АО) — это часть атомного пространства, в котором вероятность нахождения электрона максимальна 1. Типы
- 5. Правило Хунда (Гунда): Орбитали данного подуровня заполняются сначала по одному электрону Правило Паули: на орбитали могут
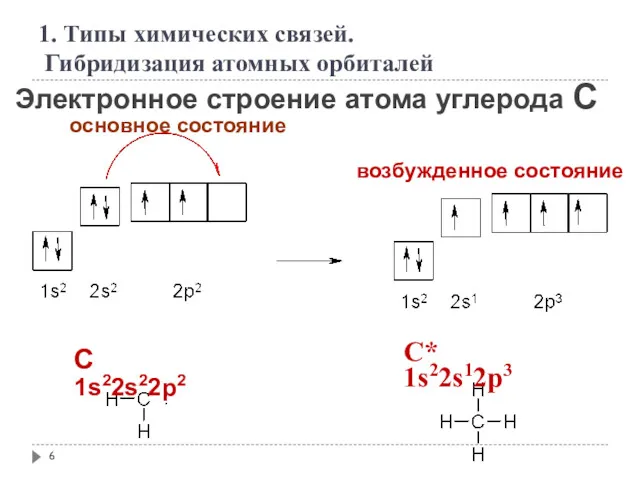
- 6. Электронное строение атома углерода С основное состояние возбужденное состояние C 1s22s22p2 C* 1s22s12p3 1. Типы химических
- 7. . Гибридизация − перестройка близких по энергии орбиталей, в ходе которой образуются орбитали с одинаковой формой
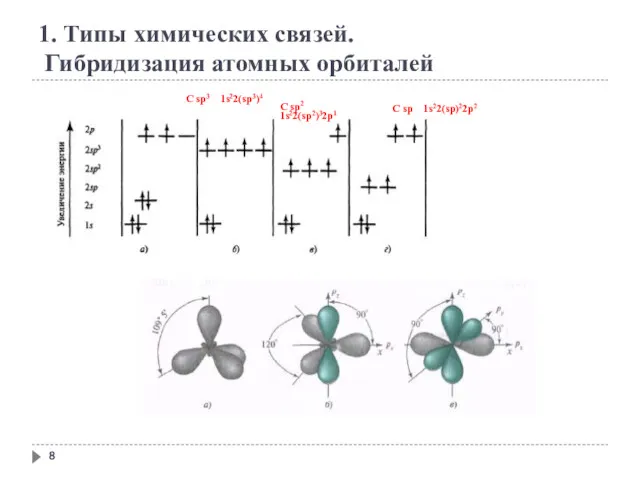
- 8. C sp3 1s22(sp3)4 C sp2 1s22(sp2)32p1 C sp 1s22(sp)22p2 1. Типы химических связей. Гибридизация атомных орбиталей
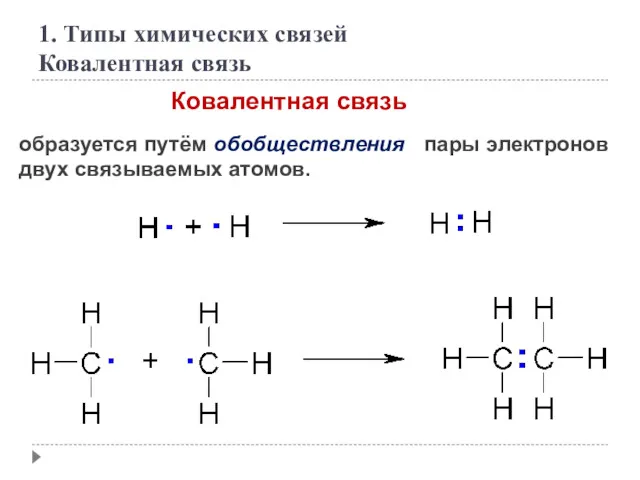
- 9. Ковалентная связь образуется путём обобществления пары электронов двух связываемых атомов. 1. Типы химических связей Ковалентная связь
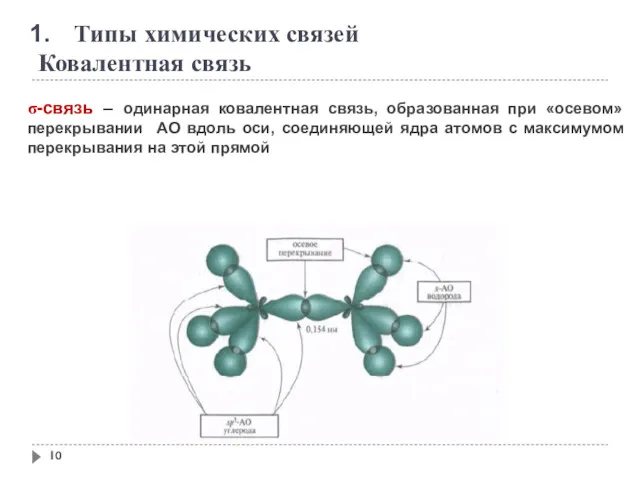
- 10. Типы химических связей Ковалентная связь σ-связь – одинарная ковалентная связь, образованная при «осевом» перекрывании АО вдоль
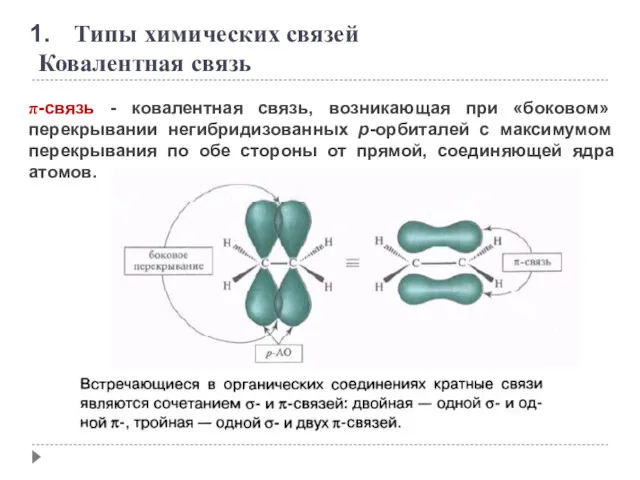
- 11. π-связь - ковалентная связь, возникающая при «боковом» перекрывании негибридизованных p-орбиталей с максимумом перекрывания по обе стороны
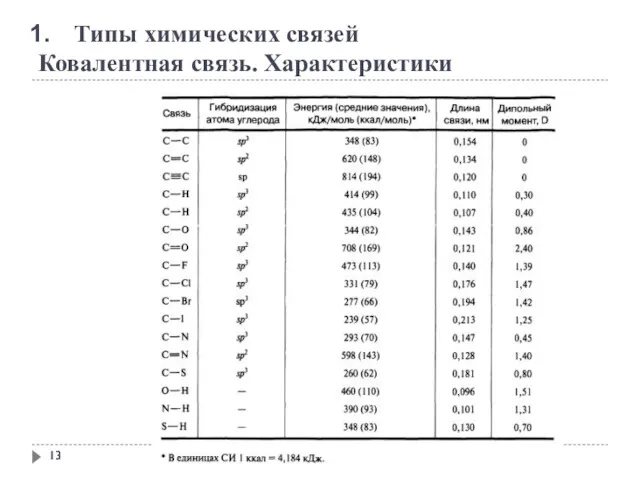
- 12. Типы химических связей Ковалентная связь. Характеристики
- 13. Типы химических связей Ковалентная связь. Характеристики
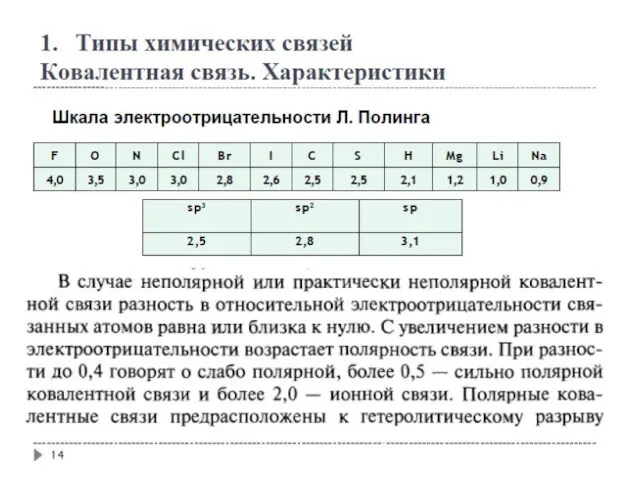
- 15. Типы химических связей Ковалентная связь. Характеристики
- 16. Типы химических связей Ковалентная связь. Характеристики
- 17. Типы химических связей Ковалентная связь. Механизмы образования обменный механизм донорно-акцепторная связь носители неподеленных пар
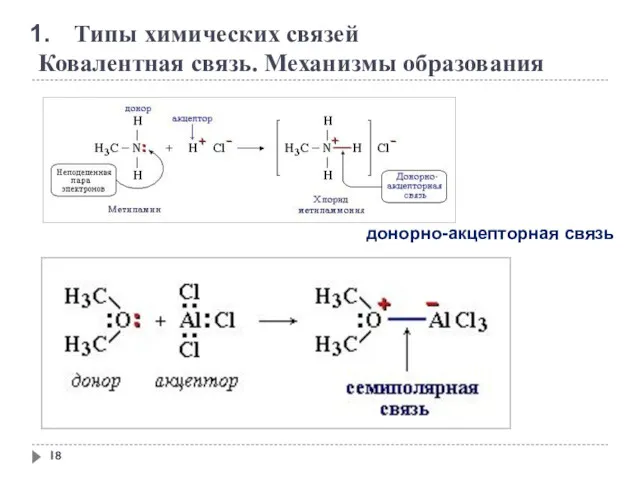
- 18. Типы химических связей Ковалентная связь. Механизмы образования донорно-акцепторная связь
- 19. Типы химических связей Ковалентная связь. Водородная связь
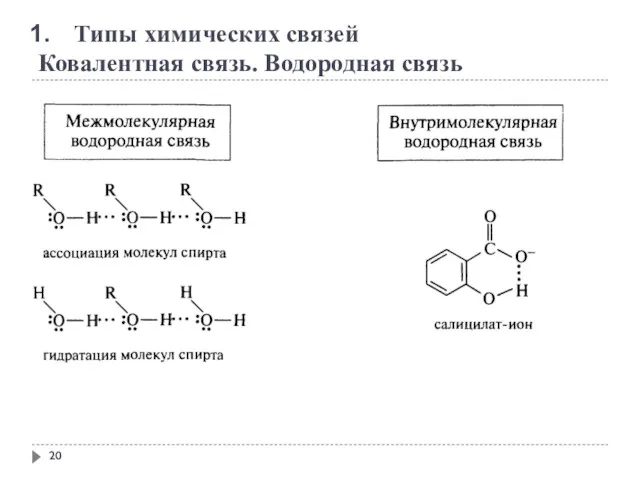
- 20. Типы химических связей Ковалентная связь. Водородная связь
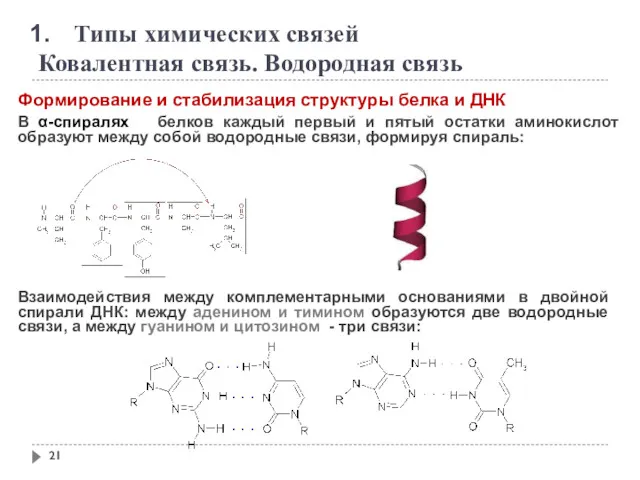
- 21. Типы химических связей Ковалентная связь. Водородная связь Формирование и стабилизация структуры белка и ДНК В α-спиралях
- 22. 1. Типы химических связей 1.Определите тип гибридизации атомов углерода, кислорода, азота в соединениях А, Б, В.
- 23. 2. Сопряжение. Сопряженные системы
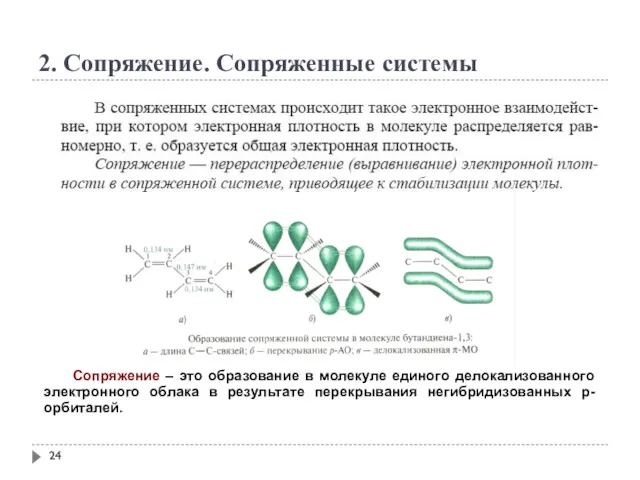
- 24. 2. Сопряжение. Сопряженные системы Сопряжение – это образование в молекуле единого делокализованного электронного облака в результате
- 25. 2. Сопряжение. Сопряженные системы. Ароматичность В результате сопряжения выделяется энергия, внутренняя энергия уменьшается, и молекула становится
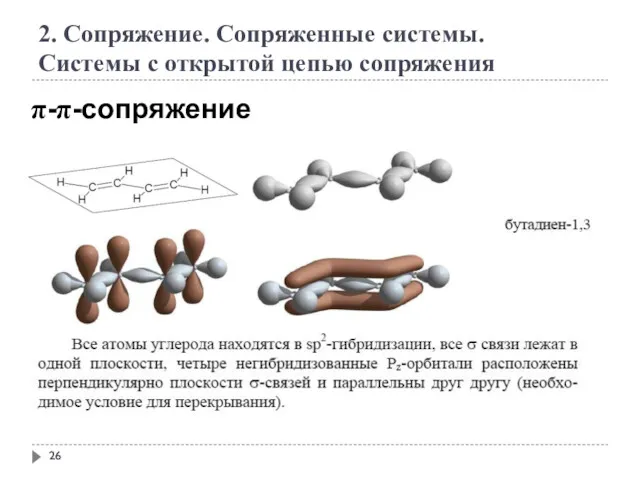
- 26. 2. Сопряжение. Сопряженные системы. Системы с открытой цепью сопряжения π-π-сопряжение
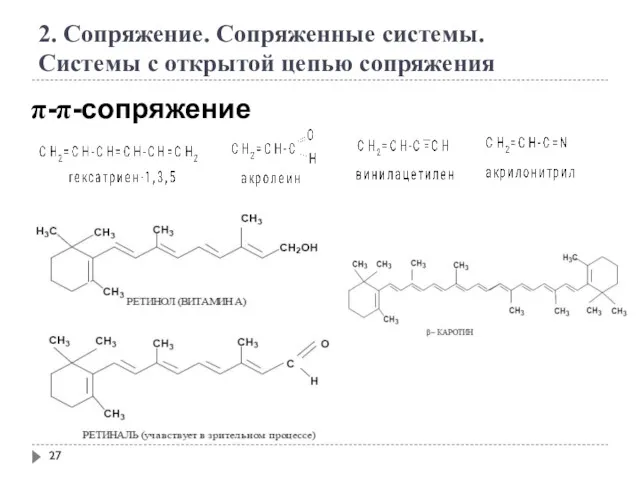
- 27. 2. Сопряжение. Сопряженные системы. Системы с открытой цепью сопряжения π-π-сопряжение
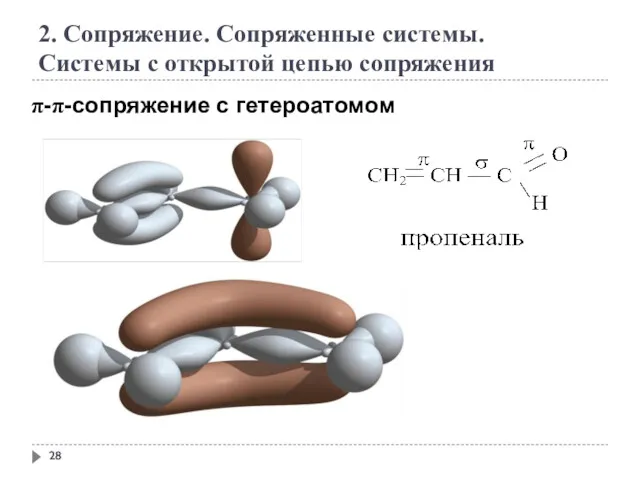
- 28. 2. Сопряжение. Сопряженные системы. Системы с открытой цепью сопряжения π-π-сопряжение с гетероатомом
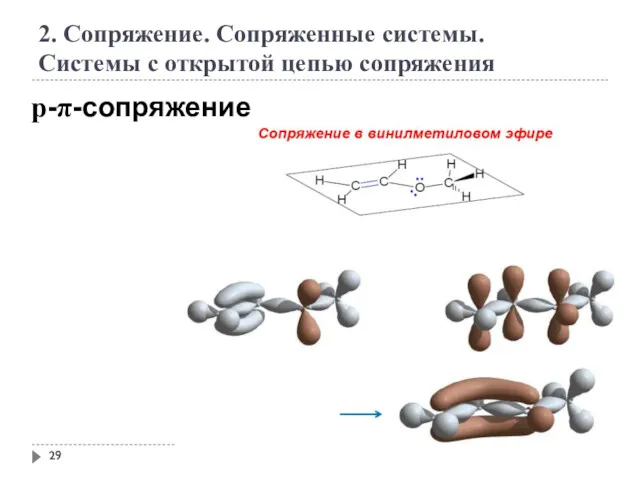
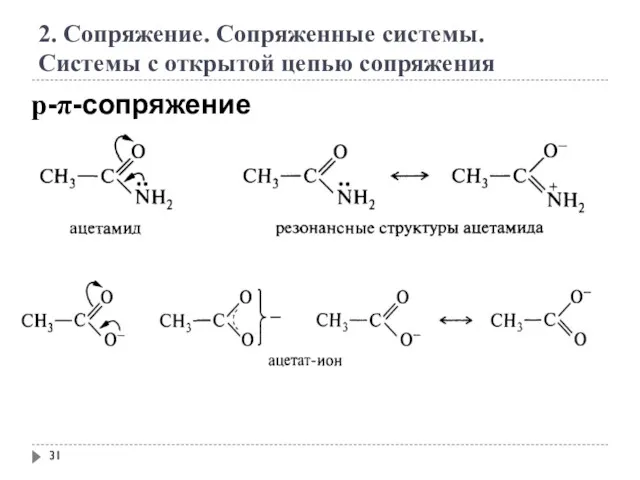
- 29. 2. Сопряжение. Сопряженные системы. Системы с открытой цепью сопряжения р-π-сопряжение
- 30. 2. Сопряжение. Сопряженные системы. Системы с открытой цепью сопряжения р-π-сопряжение
- 31. 2. Сопряжение. Сопряженные системы. Системы с открытой цепью сопряжения р-π-сопряжение
- 33. 2. Сопряжение. Сопряженные системы. Ароматичность Ароматичность — особое свойство некоторых химических соединений, благодаря которому сопряженное кольцо
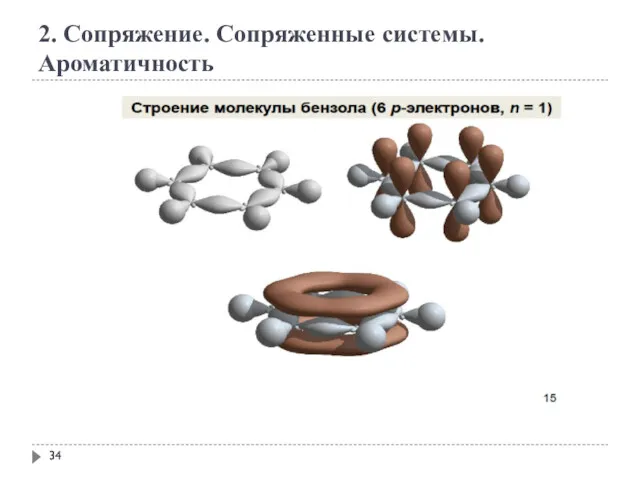
- 34. 2. Сопряжение. Сопряженные системы. Ароматичность
- 35. 2. Сопряжение. Сопряженные системы. Ароматичность
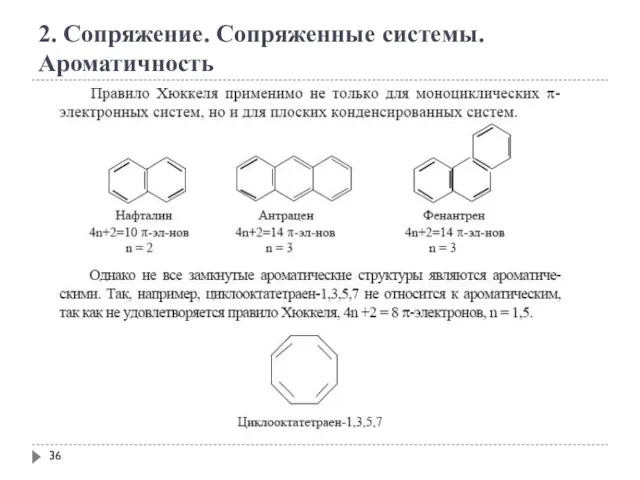
- 36. 2. Сопряжение. Сопряженные системы. Ароматичность
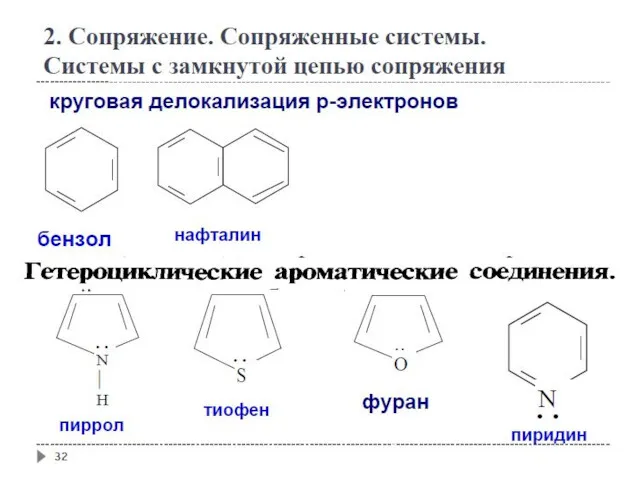
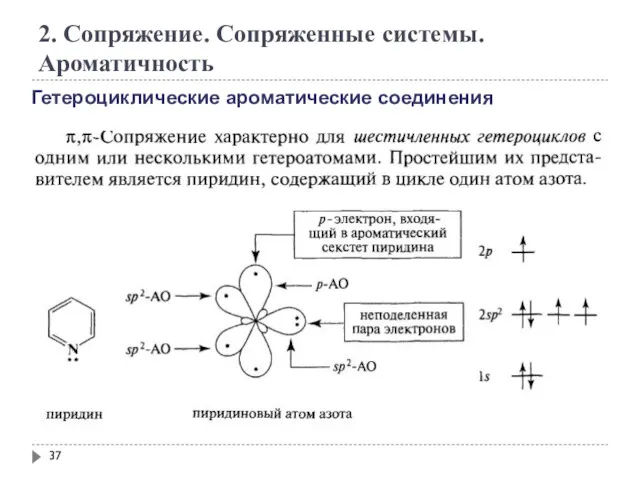
- 37. 2. Сопряжение. Сопряженные системы. Ароматичность Гетероциклические ароматические соединения
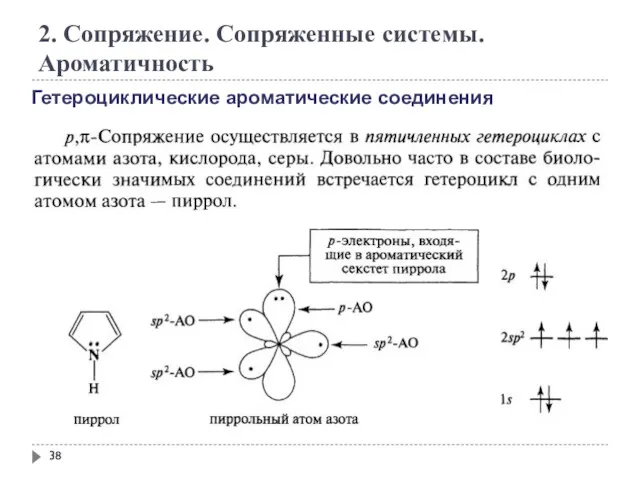
- 38. 2. Сопряжение. Сопряженные системы. Ароматичность Гетероциклические ароматические соединения
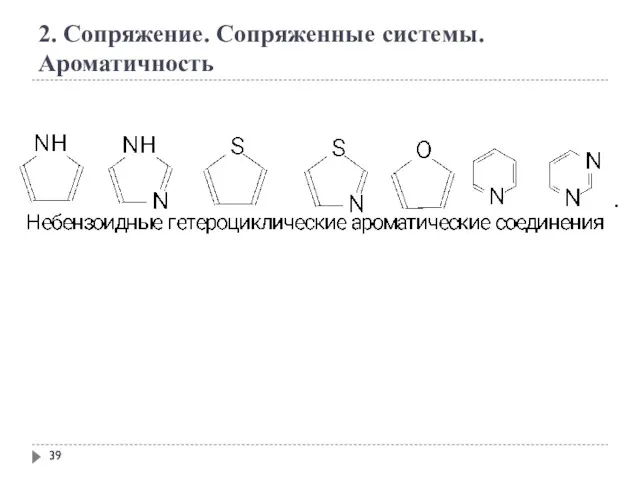
- 39. 2. Сопряжение. Сопряженные системы. Ароматичность
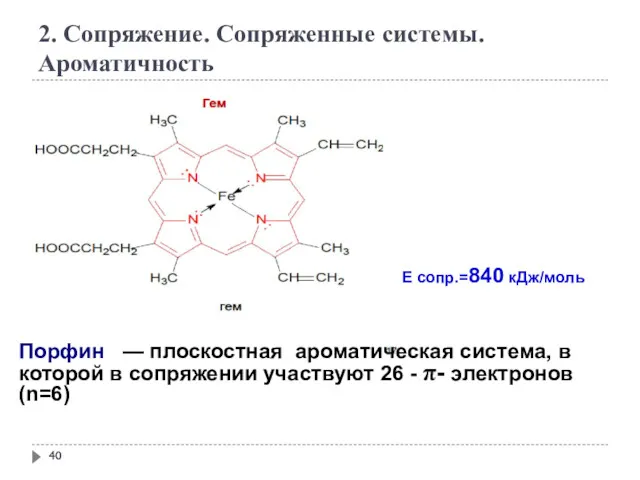
- 40. 2. Сопряжение. Сопряженные системы. Ароматичность Порфин — плоскостная ароматическая система, в которой в сопряжении участвуют 26
- 41. 2. Сопряжение. Сопряженные системы. Ароматичность Для проверки усвоения раздела . 1.Укажите число π -электронов в сопряженной
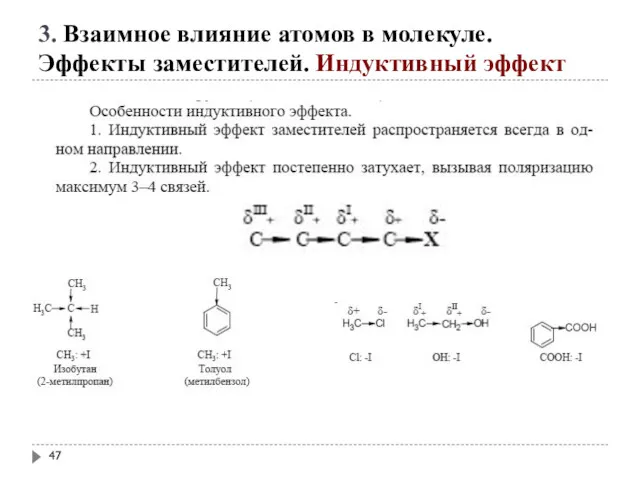
- 42. 3. Взаимное влияние атомов в молекуле. Эффекты заместителей. Индуктивный эффект
- 43. 3. Взаимное влияние атомов в молекуле. Эффекты заместителей. Индуктивный эффект Электроноакцепторные заместители X, т.е. атом или
- 44. 3. Взаимное влияние атомов в молекуле. Эффекты заместителей. Индуктивный эффект
- 45. 3. Взаимное влияние атомов в молекуле. Эффекты заместителей. Индуктивный эффект
- 46. 3. Взаимное влияние атомов в молекуле. Эффекты заместителей. Индуктивный эффект –I эффект проявляют 1. заместители, которые
- 47. 3. Взаимное влияние атомов в молекуле. Эффекты заместителей. Индуктивный эффект
- 48. 3. Взаимное влияние атомов в молекуле. Эффекты заместителей. Индуктивный эффект
- 49. 3. Взаимное влияние атомов в молекуле. Эффекты заместителей. Мезомерный эффект
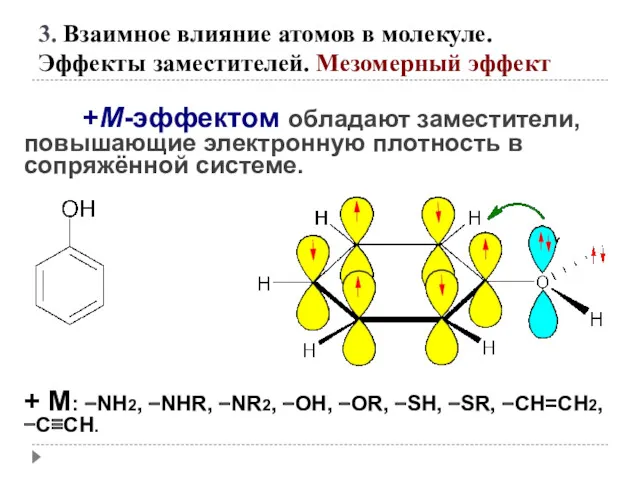
- 50. +М-эффектом обладают заместители, повышающие электронную плотность в сопряжённой системе. + М: −NH2, −NHR, −NR2, −OH, −OR,
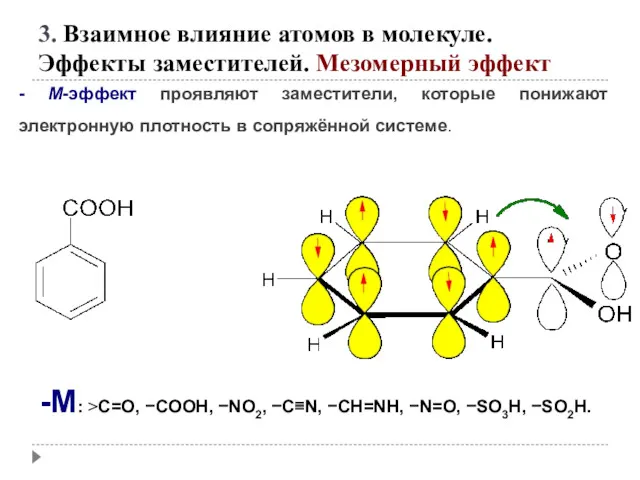
- 51. - М-эффект проявляют заместители, которые понижают электронную плотность в сопряжённой системе. -M: >C=O, −COOH, −NO2, −C≡N,
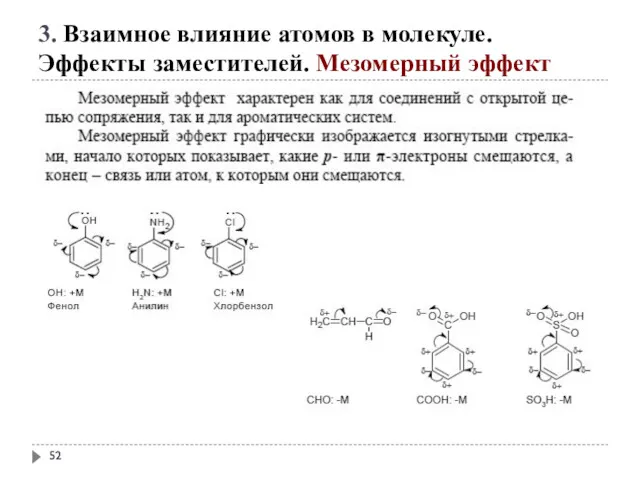
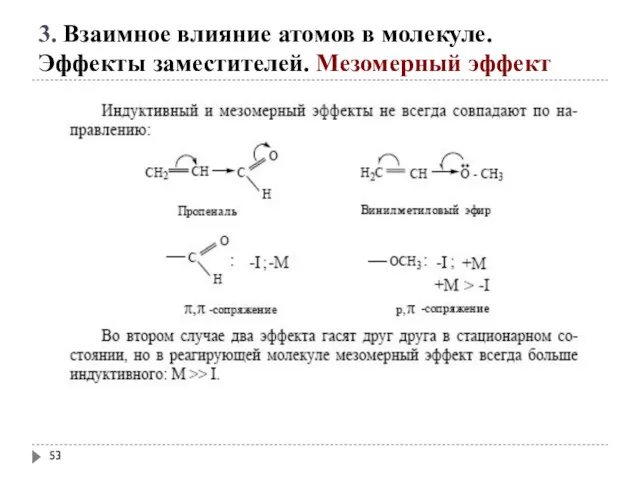
- 52. 3. Взаимное влияние атомов в молекуле. Эффекты заместителей. Мезомерный эффект
- 53. 3. Взаимное влияние атомов в молекуле. Эффекты заместителей. Мезомерный эффект
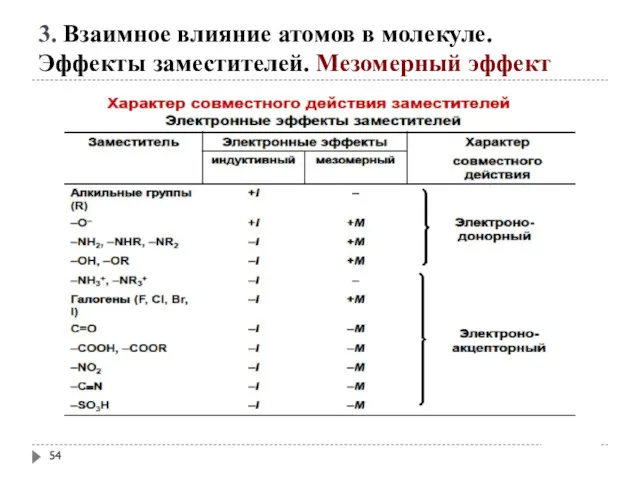
- 54. 3. Взаимное влияние атомов в молекуле. Эффекты заместителей. Мезомерный эффект
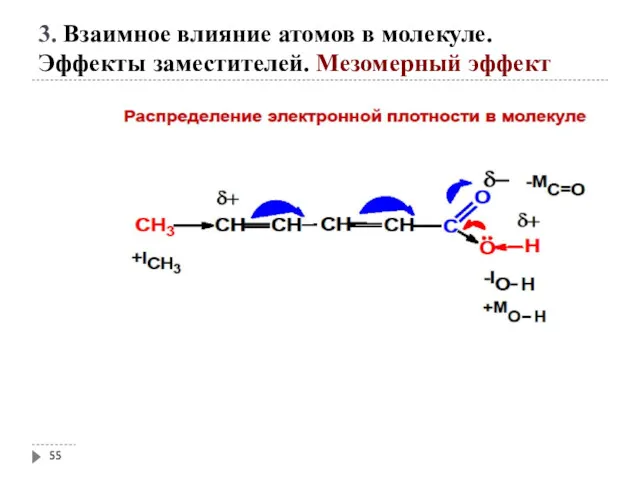
- 55. 3. Взаимное влияние атомов в молекуле. Эффекты заместителей. Мезомерный эффект
- 57. Скачать презентацию























 Галогены. Строение атомов фтора и хлора
Галогены. Строение атомов фтора и хлора Изомерия и ее виды
Изомерия и ее виды Химиялық тепе-теңдік
Химиялық тепе-теңдік Классификация опасных грузов
Классификация опасных грузов Химия 8 класс. Введение в химию
Химия 8 класс. Введение в химию Новинки СН старт: июль 2016 Профессиональная химия PRO service
Новинки СН старт: июль 2016 Профессиональная химия PRO service Кислородсодержащие соединения азота
Кислородсодержащие соединения азота Подгруппа азота
Подгруппа азота Зелёные камни
Зелёные камни Химия. Викторина
Химия. Викторина Материаловедение и технологии конструкционных материалов
Материаловедение и технологии конструкционных материалов Комплексные соединения
Комплексные соединения Элементы VIА группы
Элементы VIА группы Равновесные электрохимические системы
Равновесные электрохимические системы Молярный объем. Закон Авогадро
Молярный объем. Закон Авогадро Гидроксид магния. Mg(OH)2
Гидроксид магния. Mg(OH)2 Аналитическая химия. Предмет и задачи
Аналитическая химия. Предмет и задачи Дослідження швидкості росту кристалів від концентрації розчину
Дослідження швидкості росту кристалів від концентрації розчину Классификация химических реакций
Классификация химических реакций Карбоновые кислоты
Карбоновые кислоты Метал конструкциялық материалдар
Метал конструкциялық материалдар Вода на Земле. Строение молекулы воды
Вода на Земле. Строение молекулы воды Акриловые волокна
Акриловые волокна Природные каменные материалы. (Лекция 3)
Природные каменные материалы. (Лекция 3) Органическая химия в ряду других наук
Органическая химия в ряду других наук Обед под микроскопом. Минеральные вещества
Обед под микроскопом. Минеральные вещества Углерод и его соединения
Углерод и его соединения Классификация химических реакций
Классификация химических реакций