Содержание
- 2. Какие явления относятся к (Ф) физическим, а какие к (Х) химическим. кипение воды, образование на деревьях
- 3. ПРОВЕРИМ! Ф – 1, 2, 5, 8, 10 Х – 3, 4, 6, 7, 9 «5»
- 4. ПОВТОРИМ! Что такое химическая реакция? Перечислите признаки протекания химической реакции. Какие условия необходимы для возникновения химической
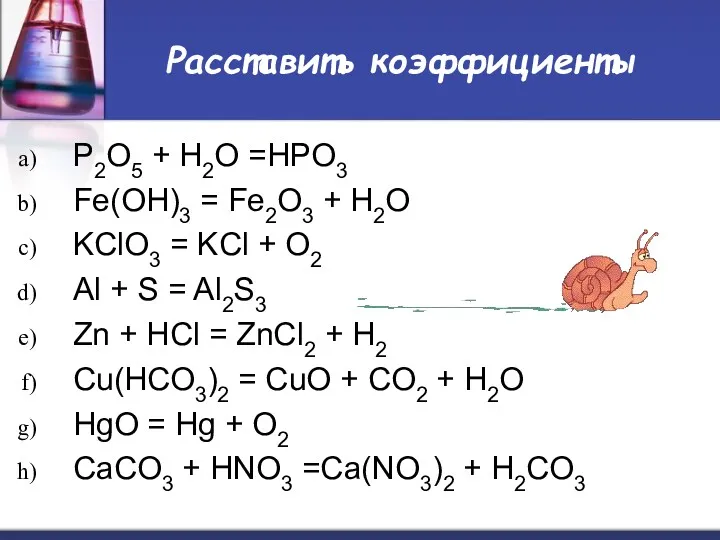
- 5. Расставить коэффициенты P2O5 + H2O =HPO3 Fe(OH)3 = Fe2O3 + H2O KClO3 = KCl + O2
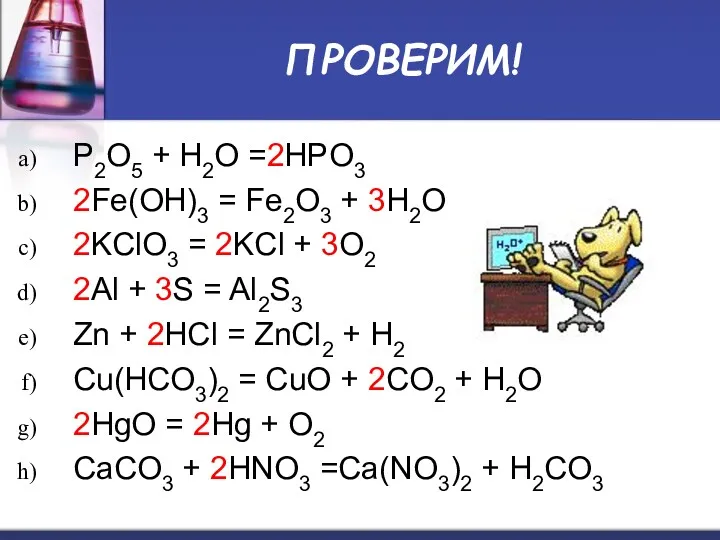
- 6. ПРОВЕРИМ! P2O5 + H2O =2HPO3 2Fe(OH)3 = Fe2O3 + 3H2O 2KClO3 = 2KCl + 3O2 2Al
- 7. Классификация – распределение объектов и явлений по классам, группам на основе их общих признаков.
- 8. Классификация химических реакций по числу и составу исходных и полученных веществ РЕАКЦИИ СОЕДИНЕНИЯ РЕАКЦИИ РАЗЛОЖЕНИЯ РЕАКЦИИ
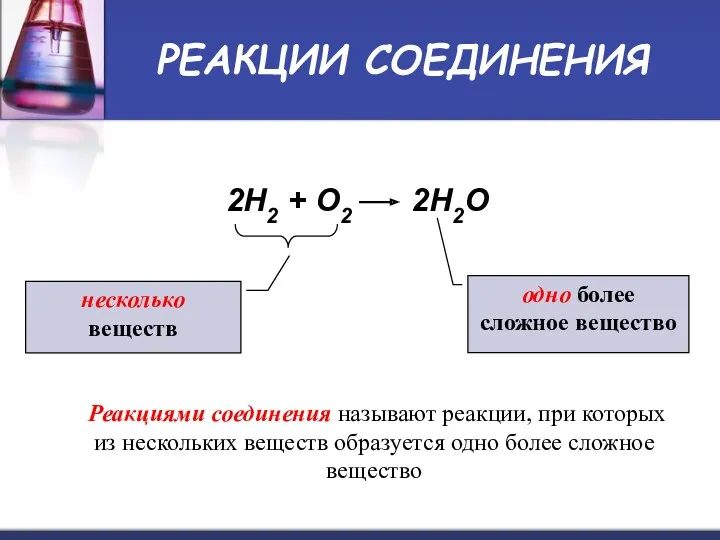
- 9. РЕАКЦИИ СОЕДИНЕНИЯ 2H2 + O2 2H2O несколько веществ одно более сложное вещество Реакциями соединения называют реакции,
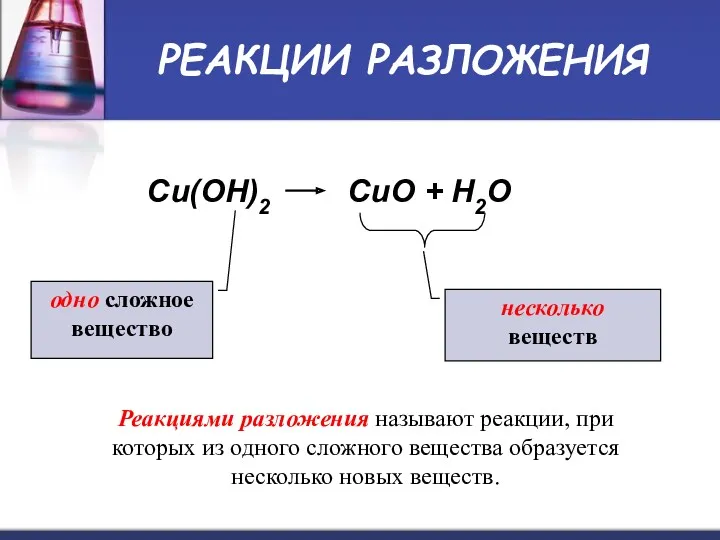
- 10. РЕАКЦИИ РАЗЛОЖЕНИЯ Cu(OH)2 CuO + H2O одно сложное вещество несколько веществ Реакциями разложения называют реакции, при
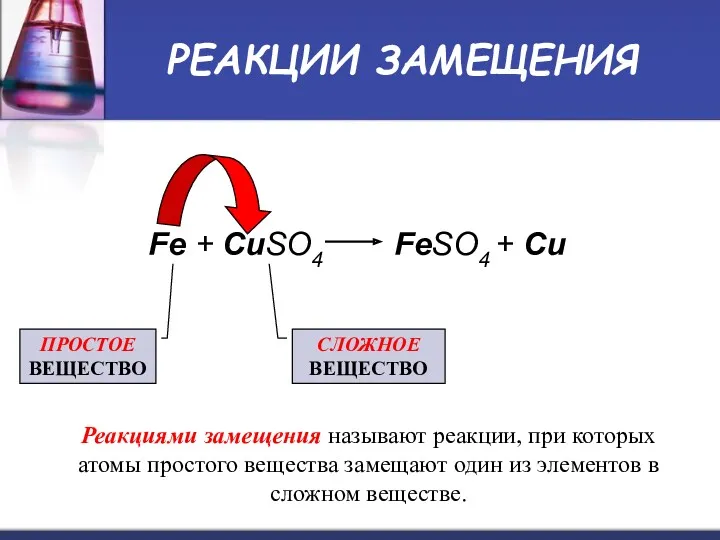
- 11. РЕАКЦИИ ЗАМЕЩЕНИЯ Fe + CuSO4 FeSO4 + Cu ПРОСТОЕ ВЕЩЕСТВО СЛОЖНОЕ ВЕЩЕСТВО Реакциями замещения называют реакции,
- 12. РЕАКЦИИ ОБМЕНА BaCl2+H2SO4 BaSO4+ 2HCl Реакциями обмена называют реакции, при которых два сложных вещества обмениваются своими
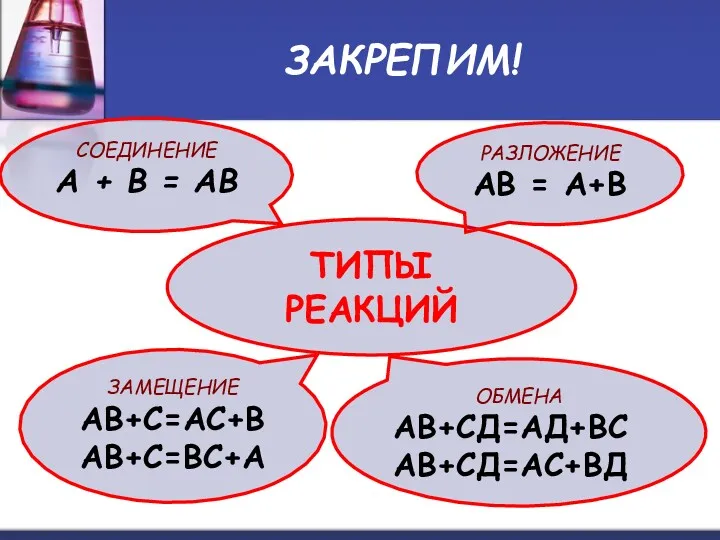
- 13. ЗАКРЕПИМ! ТИПЫ РЕАКЦИЙ РАЗЛОЖЕНИЕ АВ = А+В ЗАМЕЩЕНИЕ АВ+С=АС+В АВ+С=ВС+А ОБМЕНА АВ+СД=АД+ВС АВ+СД=АС+ВД СОЕДИНЕНИЕ А +
- 14. ЗАКРЕПИМ! P2O5 + H2O =2HPO3 2Fe(OH)3 = Fe2O3 + 3H2O 2KClO3 = 2KCl + 3O2 2Al
- 15. Указать тип химических реакций, расставить коэффициенты.
- 16. Дописать уравнение, указать тип реакций, расставить коэффициенты.
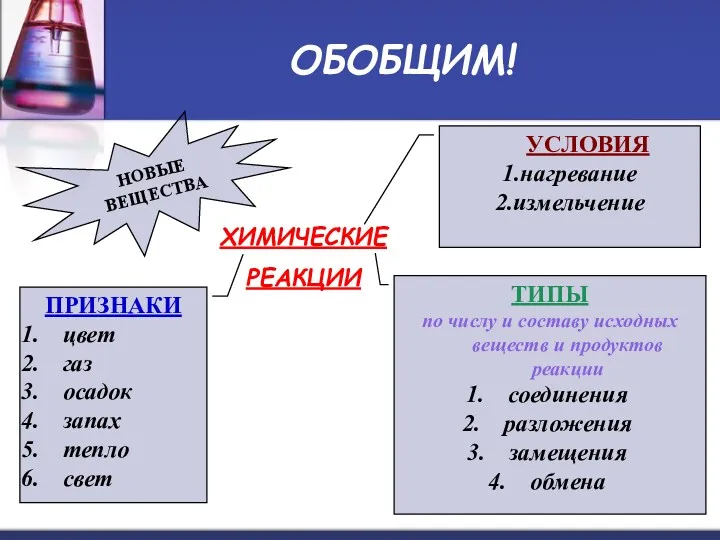
- 17. ОБОБЩИМ! ХИМИЧЕСКИЕ РЕАКЦИИ НОВЫЕ ВЕЩЕСТВА ПРИЗНАКИ цвет газ осадок запах тепло свет УСЛОВИЯ 1.нагревание 2.измельчение ТИПЫ
- 19. Скачать презентацию









 Спирты. Состав, строение спиртов
Спирты. Состав, строение спиртов Реакции ионного обмена
Реакции ионного обмена Аминокислоты – структурные единицы белков
Аминокислоты – структурные единицы белков Пурин нуклеозидтері (аденозии 3-фосфор қышқылы, рибоксии). Сапасына Қойылантын талаптар, талдау әдістері
Пурин нуклеозидтері (аденозии 3-фосфор қышқылы, рибоксии). Сапасына Қойылантын талаптар, талдау әдістері Химический диктант Алканы. Алкены
Химический диктант Алканы. Алкены Фракционная перегонка нефти
Фракционная перегонка нефти Жесткость воды
Жесткость воды Алкины
Алкины Общее понятие напряженно – деформированного состояния деталей машин из металлических материалов, применяемых в машиностроении
Общее понятие напряженно – деформированного состояния деталей машин из металлических материалов, применяемых в машиностроении Вода – это жизнь!
Вода – это жизнь! Электрохимические процессы. Лекция 7
Электрохимические процессы. Лекция 7 Сағыз пайдалы ма, әлде зиян ба?
Сағыз пайдалы ма, әлде зиян ба? Классификация химических реакций в органической и неорганической химии
Классификация химических реакций в органической и неорганической химии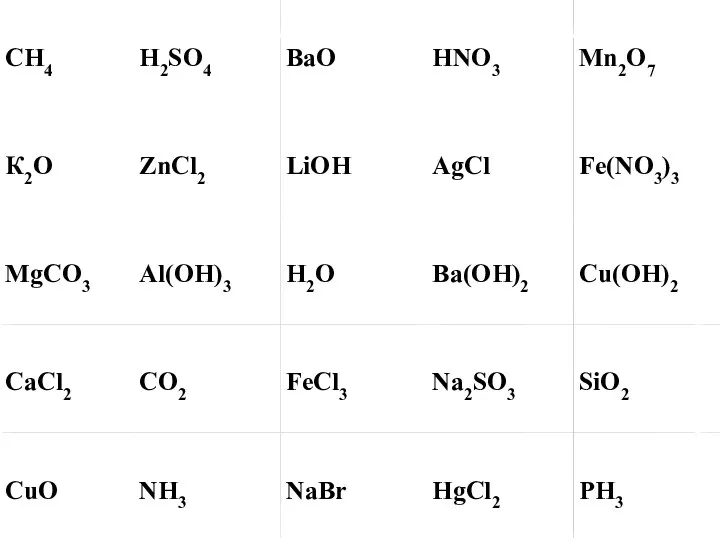 Химические реакции
Химические реакции Бытовая химия
Бытовая химия Углеводы: классификация, строение и физико-химические свойства
Углеводы: классификация, строение и физико-химические свойства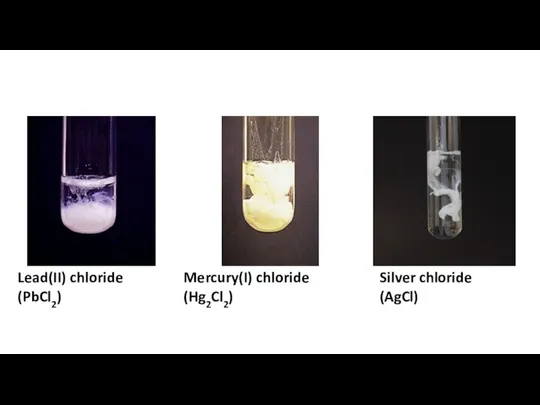 Separation amp confirmation
Separation amp confirmation Соляная кислота (HCI)
Соляная кислота (HCI) Гидролиз солей
Гидролиз солей Полимеры. Волокна
Полимеры. Волокна Окислительно - восстановительные реакции
Окислительно - восстановительные реакции Щелочные металлы и их соединения. 9 класс
Щелочные металлы и их соединения. 9 класс 20191107_binarnye_oksidy_1
20191107_binarnye_oksidy_1 Катиониты. Классификация катионитов
Катиониты. Классификация катионитов Калій. Знаходження в періодичній системі і основні характеристики
Калій. Знаходження в періодичній системі і основні характеристики Кислородсодержащие органические соединения. Лабораторная работа
Кислородсодержащие органические соединения. Лабораторная работа Бериллий, магний и щелочноземельные металлы
Бериллий, магний и щелочноземельные металлы Щелочные металлы
Щелочные металлы