Содержание
- 2. ДЕВИЗ «Никакое усвоение, воспроизведение и применение знаний без запоминания невозможно!»
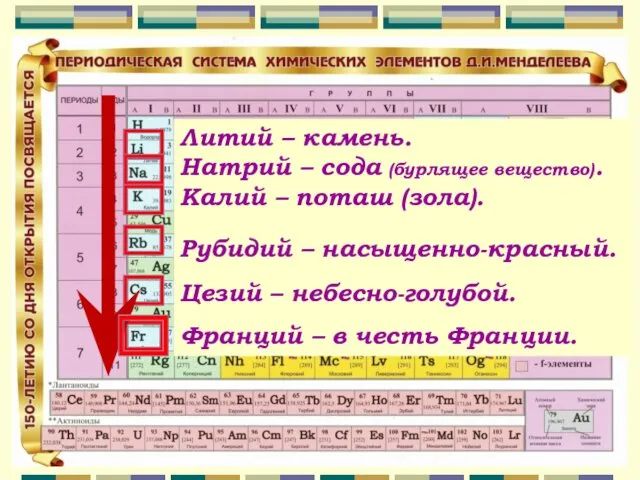
- 3. Литий – камень. Натрий – сода (бурлящее вещество). Калий – поташ (зола). Рубидий – насыщенно-красный. Цезий
- 4. ЩЕЛОЧНЫЕ МЕТАЛЛЫ это металлические элементы I-А группы (I группы, главной подгруппы): Li (литий), Na (натрий), K
- 5. КРАТКАЯ ИСТОРИЧЕСКАЯ СПРАВКА Натрий и калий были открыты английским учёным (физик, химик, агрохимик, изобретатель, один из
- 6. НАТРИЙ И КАЛИЙ В ПРИРОДЕ Из-за высокой активности в природе встречаются только в виде соединений.
- 7. Na K
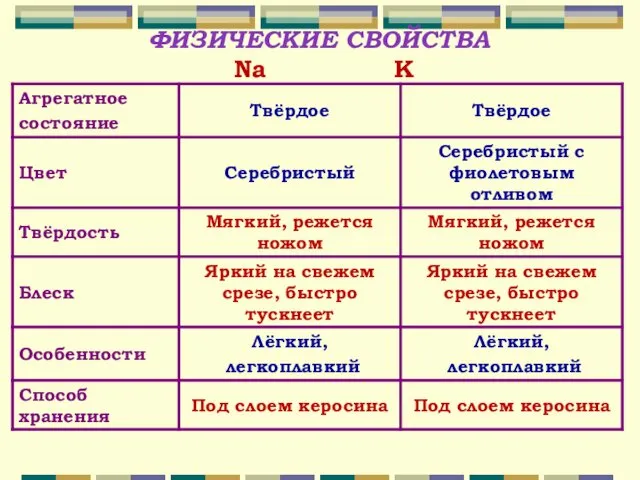
- 8. ФИЗИЧЕСКИЕ СВОЙСТВА Na K
- 9. ХИМИЧЕСКИЕ СВОЙСТВА Na – натрий K – калий
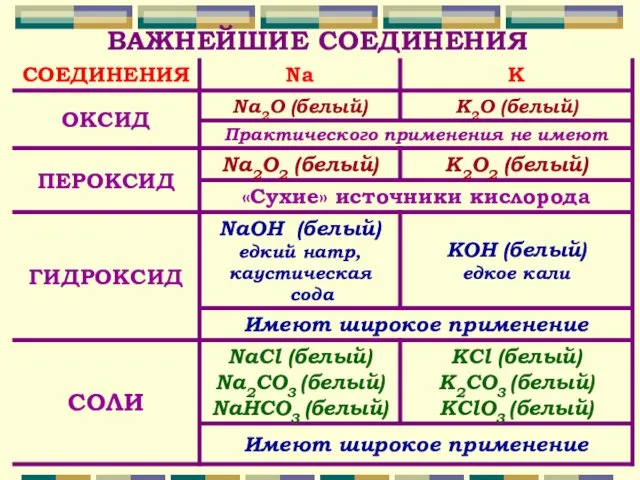
- 10. ВАЖНЕЙШИЕ СОЕДИНЕНИЯ
- 11. СОЕДИНЕНИЯ НАТРИЯ В БЫТУ ПИЩЕВАЯ СОЛЬ СОДА ПИЩЕВАЯ СОДА ТЕХНИЧЕСКАЯ СОДА КАУСТИЧЕСКАЯ или ЕДКИЙ НАТР NaCl
- 13. Скачать презентацию







 Топливо и топливосжигающие устройства
Топливо и топливосжигающие устройства большая стирка
большая стирка Бытовая химия. Правила безопасного обращения со средствами бытовой химии
Бытовая химия. Правила безопасного обращения со средствами бытовой химии Redox reactions
Redox reactions Железо. Fe (лат. Феррум)
Железо. Fe (лат. Феррум) Фармацевтическая химия натрия гидрокарбоната
Фармацевтическая химия натрия гидрокарбоната Решение задач в химии (ОГЭ, ЕГЭ, Олимпиады)
Решение задач в химии (ОГЭ, ЕГЭ, Олимпиады) Диссоциация воды. Водородный и гидроксильный показатели (рН и рОН)
Диссоциация воды. Водородный и гидроксильный показатели (рН и рОН) Теоретические аспекты химического осаждения из газовой фазы
Теоретические аспекты химического осаждения из газовой фазы Занимательные опыты
Занимательные опыты Валентність. Хімія. 7 клас
Валентність. Хімія. 7 клас Химические уравнения. Типы химических реакций. А что такое химическая реакция?
Химические уравнения. Типы химических реакций. А что такое химическая реакция? Электронные конфигурации атомов
Электронные конфигурации атомов Общая характеристика неметаллов
Общая характеристика неметаллов Кремний и его соединения
Кремний и его соединения Химия нефти и газа
Химия нефти и газа яжелые металлы полезны или вредны?
яжелые металлы полезны или вредны? Metal–metal multiple bonded intermediates in catalysis
Metal–metal multiple bonded intermediates in catalysis Закон сохранения массы веществ
Закон сохранения массы веществ Методические проблемы преподавания органической химии и ее основные теоретические понятия
Методические проблемы преподавания органической химии и ее основные теоретические понятия Щелочноземельные металлы
Щелочноземельные металлы Значення хімії у повсякденному житті
Значення хімії у повсякденному житті Неорганические строительные материалы. Стекло
Неорганические строительные материалы. Стекло Теория растворов электролитов и неэлектролитов
Теория растворов электролитов и неэлектролитов Химия и повседневная жизнь человека
Химия и повседневная жизнь человека Кремний и его соединения
Кремний и его соединения Химическая связь и ее типы
Химическая связь и ее типы Превращение веществ
Превращение веществ